Clear Sky Science · nl
Interactie van gepulseerd laagfrequent elektromagnetisch veld (PEMF) met mitochondriën
Zachte velden en de energiecentrales van de cel
Gepulseerde elektromagnetische veldtherapie (PEMF) wordt al in klinieken gebruikt om gebroken botten te helpen genezen, gewrichtspijn te verlichten en herstel na operaties te versnellen. Toch begrijpen we nog niet volledig hoe deze zachte, laagfrequente velden in ons lichaam werken. Deze studie stelt een fundamentele maar belangrijke vraag: beïnvloeden PEMF‑signalen mitochondriën direct — de kleine energiecentrales in onze cellen die het grootste deel van onze energie produceren — en zo ja, op welke manier?
Waarom mitochondriën belangrijk zijn voor alledaagse gezondheid
Mitochondriën zetten voedsel en zuurstof om in het molecuul ATP, de universele "energievaluta" van cellen. Als mitochondriën tekortschieten, genezen we langzamer, raken spieren sneller vermoeid en kunnen aandoeningen gerelateerd aan een verstoord metabolisme verergeren. Omdat eerder onderzoek suggereerde dat PEMF‑behandelingen het energiemetabolisme verbeteren en weefselherstel ondersteunen, richtten de auteurs zich erop of een specifiek PEMF‑apparaat de mitochondriale activiteit fijn kan afstemmen. Ze gebruikten een goed omschreven magnetisch signaal: korte, millisecondenlange pulsen van een 30 kHz sinusgolf met lage ingangsenergie, toegepast op spiercellen in kweek, op rattenweefsel en op gezuiverde mitochondriën.
Naar binnen kijken in levende cellen
In in het laboratorium gekweekte menselijke spiercellen maten de onderzoekers drie belangrijke indicatoren na PEMF‑blootstelling: het elektrische potentiaal over het inwendige mitochondriale membraan (een soort mini‑batterij), niveaus van reactieve zuurstofsoorten (hoge niveaus kunnen schadelijk zijn) en stikstofoxide, een gas dat mitochondriale respiratie tijdelijk kan blokkeren. Ongeveer 90 minuten na behandeling was het mitochondriale membraanpotentiaal iets lager, terwijl de stikstofoxideniveaus verminderd waren; reactieve zuurstofsoorten namen niet toe. Een kleine daling van het membraanpotentiaal kan wijzen op schade of op een verhoogde ATP‑productie. Omdat de cellen geen stresssignalen vertoonden, vermoedden de auteurs dat de mitochondriën gewoon iets harder werkten en daarmee de over het binnenmembraan opgeslagen spanning verbruikten.
Testen hoe mitochondriën "ademen"
Om dit idee directer te testen, doorboorden de onderzoekers voorzichtig het buitenste celmembraan zodat ze nauwkeurig verschillende brandstoffen aan de mitochondriën konden geven en het zuurstofgebruik konden meten. Ze zagen consequent een tendens naar hogere respiratie gekoppeld aan ATP‑productie na PEMF, vooral wanneer glutamaat, een veelvoorkomende mitochondriale brandstof, aanwezig was. Statistische analyse over veel monsters suggereerde dat de combinatie van PEMF‑blootstelling en de keuze van brandstof significant bepaalde hoe snel mitochondriën zuurstof verbruikten. Belangrijk is dat er geen aanwijzing was dat PEMF schadelijk was voor de cellen of hun mitochondriën. In plaats daarvan leken de velden selectief de "gekoppelde" modus van respiratie te stimuleren — waarbij zuurstofgebruik nauw verbonden is met ATP‑productie — zonder de verspilling door ontkoppelde verbranding van brandstof te verhogen.
Ontsteking, stikstofoxide en een verrassing van blauw licht
Aangezien stikstofoxide tijdens ontsteking kan ophopen en een sleutelstap in mitochondriale respiratie kan blokkeren, vroegen de onderzoekers zich af of PEMF mitochondriën kon helpen herstellen van zo’n remming. Ze voegden een chemische stikstofoxide‑donor toe aan gehomogeniseerd spier‑ en leverweefsel en aan geïsoleerde levermitochondriën, wat de respiratie sterk vertraagde. Onder deze omstandigheden herstelde PEMF de mitochondriale functie niet, zelfs niet bij sterk geconcentreerde mitochondriën. Om te zien of de blokkade überhaupt omkeerbaar was, bestraalden ze de door stikstofoxide geremde mitochondriën met blauw licht, een methode die bekend staat om stikstofoxide van zijn bindingsplaats los te maken. Blauw licht herstelde de respiratie deels, wat bevestigde dat het systeem kon terugveren, maar PEMF voegde geen extra voordeel toe. Dit toonde aan dat de positieve effecten van PEMF niet voortkomen uit het verwijderen van stikstofoxide onder ontstekingsachtige omstandigheden.
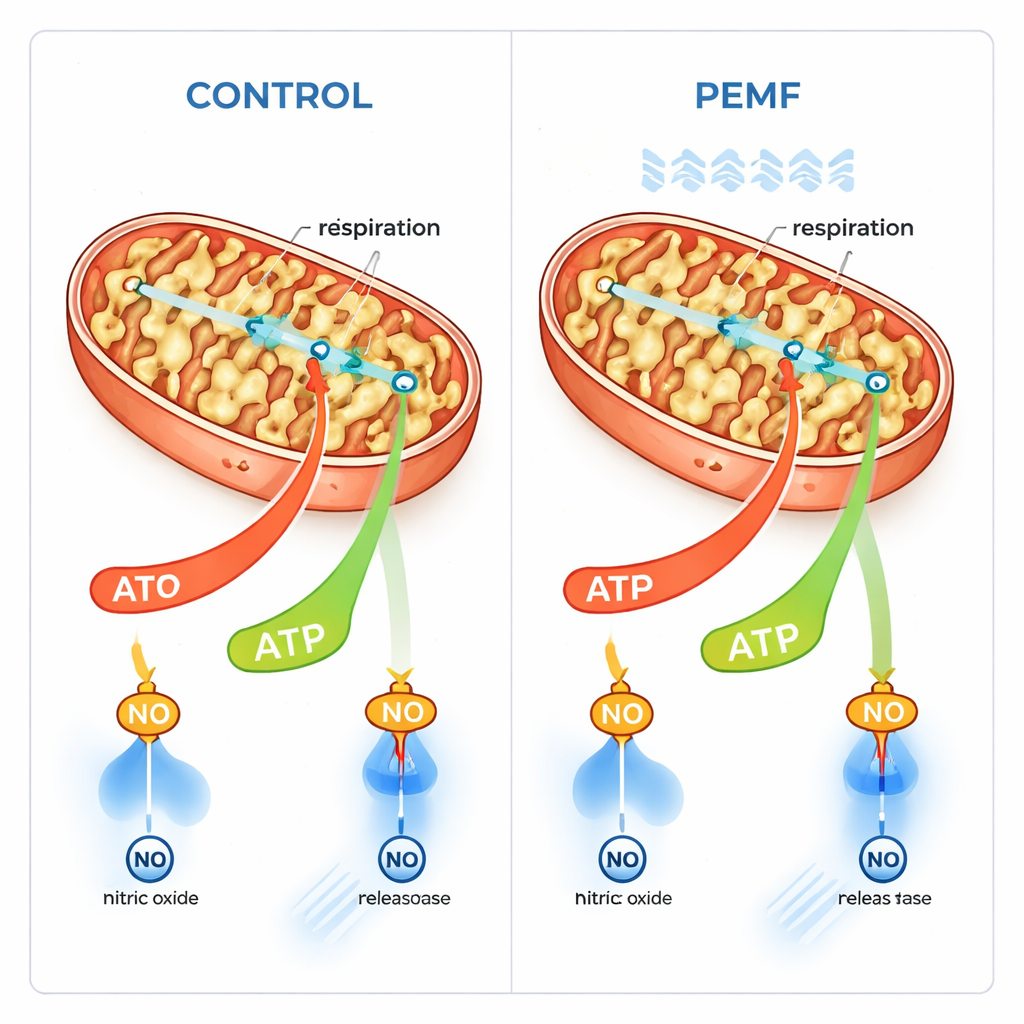
Membraanpoorten en energiestromen
Aan de hand van een analogie tussen cellen en elektrische circuits suggereren de auteurs dat PEMF voornamelijk op biologische membranen kan inwerken. Mitochondriën zijn omgeven door een buitenmembraan dat een belangrijke poorteiwit bevat, VDAC, dat energiegerelateerde moleculen in en uit laat. In tegenstelling tot het binnenmembraan met zijn zeer hoge spanning, heeft het buitenmembraan een kleinere, gemakkelijker beïnvloedbare spanning. De auteurs stellen voor dat PEMF dit buitenmembraanpotentiaal subtiel wijzigt, waardoor de openingsfrequentie van VDAC‑poorten verandert en zo de doorstroming van brandstof en verbruikte ATP over het membraan vergemakkelijkt. Dit zou op natuurlijke wijze de gekoppelde, ATP‑producerende modus van respiratie versterken zonder de maximale capaciteit van de elektronen‑transportketen zelf te veranderen.
Wat dit betekent voor toekomstige therapieën
Al met al levert de studie geen bewijs dat dit type PEMF schadelijk is voor mitochondriën. Integendeel, PEMF versterkt zachtjes het deel van de mitochondriale respiratie dat ATP produceert, terwijl de maximale respiratoire capaciteit en oxidatieve stress ongewijzigd blijven. Het herstelt echter geen mitochondriën die geblokkeerd zijn door hoge stikstofoxideniveaus, wat suggereert dat de voordelen in ontstoken weefsels via andere wegen moeten optreden. Voor patiënten en clinici ondersteunen deze resultaten het idee dat zorgvuldig afgestelde elektromagnetische velden de energiecentrales van de cel kunnen aansporen naar een efficiëntere, energieproducerende staat — een plausibele, mechanistische verklaring voor sommige van de herstellende effecten die worden gerapporteerd bij botgenezing, wondzorg en postoperatief herstel.
Bronvermelding: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Trefwoorden: gepulseerde elektromagnetische veldtherapie, mitochondriën, cellulaire energie, stikstofoxide, ATP‑productie