Clear Sky Science · nl
Validatie van een nieuw genomisch biomarker voor de schaalbaarheid van mesenchymale stamcellen en implicaties van genotype-status voor kenmerken van cellulaire veroudering
Waarom het kweken van stamcellen mettertijd moeilijker wordt
Stamcellen uit het volwassen beenmerg vormen de ruggengraat van veel experimentele therapieën, van het herstellen van beschadigde botten tot het dempen van ontsteking. Er zit echter een addertje onder het gras: om een patiënt te behandelen moeten laboratoria deze cellen buiten het lichaam laten groeien, en hoe langer ze worden uitgebreid, hoe meer ze vertragen en zich gedragen als "verouderde" cellen. Deze studie onderzoekt waarom de stamcellen van sommige mensen in een kweek langzaam verouderen, en of een klein ontbrekend stukje DNA onderzoekers kan helpen de meest robuuste cellen voor toekomstige behandelingen te selecteren.
Een ontbrekend gen dat de regels verandert
De onderzoekers richtten zich op een gen genaamd GSTT1, dat cellen helpt schadelijke moleculen te ontgiften die tijdens normaal metabolisme en stress ontstaan. Verrassend genoeg ontbreekt dit gen bij een aanzienlijk deel van de mensen volledig – zij zijn "GSTT1 null." Eerder werk suggereerde dat beenmergstamcellen van deze personen mogelijk sneller groeien en hun beschermende chromosoomuiteinden, telomeren genoemd, langer behouden. In dit project onderzocht het team stamcellen van zes gezonde donoren, verdeelde ze in GSTT1-positief en GSTT1-nul, en volgde vervolgens het gedrag van de cellen tijdens vele kweekrondes en na blootstelling aan röntgenstraling, een sterke trigger van cellulaire veroudering.
Snel delende cellen die bestendiger zijn tegen verouderingssignalen
Toen de wetenschappers de aantallen cellen over meerdere dagen volgden, deelden GSTT1-nul stamcellen zich in vroege passages sneller dan cellen met het gen. Bij zeer langdurige uitbreiding werden de groeisnelheden tussen de groepen meer vergelijkbaar, maar het vroege voordeel was duidelijk. Om veroudering direct te onderzoeken gebruikte het team een klassieke kleuring die senescente, of "oude", cellen blauw kleurt. Na vele delingsrondes, en opnieuw na bestraling, bevatten GSTT1-nul culturen consequent minder blauwe, senescente cellen dan GSTT1-positieve culturen. Belangrijk is dat dit verschil niet voortkwam uit langzamere verkorting van telomeren of uit hogere activiteit van het enzym dat telomeren onderhoudt (hTERT); beide metingen leken vergelijkbaar ongeacht GSTT1-status, wat suggereert dat een ander mechanisme werkzaam is.
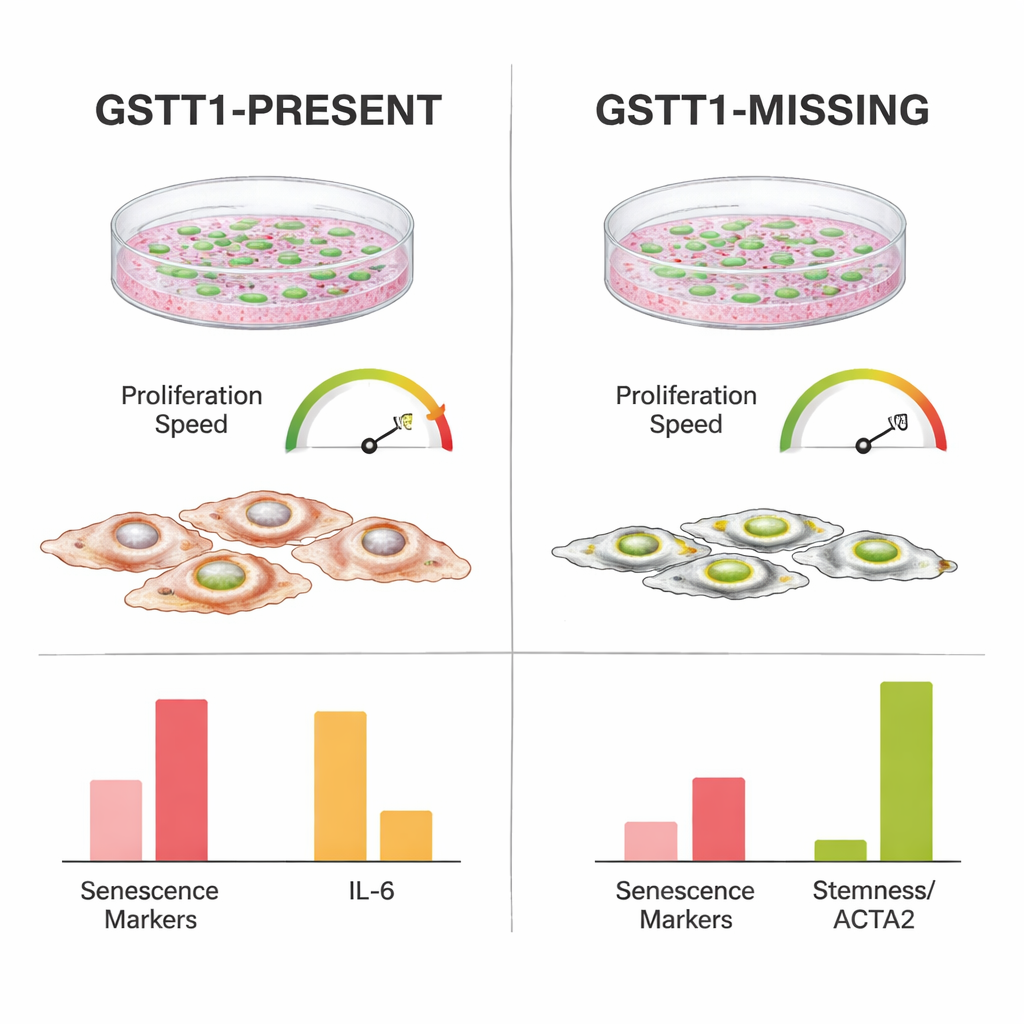
Rustiger stress- en ontstekingsprofiel in de kweek
Om te begrijpen wat GSTT1-nul cellen veerkrachtiger maakte, maten de onderzoekers de activiteit van genen die verband houden met celcyclusstop, DNA-schade en het zogenaamde senescentie-geassocieerde secretiefenotype — een cocktail van ontstekings- en stresssignalen die verouderende cellen afgeven. Cellen met GSTT1 vertoonden hogere niveaus van belangrijke "stop"-signalen zoals p21 en p14, vooral in latere passages en na bestraling. Ze verhoogden ook sterker IL-6, een krachtig ontstekingsmolecuul, en andere stressgerelateerde genen dan GSTT1-nul cellen. Daarentegen behielden GSTT1-nul stamcellen lagere niveaus van deze verouderings- en ontstekingsmarkers, terwijl ze hogere niveaus van ACTA2 en TWIST1 aanhielden, genen die geassocieerd zijn met structurele integriteit en stamcelachtig gedrag. Opvallend is dat beide genotypen een vergelijkbaar vermogen behielden om zich te differentiëren in bot- en vetcellen, wat betekent dat het beschermende effect niet louter te wijten was aan verlies van normale stamcelfunctie.
Wat dit kan betekenen voor toekomstige celtherapieën
Gezamenlijk suggereren de bevindingen dat beenmergstamcellen zonder GSTT1 gedeeltelijk beschermd zijn tegen de gebruikelijke slijtage door kweekuitbreiding en bestraling. Ze groeien vroeg in de kweek sneller, hopen minder duidelijke verouderde cellen op en behouden een minder inflammatoir profiel, ondanks dat hun chromosomen in vergelijkbare mate verkorten. Voor bedrijven en klinieken die grote aantallen stamcellen produceren kan GSTT1-nul status dienen als een praktisch genetisch kenmerk om donoren te identificeren wiens cellen beter bestand zijn tegen uitbreiding, wat mogelijk consistentere en krachtigere therapieën oplevert. Natuurlijk gebruikte de studie een kleine donorpopulatie en niet-klinische kweekcondities, dus zijn grotere, zorgvuldig gecontroleerde studies nodig. Desalniettemin benadrukt het werk hoe een enkele erfelijke variatie het verschil kan maken tussen jeugdige en verouderende eigenschappen in stamcellen die voor regeneratieve geneeskunde worden gekweekt.
Bronvermelding: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Trefwoorden: mesenchymale stamcellen, cellulaire veroudering, biomarkers, productie van celtherapieën, GSTT1-polymorfisme