Clear Sky Science · nl
Een klinisch toepasbaar en generaliseerbaar deep learning-model voor anterieure mediastinale tumoren in CT-beelden over meerdere instellingen
Waarom het opsporen van zeldzame borsttumoren belangrijk is
De meesten van ons zullen het woord "anterieure mediastinale tumor" nooit in een spreekkamer horen, juist omdat deze gezwellen—vaak met de thymus voor het hart betrokken—zeldzaam zijn. Wanneer ze wel voorkomen, zijn ze moeilijk te herkennen en nog moeilijker nauwkeurig te meten op CT-scans; dat zijn taken die meestal specialisten in grote kankercentra vereisen. Deze studie onderzoekt of een zorgvuldig getraind systeem voor kunstmatige intelligentie (AI) artsen in veel ziekenhuizen kan helpen deze lastige tumoren op routinematige CT-beelden betrouwbaar te vinden en af te lijnen, wat mogelijk de diagnose en behandelingsplanning verbetert voor patiënten die anders over het hoofd gezien zouden worden.
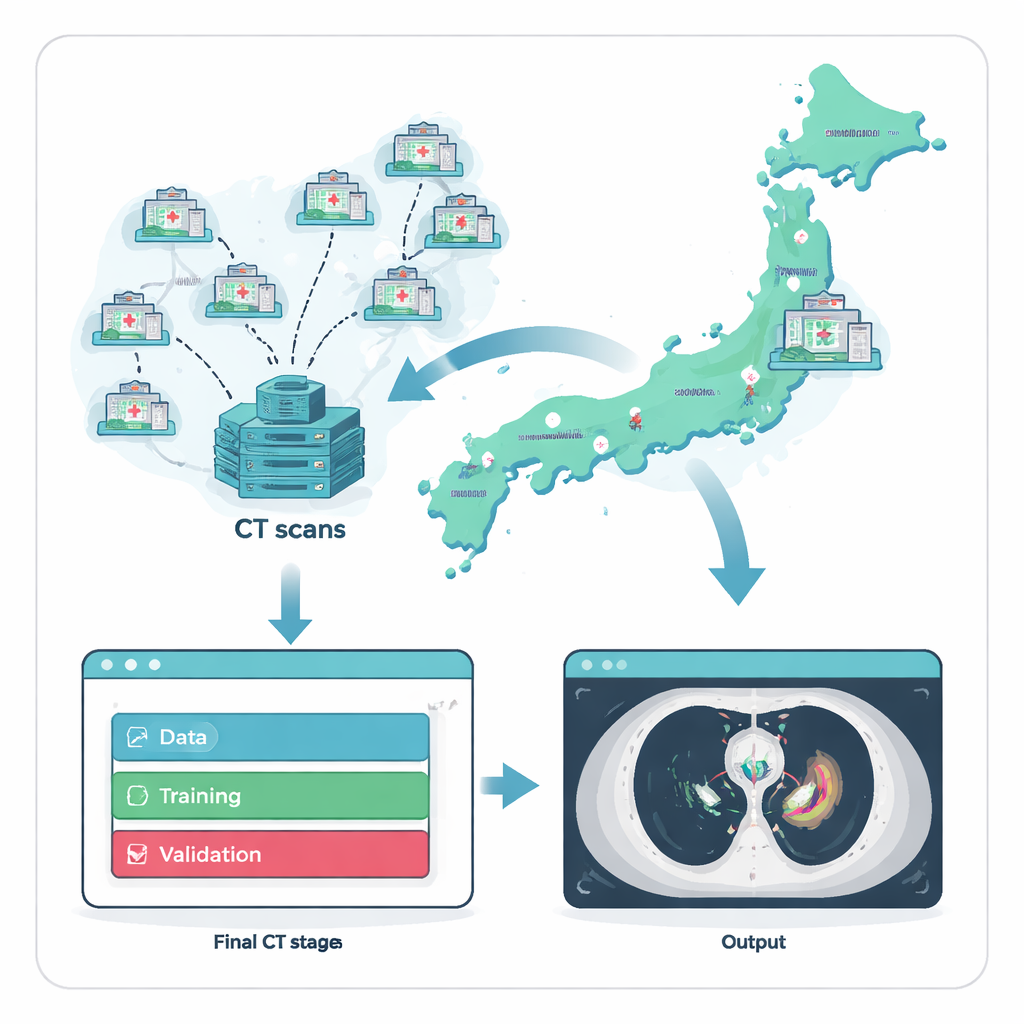
Schaarse gevallen verzamelen uit het hele land
Aangezien anterieure mediastinale tumoren weinig voorkomen, is de eerste uitdaging simpelweg voldoende voorbeelden te vinden om een AI-systeem te trainen. De onderzoekers losten dit op door samen te werken met het National Cancer Center Hospital van Japan en 135 verwijzende ziekenhuizen in het hele land. Over twee decennia verzamelden ze 711 borst-CT-scans, elk van een andere volwassen patiënt waarvan de tumordiagnose microscopisch bevestigd was. Om een eerlijke en realistische test te garanderen, splitsten ze de data in drie groepen: een grote set voor training, een kleinere set voor fijnregeling, en een volledig aparte externe testset van 164 scans afkomstig uit 121 ziekenhuizen die geen trainingsbeelden bijdroegen. Deze strikte scheiding bootst na hoe het systeem zou presteren wanneer het in nieuwe ziekenhuizen wordt geïntroduceerd die het nog nooit "gezien" heeft.
Scans omzetten in betrouwbaar lesmateriaal
Een AI-model is slechts zo goed als de voorbeelden waarvan het leert, dus het team investeerde fors in deskundige annotatie. Voor elke CT-scan tekenden specialisten de exacte grenzen van tumoren in het voorste deel van de borstkas. Een thoracale chirurg of radiologietechnoloog maakte de eerste contouren, die vervolgens werden gecontroleerd door twee ervaren diagnostische radiologen. Eventuele meningsverschillen werden opgelost door overleg, waardoor een referentie van hoge kwaliteit ontstond die weerspiegelt hoe experts de beelden in de praktijk zouden interpreteren. Met behulp van een commercieel no-code AI-platform bouwden en trainden clinici—zonder computercode te schrijven—een driedimensionaal model om deze expertcontouren na te bootsen, zodat medisch personeel direct de ontwikkeling kon sturen.
Hoe de AI tumoren in drie dimensies ziet
De kern van het systeem is een 3D-versie van een neurale netwerkarchitectuur bekend als U-Net, ontworpen om hele CT-volumes te analyseren in plaats van losse plakjes. Het neemt een stapel borstbeelden en voorspelt voor elk klein volume-element of het tot tumor of normaal weefsel behoort, waardoor als het ware een 3D-masker over de tumor wordt geschilderd. Tijdens de training werd het model blootgesteld aan willekeurige rotaties, herschaling en bijsnijden van beelden zodat het robuust wordt tegen kleine verschillen in patiëntpositie en scannersettings. De onderzoekers maten vervolgens hoe nauwkeurig de door het model voorspelde tumorregio’s overeenkwamen met de experttekeningen, met behulp van standaard overlap-scores die zowel nauwkeurige begrenzing als volledige dekking van het tumorvolume waarderen.
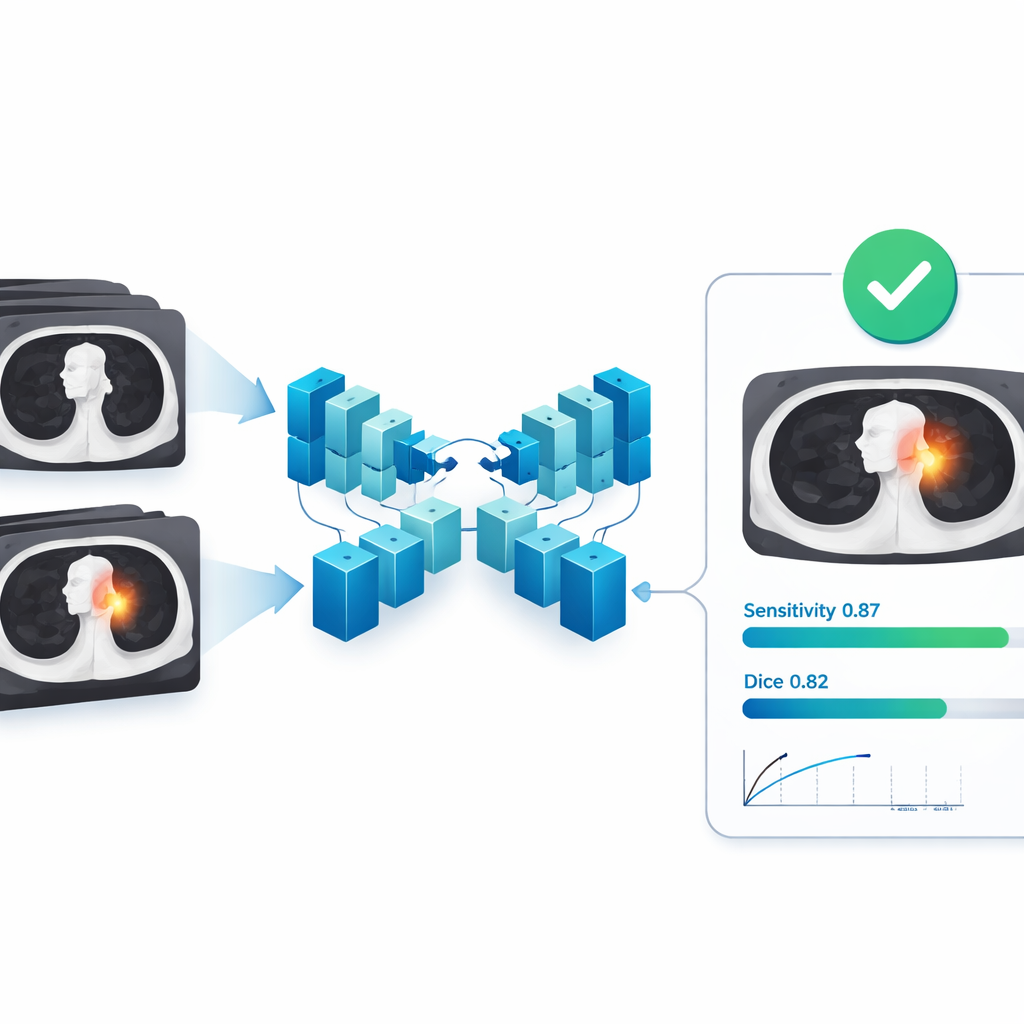
Prestaties over veel ziekenhuizen en tumortypes
Op de externe testset uit 121 onafhankelijke ziekenhuizen liet het AI-model een sterke overeenstemming zien met de expertsegmentaties. Gemiddeld was de overlapscore (Dice) 0,82, met een gerelateerde maat genaamd Intersection over Union van 0,72; precisie en recall lagen beide rond 0,82–0,85, wat betekent dat het model zelden normaal weefsel als tumor aanmerkte en het grootste deel van het tumormateriaal succesvol vastlegde. Belangrijk is dat deze resultaten standhielden over verschillende scanfabrikanten, tumorgroottes en tumortypes, wat suggereert dat het systeem kan omgaan met de variatie die in de klinische praktijk voorkomt. Wanneer het model werd geëvalueerd als detector—simply of het elke laesie überhaupt vindt—bereikte het een sensitiviteit van ongeveer 0,87, zelfs onder een strikte matchingsregel, met ruim onder één vals alarm per scan gemiddeld, een profiel dat bijzonder aantrekkelijk is voor ondersteuning bij kankerpopulatiescreening.
Waar het systeem helpt en waar mensen cruciaal blijven
Een nadere blik op successen en mislukkingen toonde een duidelijk patroon: de AI presteerde het beste bij grotere tumoren en had moeite met zeer kleine of zwakke laesies, waarbij het ze deels miste of nabijgelegen normale structuren zoals bloedvaten of vochtcollecties verwarde. Dit komt overeen met de dagelijkse ervaring in de radiologie, waar kleine of laagcontrastbevindingen het gemakkelijkst over het hoofd worden gezien. De auteurs betogen daarom dat het hulpmiddel het best in een "human-in-the-loop"-setting wordt gebruikt. Het kan dienen als een efficiënte eerste beoordelaar die waarschijnlijke tumoren markeert en hun grenzen aftekent, en zo kant-en-klare volumes levert voor taken zoals behandelingsplanning en chirurgie, terwijl radiologen hun aandacht richten op het dubbel controleren van kleine, subtiele of ambiguïte gebieden.
Wat dit betekent voor patiënten en toekomstige hulpmiddelen
Voor een leek is de kernboodschap dat een AI-systeem dat getraind is op een zeldzame maar ernstige groep borsttumoren artsen betrouwbaar kan helpen deze kankers op CT-scans te vinden en af te lijnen, zelfs in ziekenhuizen die nooit data aan de training hebben bijgedragen. Door nauwkeurige 3D-tumorkaarten te leveren en het aantal valse alarmen laag te houden, kan het model de diagnose versnellen, nauwkeurigere stralings- en chirurgische planning ondersteunen en een extra veiligheidsnet bieden tegen gemiste laesies. Tegelijkertijd benadrukt het werk dat AI geen vervanging is voor deskundig oordeel—vooral niet bij de kleinste en zwakste tumoren—maar een veelbelovende assistent die krachtiger wordt naarmate clinici, beeldvormingsdata en gebruiksvriendelijke AI-platforms samenkomen.
Bronvermelding: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
Trefwoorden: anterieure mediastinale tumoren, deep learning in CT-beeldvorming, medische beeldsegmentatie, ondersteuning bij kankerdiagnose, radiologie kunstmatige intelligentie