Clear Sky Science · nl
Het medicijn resmetirom voor metabool disfunctie-geassocieerde steatohepatitis (MASH) vertoont brede activiteit op nucleaire receptoren met minimale functionele impact
Waarom een nieuw levermedicijn ertoe doet
Wereldwijd leven miljoenen mensen met een gevaarlijke vorm van leververvetting die nu metabool disfunctie–geassocieerde steatohepatitis heet, ofwel MASH. De aandoening kan jaren stilletjes de lever beschadigen en uiteindelijk leiden tot littekenvorming, leverfalen of kanker. In 2024 werd een geneesmiddel genaamd resmetirom het eerste middel dat in de Verenigde Staten specifiek voor MASH werd goedgekeurd. Deze studie behandelt een cruciale vraag voor patiënten en artsen: werkt resmetirom precies op zijn bedoelde doel in de lever, of raakt het ook andere moleculaire schakelaars die de voordelen kunnen verminderen of bijwerkingen kunnen veroorzaken?
Een gerichte manier om levervet te verbranden
Resmetirom is ontworpen om te werken als een gefocuste versie van het natuurlijke schildklierhormoon. Schildklierhormonen regelen hoe snel onze cellen energie gebruiken en beïnvloeden hartslag, lichaamstemperatuur en de verwerking van vet en suiker. Ze werken via twee verwante receptoren, alpha en beta. De beta-vorm komt het meest voor in de lever, terwijl de alpha-vorm domineert in het hart en het bot. Bij mensen met MASH is de schildklierhormoonsignalisatie in de lever vaak traag, zelfs als bloedtesten normaal lijken. Resmetirom is bedoeld om de beta-receptor in levercellen te "herwekken" zodat er meer vet wordt verbrand, cholesterol wordt afgebroken en vetopslag vermindert, terwijl de alpha-receptor wordt gespaard om hart- en botbijwerkingen te vermijden. 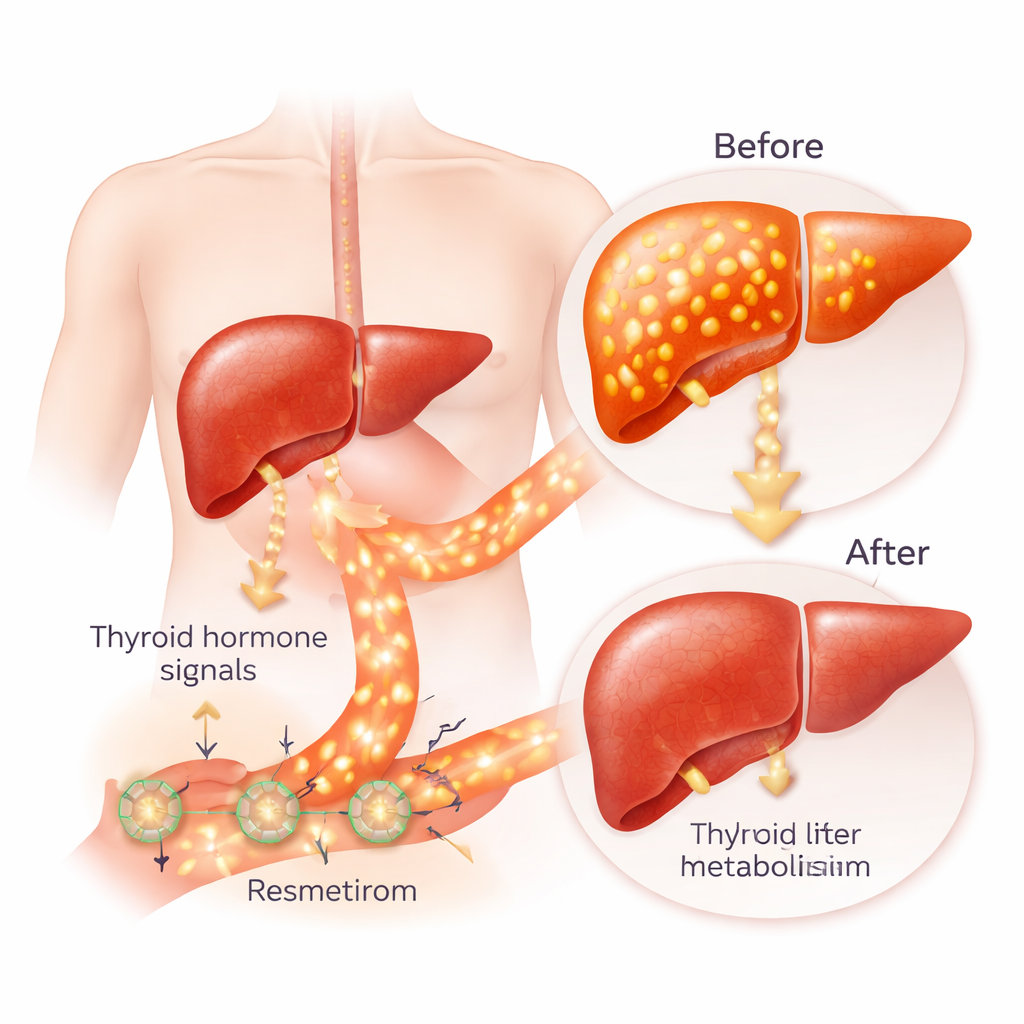
Controleren op ongewenste moleculaire doelen
Aangezien resmetirom relatief hoge doses moet krijgen om effectief te zijn, vroegen de auteurs zich af of het ook aan andere nucleaire receptoren kan binden—eiwitten in de celkern die als hoofdschakelaars fungeren voor metabolisme, ontgifting en dagelijkse biologische ritmes. Met computermodellering en een reeks celgebaseerde rapportagetests controleerden ze eerst of resmetirom zich gedroeg als bepaalde afbraakproducten van schildklierhormoon die een andere receptor, PPARγ, activeren. De modellering suggereerde dat resmetirom, ondanks vergelijkbare vormen, slecht in het bindingsvak van PPARγ zou passen, en de celtesten bevestigden dat resmetirom deze receptor niet activeerde.
Off-target treffers, maar gedempte effecten
Vervolgens screenden de onderzoekers resmetirom tegen een breder paneel van nucleaire receptoren die betrokken zijn bij vet- en glucosehuishouding. Zoals verwacht activeerde resmetirom de schildklierhormoon beta-receptor sterker dan de alpha-versie. Het middel ging echter ook interacties aan met meerdere andere receptoren: het remde een receptor genaamd CAR, verlaagde de basale activiteit van drie ROR-receptoren en dempte bescheiden een leverbeschermende factor bekend als HNF4α. Op papier zouden deze off-target acties zorgwekkend kunnen zijn, omdat al deze schakelaars helpen bij het regelen van levermetabolisme en ontgifting. Toch waren de sterkte van deze effecten slechts matig, en vaak gedeeltelijk, wat suggereert dat resmetirom deze receptoren duwt in plaats van ze volledig om te schakelen.
Het medicijn testen in realistischer levercellen
Om te zien of deze off-target interacties onder meer levensechte omstandigheden van belang zijn, gebruikten de onderzoekers menselijke leverkankercellen die vaak dienstdoen als model voor leverweefsel. Ze maten de activiteit van sleutelgenen die bekendstaan om te reageren op schildklierhormoon evenals op CAR, RORs en HNF4α. Resmetirom verhoogde genen die betrokken zijn bij glucoseproductie en ontgifting in een patroon dat overeenkomt met de werking van schildklierhormoon, ondanks dat de off-target acties sommige van die genen de andere kant op hadden moeten duwen. Toen de wetenschappers vetopslag in deze cellen opwekten, verminderden zowel resmetirom als natuurlijk schildklierhormoon duidelijk de vetophoping, terwijl middelen die specifiek ROR, CAR of HNF4α targetten weinig effect hadden. 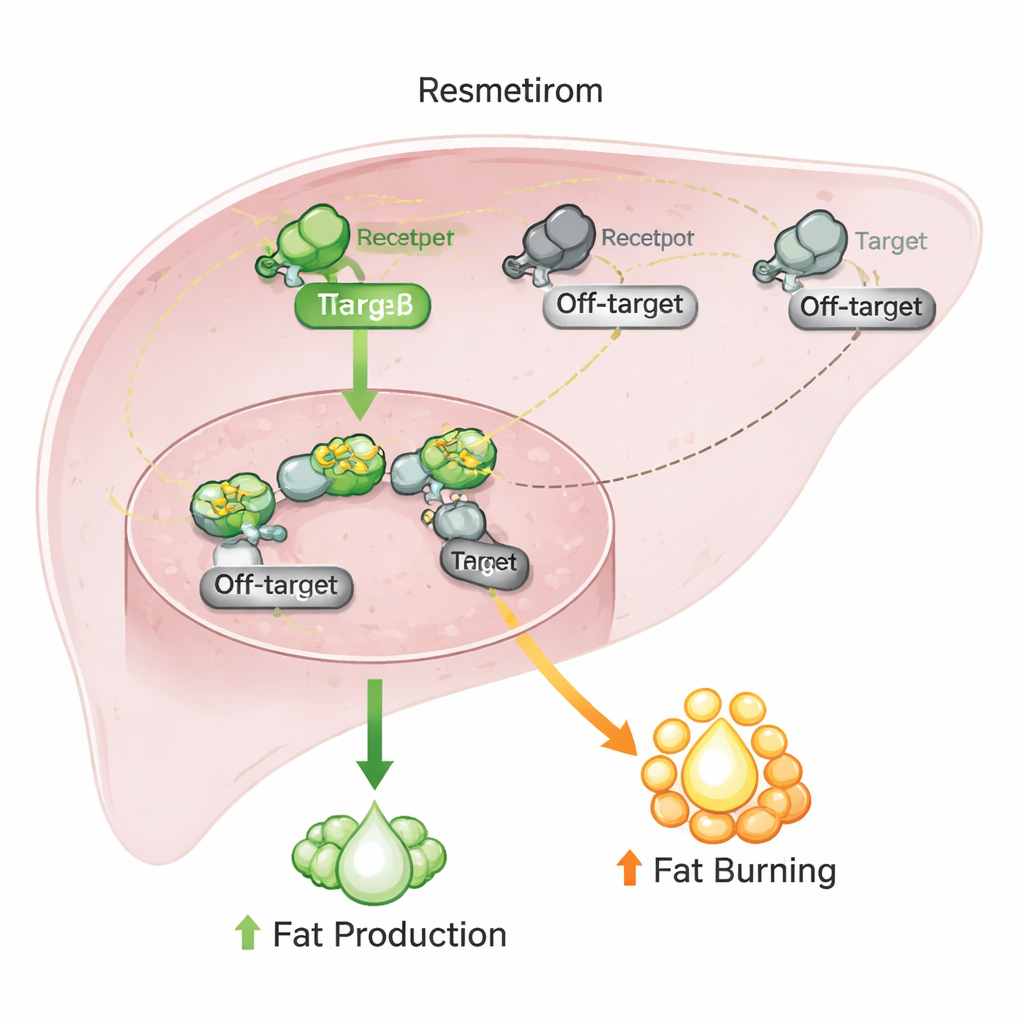
Wat dit betekent voor patiënten en toekomstige geneesmiddelen
Samengevat suggereren de bevindingen dat resmetirom inderdaad meerdere andere nucleaire receptoren raakt, maar dat het hoofdwerkingsmechanisme in levercellen nog steeds door de bedoelde schildklierhormoon beta-receptor wordt gedreven. Praktisch gezien betekent dit dat het vermogen van het middel om levervet te verlagen en de levergezondheid bij MASH te verbeteren waarschijnlijk niet door deze nevenactiviteiten wordt ondermijnd, althans in de onderzochte experimentele systemen. Het werk benadrukt ook een bredere les: omdat resmetirom slechts matig krachtig is, zijn relatief hoge concentraties nodig om te werken, wat de kans op subtiele off-target effecten elders in het lichaam vergroot. Dat maakt het des te belangrijker om toekomstige, op schildklierhormoon gebaseerde geneesmiddelen te ontwikkelen die de beta-receptor strakker en selectiever binden, zodat dezelfde of betere levervoordelen bij lagere doses en met nog minder onbedoelde moleculaire interacties worden bereikt.
Bronvermelding: Kärcher, A., Isigkeit, L., Bandomir, N.C. et al. The metabolic dysfunction-associated steatohepatitis (MASH) drug resmetirom exhibits broad nuclear receptor activity with minimal functional impact. Sci Rep 16, 4083 (2026). https://doi.org/10.1038/s41598-026-37494-y
Trefwoorden: leververvetting, MASH, resmetirom, schildklierhormoonreceptor, levermetabolisme