Clear Sky Science · nl
Vloeibare biopsie van plasma en urine cfDNA onderscheidt glioma‑recidief van radiation brain necrosis in preklinische modellen
Waarom een eenvoudige bloed‑ en urinetest hersentumorpatiënten kan helpen
Voor mensen die behandeld zijn voor hersentumoren is een van de meest angstaanjagende vragen na bestraling of een nieuwe plek op een scan betekent dat de kanker terug is, of dat het hersenweefsel simpelweg door de behandeling is littekengeslagen. Deze twee mogelijkheden lijken op standaard MRI‑beelden bijna identiek, maar vragen om heel verschillende beslissingen: agressievere therapie versus afwachtend beleid. Deze studie bij ratten onderzoekt of fragmenten DNA die in bloed en urine circuleren een eenvoudige, niet‑invasieve manier kunnen bieden om het verschil te zien, mogelijk patiënten te besparen van risicovolle hersenbiopsieën en artsen te helpen de juiste vervolgstap te kiezen.
De uitdaging van het lezen van hersenscans na behandeling
Gliomen behoren tot de dodelijkste hersentumoren, met hoge recidiefkansen zelfs na operatie, bestraling en chemotherapie. Wanneer een behandeld gebied op de MRI opnieuw oplicht, kan dat duiden op ofwel tumorgroei ofwel radiation brain necrosis, een vertraagde vorm van weefselafsterving veroorzaakt door hoge‑dosis bestraling. Beide toestanden kunnen zwelling, neurologische klachten en vergelijkbare scanpatronen veroorzaken. Tegenwoordig vertrouwen artsen vaak op langdurige beeldopvolging of invasieve chirurgische biopsieën om vast te stellen welk proces zich voordoet. Deze benaderingen zijn traag, riskant en soms onduidelijk, wat een dringende behoefte schept aan een veiliger, eerder en betrouwbaarder onderzoek.
Op zoek naar aanwijzingen in vrij rondzwervend DNA
Onze cellen laten voortdurend kleine stukjes genetisch materiaal los, zogenoemd cell‑free DNA, in lichaamsvloeistoffen zoals bloed en urine. Tumoren en beschadigde weefsels zetten nog meer van deze fragmenten vrij. De onderzoekers richtten zich op twee specifieke signalen: B1‑SINE, een veelvoorkomende repetitieve DNA‑sequentie die het algemene cell‑free DNA in knaagdierbloed weerspiegelt, en mitochondriaal DNA (mtDNA), dat afkomstig is van de energiecentrales van de cel en kan lekken wanneer cellen gestrest zijn of afsterven. Omdat bloedafnames en urineverzameling veel makkelijker en veiliger zijn dan hersenbiopsieën, zijn deze markers veelbelovende kandidaten voor een “vloeibare biopsie” — een test die moleculaire informatie uit vloeistoffen leest in plaats van uit weefsel.
Het bouwen van ratmodellen om menselijke ziekte te imiteren
Om dit idee onder gecontroleerde omstandigheden te testen, zette het team twee afzonderlijke ratmodellen op. In de ene groep implanteren ze gliomacellen in de hersenen, lieten een tumor groeien, verwijderden die chirurgisch en volgden de dieren totdat de tumor terugkwam — een nabootsing van menselijk glioma‑recidief. In een andere groep gebruikten ze zorgvuldig geplande, hoge dosis bestraling gericht op één zijde van de hersenen om vertraagde radiation necrosis te veroorzaken, als spiegel van een ernstige complicatie die bij patiënten voorkomt. In de weken daarna verzamelden ze bloed en urine, bepaalden B1‑SINE‑ en mtDNA‑niveaus met een gevoelige DNA‑versterkingstechniek en bevestigden hersenveranderingen met MRI‑scans en weefselanalyse onder de microscoop.
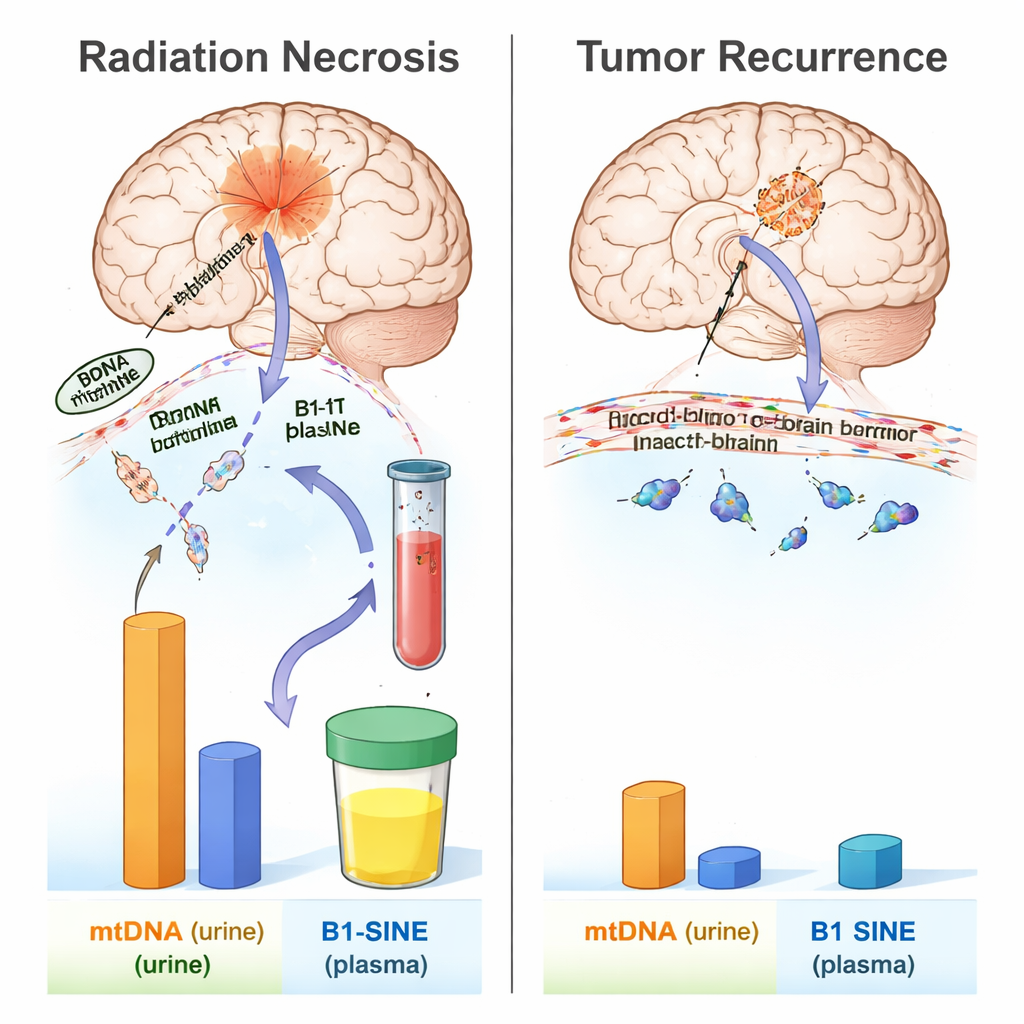
Kenmerkende DNA‑handtekeningen voor stralingsschade
De patronen van DNA‑fragmenten in vloeistoffen bleken opvallend verschillend tussen de twee toestanden. Na bestraling steeg het urine‑mtDNA binnen 24 uur, keerde kort terug naar bijna normaal en nam daarna weer toe rond week zes, met een piek in week acht en een aanhoudende verhoging naarmate radiation necrosis zich ontwikkelde. Plasma B1‑SINE‑waarden schoten ook omhoog na bestraling, met een duidelijke piek in week acht en blijvend hoge waarden van week acht tot zestien, het venster waarin weefselafsterving zichtbaar was in hersenscans en pathologie. Daarentegen lieten ratten met terugkerende glioma geen significante veranderingen zien in zowel urine‑mtDNA als plasma B1‑SINE vergeleken met gezonde en sham‑operatie controles in dezelfde periode. Dit suggereert dat door bestraling beschadigd hersenweefsel een karakteristieke golf van DNA‑fragmenten in de circulatie vrijgeeft die in dit model niet wordt nagebootst door tumorhergroei.
Wat dit voor toekomstige patiënten kan betekenen
Voor leken is de kernboodschap dat eenvoudige bloed‑ en urinetests artsen mogelijk kunnen helpen behandelgerelateerde hersenbeschadiging te onderscheiden van terugkerende kanker zonder de schedel te openen. In deze ratexperimenten stegen twee signalen — mtDNA in urine en B1‑SINE in bloed — duidelijk alleen wanneer radiation necrosis aanwezig was, niet wanneer de tumor terugkwam. Hoewel verder onderzoek nodig is in grotere studies en bij menselijke patiënten, en de exacte drempels en mensspecifieke markers nog moeten worden vastgesteld, wijst dit onderzoek op een toekomst waarin een “vloeibare momentopname” van circulerend DNA de follow‑up van hersentumoren kan sturen, onzekerheid kan verminderen en persoonlijker, minder invasieve zorg kan ondersteunen.
Bronvermelding: Sun, J., Jin, C., Chen, Y. et al. Liquid biopsy of plasma and urinary CfDNA differentiates glioma recurrence from radiation brain necrosis in preclinical models. Sci Rep 16, 7123 (2026). https://doi.org/10.1038/s41598-026-37493-z
Trefwoorden: glioma, radiation necrosis, liquid biopsy, cell-free DNA, brain tumor monitoring