Clear Sky Science · nl
Uitzonderlijk selectieve blokkering van spanningssensoren van NaV1.5-kanalen door Mg-protoporfyrine remt migratie van kankercellen
Plantpigment wijst op een nieuwe kankerstrategie
Onze harten en onze tumoren delen mogelijk een onverwachte kwetsbaarheid: een speciaal soort elektrisch poortje in het celmembraan dat NaV1.5 wordt genoemd. Deze studie laat zien dat een natuurlijke verwant van de bouwstenen van chlorofyl in planten, magnesium‑protoporfyrine IX (MgPpIX), dit poortje met buitengewone precisie kan uitschakelen. Daarmee vertraagt het duidelijk de beweging van bepaalde kankercellen—wat suggereert dat een door fotosynthesechemie geïnspireerd molecuul metastase kan temmen zonder de hersenen of spieren sterk te verstoren.
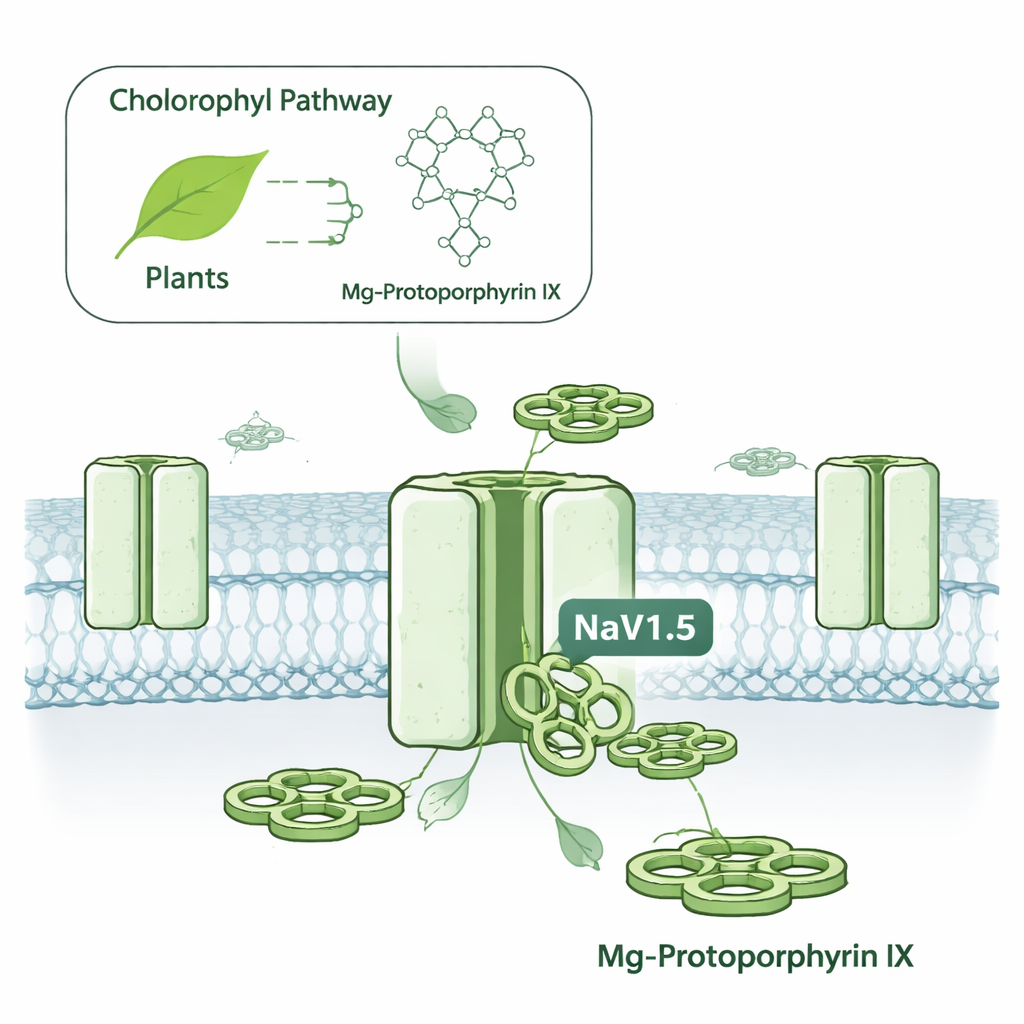
Een verborgen elektrische schakelaar in kankercellen
Cellen gebruiken spanningsafhankelijke natriumkanalen als kleine deurtjes die openen en sluiten om geladen deeltjes door te laten en elektrische signalen te genereren. NaV1.5 is vooral bekend door zijn rol in hartslagen, waar het helpt elke contractie te initiëren. Maar hetzelfde kanaal komt ook voor in verschillende kankers, waaronder borst- en dikkedarmtumoren, waar de activiteit ervan in verband is gebracht met verhoogde celbeweging en invasiviteit. Het richten op NaV1.5 is lastig geweest omdat de meeste natriumkanaalmiddelen ook verwante kanalen in zenuwen en skeletspieren aantasten, met risico op bijwerkingen zoals convulsies, gevoelloosheid of spierzwakte. De auteurs wilden ontdekken of kleine moleculen NaV1.5 met veel grotere selectiviteit van zijn verwanten konden onderscheiden.
Een door planten geïnspireerde remmer met recordprecisie
Het team onderzocht een familie ringvormige moleculen genaamd metaalprotoporfyrines, die lijken op de kernen van heem in bloed en chlorofyl in planten, maar verschillende centrale metaalatomen bevatten. Toen zij verschillende varianten toepasten op menselijke NaV1.5-kanalen die in gekweekte cellen werden geproduceerd, stak één verbinding eruit: MgPpIX. Die verminderde de elektrische stroom door NaV1.5 met ongeveer 99% bij nanomolaire concentraties, ruwweg 100 keer krachtiger dan een op ijzer gebaseerde tegenhanger (hemin). Andere metalen varianten, zoals die met nikkel of koper, waren in wezen inactief. Opmerkelijk genoeg liet MgPpIX meerdere andere menselijke natriumkanaaltypes (gebruikt door de hersenen, perifere zenuwen en skeletspier) bij dezelfde doses volledig ongemoeid, waardoor de selectiviteit één van de scherpste is die ooit voor deze kanaalfamilie is gerapporteerd.
Hoe het molecuul een kleine spanningshefboom blokkeert
Om deze ongebruikelijke precisie te doorgronden combineerden de onderzoekers genetische wijziging met computersimulaties. Natriumkanalen bestaan uit vier herhalende delen, elk met een "spanningssensor" die van positie verschuift wanneer het membraanpotentiaal verandert. Door individuele aminozuren tussen NaV1.5 en zijn ongevoelige familieleden te wisselen, bracht het team MgPpIX’ werking terug tot de spanningssensor in het tweede domein, met name twee residuen die naar buiten zijn blootgesteld. Moleculaire dynamicasimulaties in een realistische membraanumgeving suggereerden dat MgPpIX zich tegen deze sensor nestelt wanneer deze in zijn rustende, "naar beneden" positie verkeert. Het positief geladen metaalcentrum van MgPpIX wordt aangetrokken door een negatief geladen zijketen op het kanaal, terwijl de platte ring interactie aangaat met omliggende lipiden. Deze binding lijkt de spanningssensor op zijn plaats te vergrendelen, zodat hij niet naar de actieve "omhoog"-toestand kan bewegen en het kanaal gesloten blijft. Interessant genoeg kunnen sterke depolarisaties—zoals tijdens een hartslag—het molecuul tijdelijk losmaken, een gedrag dat de auteurs beschrijven als "reverse use-dependence."
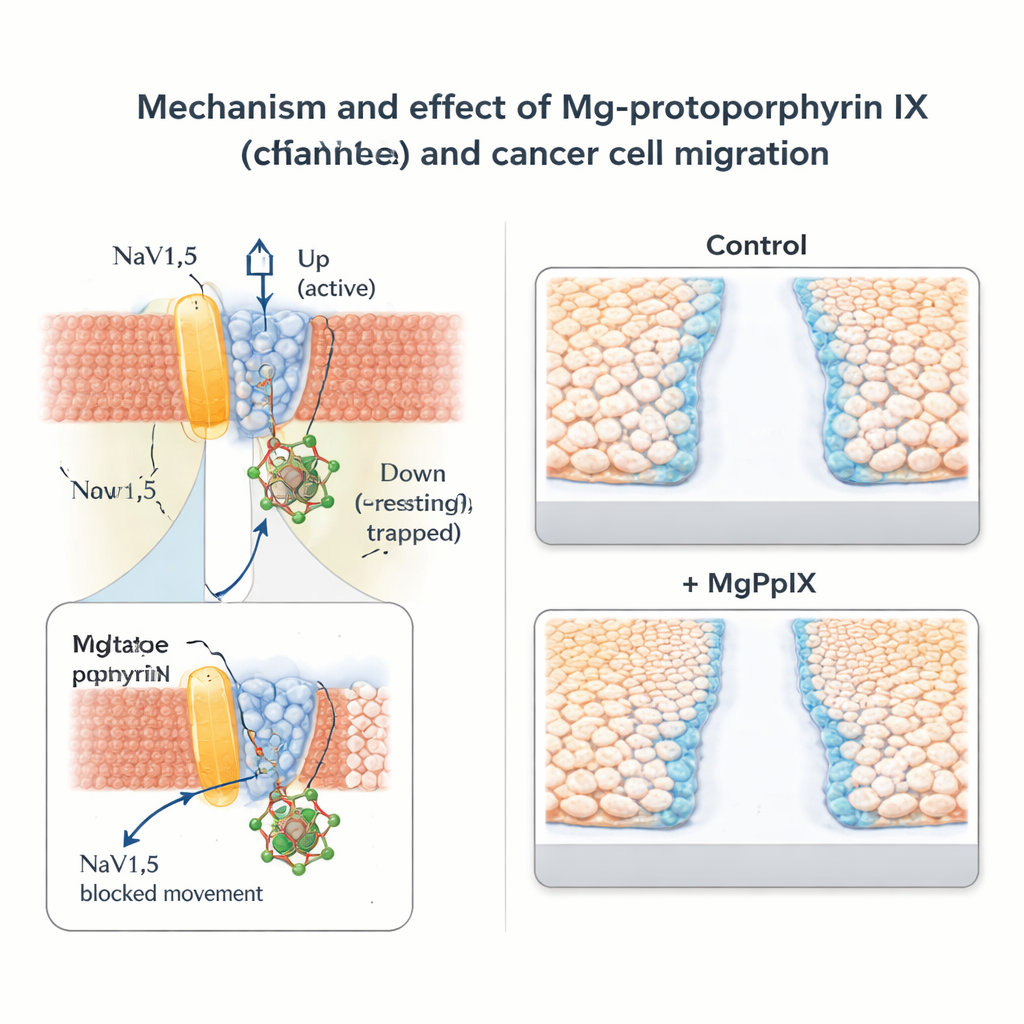
Het vertragen van kankercelmigratie zonder algemene zenuwblokkade
Vervolgens onderzocht het team wat deze moleculaire rem betekent voor kankergedrag. In borstkanker- (MDA-MB-231) en dikkedarmkanker- (SW-480) cellijnen die van nature NaV1.5 tot expressie brengen, verminderde MgPpIX de natriumstromen drastisch en vertraagde het de celmigratie in standaard "scratch"- en transwell-assays. Hoe sterker een gegeven metaalprotoporfyrine NaV1.5 blokkeerde, hoe meer het de celbeweging belemmerde, wat de koppeling tussen kanaalactiviteit en mobiliteit versterkt. Daarentegen reageerden kankercellijnen zonder NaV1.5 niet op MgPpIX, noch elektrisch noch in migratietests, wat ondersteunt dat het effect hoogst specifiek is en niet algemeen toxisch. Vergeleken met het klassieke natriumkanaalgif tetrodotoxine bereikte MgPpIX sterkere onderdrukking van migratie bij veel lagere concentraties.
Belofte en voorzichtigheid voor toekomstige anti-metastatische geneesmiddelen
Voor de niet‑specialist is de kernboodschap dat de onderzoekers een plantaardig verwant molecuul hebben gevonden dat als een precisieklem werkt op een hart‑type elektrisch poortje dat door sommige kankers is gekaapt. Door de kleine spanningshefboom van het poortje in zijn rustpositie vast te zetten, kan MgPpIX de mobiliteit van kankercellen in het lab sterk beperken terwijl andere natriumkanalen die essentieel zijn voor gevoel en beweging ongemoeid blijven. Omdat de snelle elektrische activiteit van het hart deze blokkade deels kan opheffen, kan er zelfs een veiligheidsvenster bestaan waarbij tumorcellen meer worden geremd dan hartcellen. Hoewel MgPpIX zelf mogelijk nog niet klaar is als medicijn, bieden de unieke bindingsplaats en het mechanisme een krachtig stappenplan voor het ontwerpen van toekomstige geneesmiddelen gericht op het stoppen van kankeruitzaaiing door NaV1.5 met ongekende selectiviteit aan te pakken.
Bronvermelding: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Trefwoorden: natriumkanalen, Nav1.5, migratie van kankercellen, chlorofyl-afgeleide moleculen, gerichte ionkanaalmedicatie