Clear Sky Science · nl
MiniPromoters Ple384 (TH) en Ple388 (PITX3) voor het richten op midbrain-dopaminerge neuronen bij muizen en apen
Waarom dit onderzoek van belang is voor de hersengezondheid
De dopamine-producerende cellen in de hersenen helpen ons bewegen, leren van beloningen en gemotiveerd blijven. Het zijn ook de cellen die afsterven bij de ziekte van Parkinson. Wetenschappers en artsen willen graag nuttige genen of moleculaire hulpmiddelen specifiek aan deze kwetsbare neuronen leveren, zowel in proefdieren als op een dag bij mensen. Het aansturen van gentherapie zodat die alleen in de juiste cellen aangaat en niet overal in de hersenen, is echter een belangrijke hindernis geweest. Deze studie beschrijft twee nieuwe, compacte DNA-"schakelaars" die betrouwbaar genen bijna uitsluitend in midbrain-dopaminerge neuronen van muizen en apen kunnen inschakelen, wat een weg opent naar preciezere en mogelijk veiligere behandelingen.
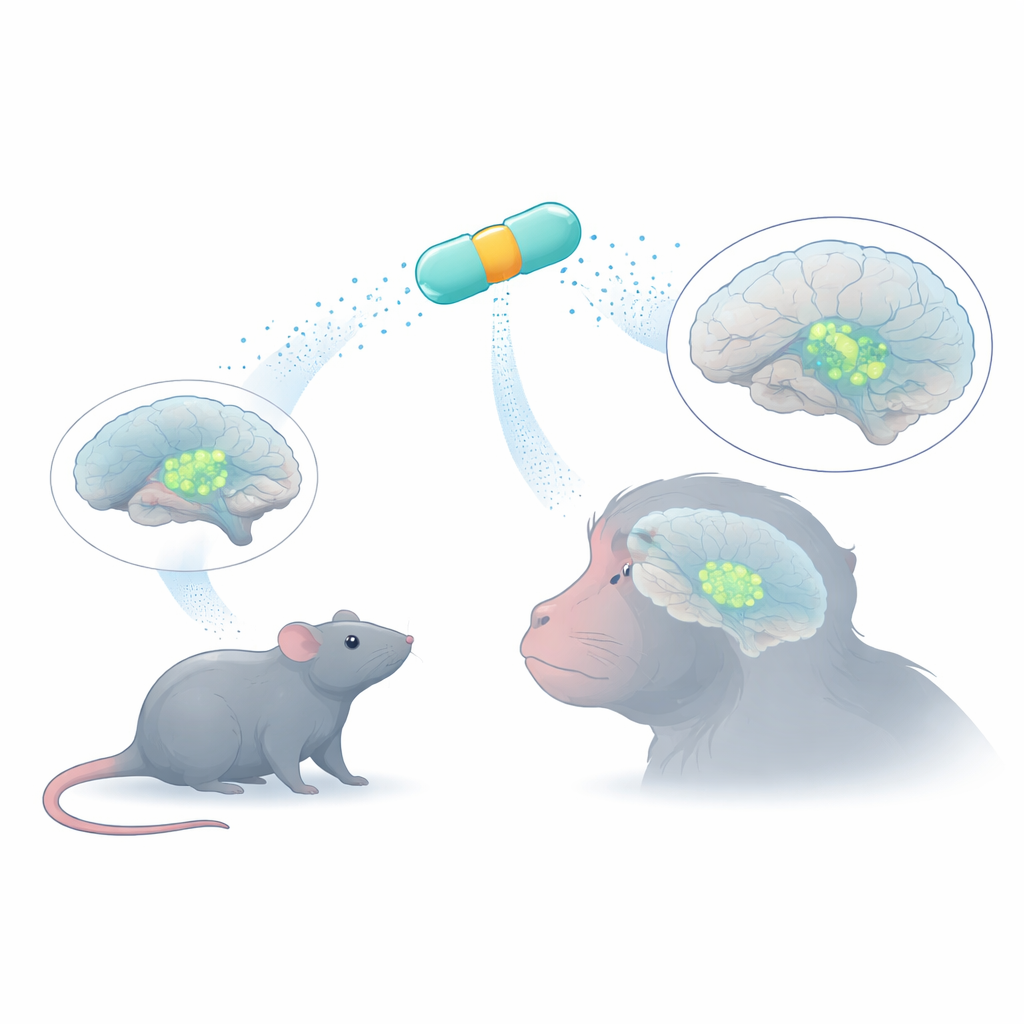
Kleine genetische schakelaars met een grote taak
Om een therapeutisch gen in hersencellen te krijgen, gebruiken onderzoekers vaak adeno-geassocieerde virussen (AAV's), onschadelijke vervoermiddelen die slechts een beperkte hoeveelheid DNA kunnen dragen. Binnen elk virus fungeert een korte promotorsequentie als een aan‑/uit‑schakelaar die bepaalt waar dat gen actief zal zijn. Veel natuurlijke promotoren zijn te groot of te ongericht en zetten genen aan in te veel celtypes. Het team gebruikte bio-informatica om acht zeer compacte "MiniPromoters" uit menselijk DNA te ontwerpen—korte combinaties van controle-elementen afkomstig van genen die bekendstaan als merkers van dopamineproducerende neuronen. Hun doel was een set schakelaars die in AAV's pasten en toch krachtige, celspecifieke expressie aandreven.
Het vinden van de juiste doelen in de muizenhersenen
De acht kandidaat‑MiniPromoters werden eerst in muizen getest. Elke promotor werd in een AAV geplaatst dat een groen fluorescerend eiwit droeg, zodat de onderzoekers konden zien waar de schakelaar actief was. Ze leverden de virussen ofwel in de bloedbaan of direct in de met vloeistof gevulde ruimten van de hersenen. De meeste MiniPromoters bleken niet selectief: sommige verlichtten veel niet‑dopaminerge cellen, andere werkten vrijwel niet. Twee staken er met kop en schouders bovenuit. De ene, Ple384 genoemd, was opgebouwd uit controlegebieden van het gen voor tyrosinehydroxylase, het sleutelenzym dat door alle catecholamine‑producerende neuronen wordt gebruikt. De andere, Ple388, kwam van PITX3, een gen dat cruciaal is voor een subset van midbrain-dopaminerge neuronen. Zowel Ple384 als Ple388 gaven heldere, sterk begrensde signalen in de substantia nigra compacta en het ventrale tegmentale gebied—de midbrain-kernen van dopamine-neuronen—waarbij meer dan 90% van de gemarkeerde cellen ook het kenmerkende dopaminemolecuul droeg.
Van muizen naar apen zonder diep in de hersenen te boren
Elke gentherapie die gericht is op menselijke ziekte moet uiteindelijk werken in primaten, waarvan de hersenen groter en complexer zijn. Rechtstreekse injectie in de substantia nigra is technisch veeleisend en kan dit kleine, diepe gebied beschadigen. In plaats daarvan testten de onderzoekers of dezelfde MiniPromoters in het cerebrospinale vocht van rhesusmacaques konden worden toegediend via een enkele injectie in een laterale ventrikel. Met een AAV-capsidevariant die bekendstaat om ruim verspreiding vanuit de vloeistofruimten, vonden ze dat zowel Ple384 als Ple388 robuuste expressie aandreven in midbrain-dopaminerge neuronen van de substantia nigra en het ventrale tegmentale gebied, terwijl andere dopaminerge gebieden zoals de hypothalamus en de locus coeruleus grotendeels werden gespaard. De meeste gemarkeerde cellen in het doelgebied waren dopamine-neuronen, wat bevestigt dat de schakelaars hun selectiviteit over soorten heen behielden.
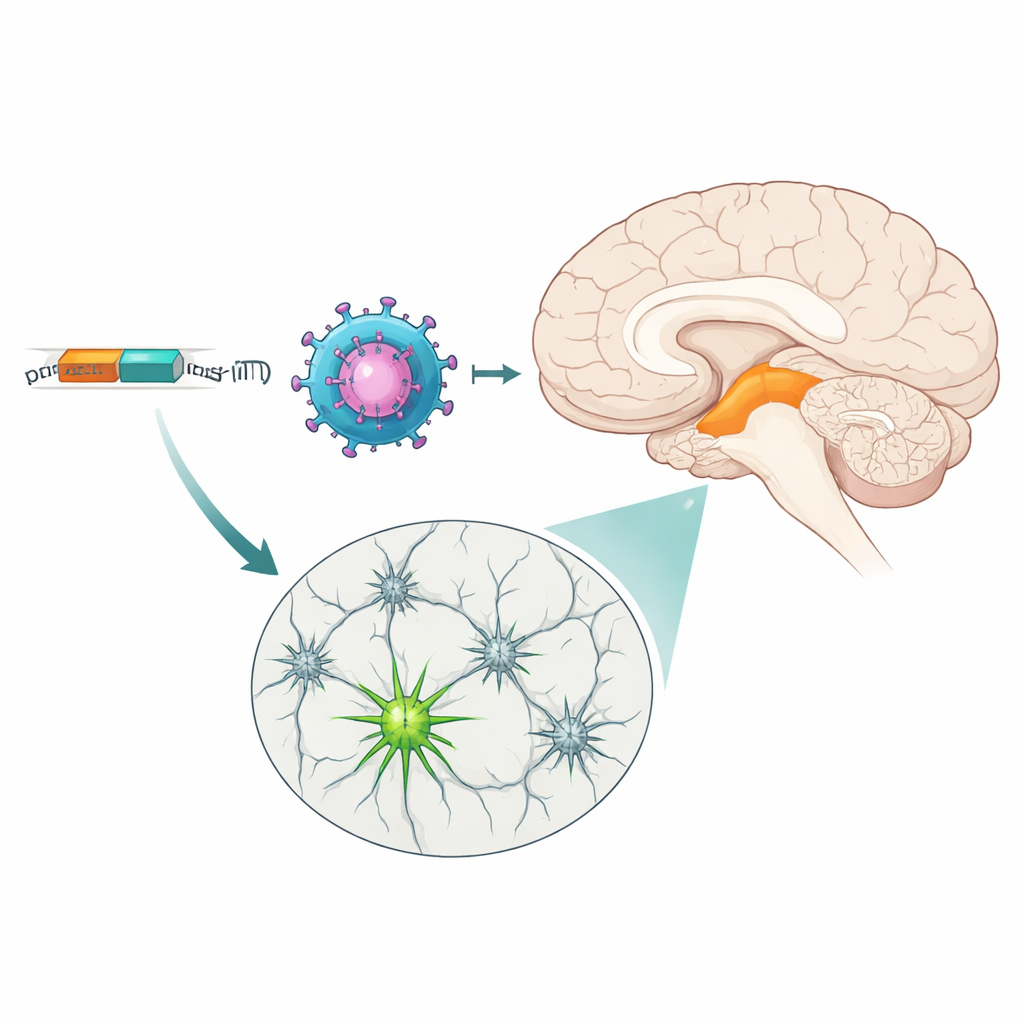
Twee hulpmiddelen met verschillende sterktes
Hoewel beide MiniPromoters hun doelen bereikten, deden ze dat met verschillende patronen. Ple384, gebaseerd op het ruimere tyrosinehydroxylase-gen, activeerde meer neuronen in het algemeen en omvatte zowel ventrale als dorsale lagen van de substantia nigra evenals een groter gedeelte van het ventrale tegmentale gebied. Ple388, reflecterend het meer beperkte PITX3-gen, markeerde voornamelijk een subset van ventrale-tier-neuronen en gaf zwakkere fluorescentie. Off‑target expressie werd vooral gezien nabij de injectieplaatsen en in sommige perifere organen na toediening via de bloedbaan, maar zorgvuldige controles toonden aan dat de virale vectoren veel hersengebieden konden bereiken; het waren de MiniPromoters zelf die de expressie grotendeels tot midbrain-dopaminerge neuronen beperkten. Deze instelbare sterkte—de ene krachtiger en breder, de andere selectiever en gematigder—betekent dat onderzoekers de schakelaar kunnen kiezen die het beste bij hun behoeften past, van zachte modulatie tot grootschalige interventie.
Wat dit betekent voor toekomstige therapieën
Voor niet‑specialisten is de kernboodschap dat de auteurs twee compacte genetische schakelaars hebben ontwikkeld die fungeren als precieze, programmeerbare lichtschakelaars voor dopamine-neuronen bij zowel muizen als apen. Ple384 biedt sterke, wijdverbreide toegang tot deze cellen, terwijl Ple388 zich richt op een nauwere, bijzonder kwetsbare subset. Omdat de schakelaars klein genoeg zijn om comfortabel in veelgebruikte virale vectoren te passen, laten ze ruimte over voor therapeutische genen en kunnen ze helpen bij het verminderen van bijwerkingen door ongewenste hersengebieden te vermijden. Naarmate gentherapie voor de ziekte van Parkinson en aanverwante aandoeningen vordert, zullen dergelijke gerichte controle-elementen essentiële ingrediënten zijn voor behandelingen die krachtig en toch precies zijn.
Bronvermelding: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Trefwoorden: dopamine-neuronen, gentherapie, ziekte van Parkinson, AAV-vectoren, celspecifieke promotoren