Clear Sky Science · nl
Therapeutische effecten van IGF-2 bij NMOSD door remming van astrocytenapoptose via modulatie van de IGF-1R/PI3K/AKT-signaleringsroute
De hersenen beschermen bij een weinig bekende auto-immuunziekte
Neuromyelitis optica spectrumstoornis, of NMOSD, is een zeldzame maar verwoestende auto-immuunziekte die de oogzenuwen en het ruggenmerg aantast en vaak blindheid, verlamming of ernstige cognitieve problemen bij patiënten achterlaat. De huidige geneesmiddelen onderdrukken vooral het immuunsysteem, zijn duur en beschermen hersencellen niet direct tegen schade. Deze studie onderzoekt of een natuurlijk in het bloed aanwezig groeigebonden molecuul, genaamd IGF‑2, hersencellen kan beschermen tegen letsel bij NMOSD en een nieuwe behandelingsmogelijkheid kan bieden.
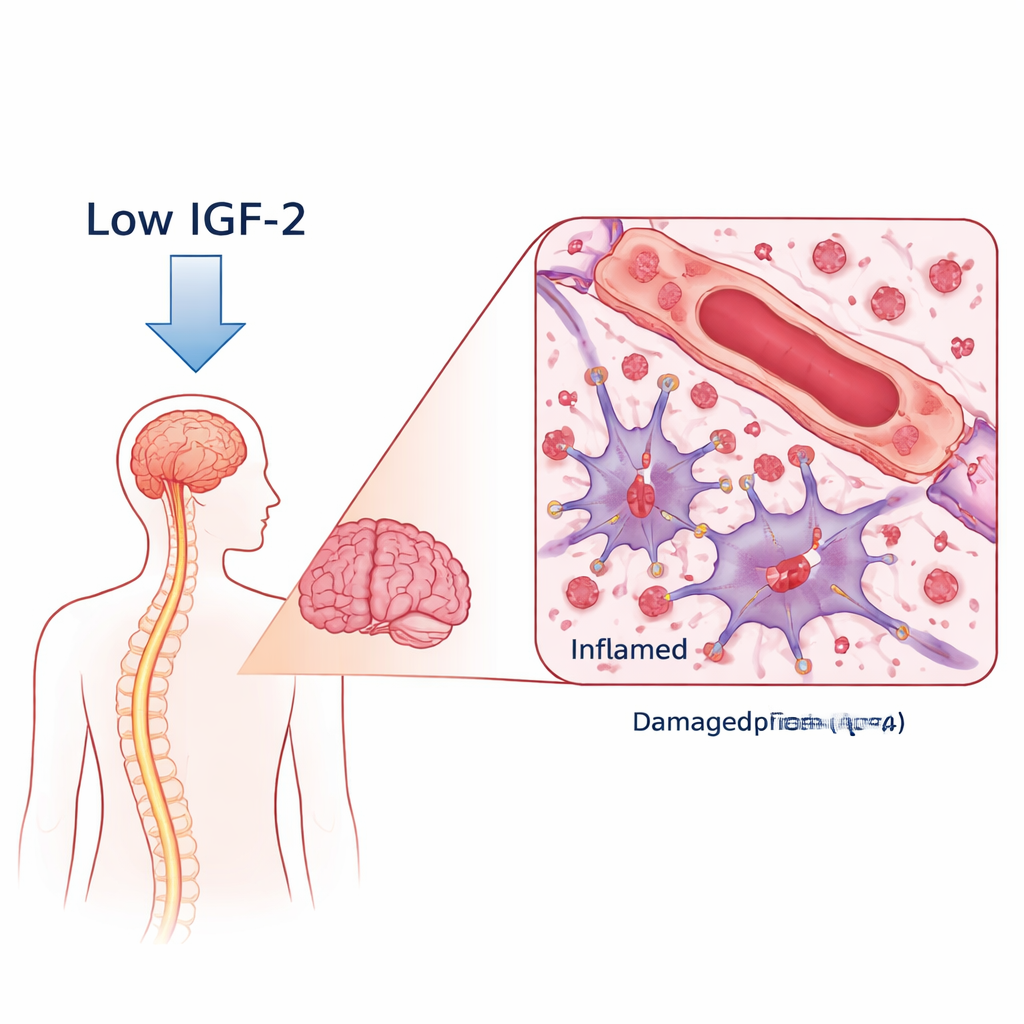
Een schadelijk antilichaam en een ontbrekende beschermer
Bij NMOSD maakt het lichaam antilichamen tegen een waterkanaaleiwit genaamd AQP4, dat voorkomt op stervormige steuncellen in de hersenen, astrocyten genoemd. Wanneer deze antilichamen binden, lokken ze immuunaanvallen uit die astrocyten beschadigen, myeline (de isolatielaag rond zenuwen) verwijderen en neuronen kunnen schaden. De onderzoekers vergeleken bloed van vrouwen met AQP4‑antilichaam‑positieve NMOSD met dat van gezonde vrijwilligers. Met een brede eiwitscreening vonden ze dat IGF‑2-niveaus sterk verlaagd waren bij NMOSD-patiënten, terwijl twee IGF-bindende eiwitten die IGF‑2 kunnen binden verhoogd waren. Belangrijk is dat patiënten met de laagste IGF‑2 doorgaans ernstiger beperkingen en slechtere scores op denk- en geheugentests hadden, wat dit molecuul koppelt aan ziekteernst en cognitieve gezondheid.
Standaardbehandeling helpt IGF-2 herstellen
Veel NMOSD-patiënten krijgen rituximab, een medicijn dat antistofproducerende B-cellen verwijdert. Het team mat bloedproteïnen voor en na rituximabbehandeling. Na therapie stegen de IGF‑2-niveaus en daalden de bindende eiwitten, waardoor het patroon dichter bij dat van gezonde personen kwam te liggen. Dit suggereert dat het temmen van het immuunsysteem het lichaam kan toestaan enkele van zijn eigen beschermende factoren te herstellen. Hoewel rituximab niet speciaal is ontworpen om op IGF‑2 in te werken, duidt de verschuiving in dit molecuul erop dat het mogelijk deel uitmaakt van het herstelmechanisme van het lichaam, en dat het monitoren van IGF‑2 kan helpen bij het volgen van de toestand van patiënten in de tijd.
IGF-2 testen in een muismodel van de ziekte
Om te onderzoeken of IGF‑2 meer kan doen dan alleen ziekteernst signaleren, richtten de onderzoekers zich op een muismodel. Ze injecteerden menselijke AQP4-antilichamen en menselijke complement in de hersenen van muizen, wat belangrijke kenmerken van NMOSD reproduceerde: verlies van AQP4 op astrocyten, ontsteking, myelineschade en ledemaatzwakte. Een andere groep muizen kreeg eerst een onschadelijk virus dat hun hersencellen extra IGF‑2 liet produceren. Deze muizen met verhoogd IGF‑2 verloren minder gewicht, hadden mildere bewegingsproblemen en toonden minder mylineverlies en ontsteking in hersen- en ruggenmergweefsel. De standaardbehandeling met rituximab hielp ook, maar overexpressie van IGF‑2 leek hersenweefsel meer direct te beschermen, wat wijst op een neuroprotectieve rol in plaats van alleen een immuunsuppressieve werking.
Hoe IGF-2 celdood en ontsteking kalmeert
Het team onderzocht vervolgens astrocyten in kweek die werden blootgesteld aan NMOSD-antilichamen. Normaal gesproken verlaagden deze antilichamen de niveaus van een belangrijke receptor genaamd IGF‑1R en dempten ze een downstream beschermende route die bekendstaat als PI3K/AKT, terwijl “zelfvernietigings”-eiwitten en ontstekingssignalen werden geactiveerd. Wanneer de onderzoekers astrocyten dwongen meer IGF‑2 te maken, werd deze beschermende route weer geactiveerd, daalden markers van celdood en gaven de cellen minder ontstekingsmoleculen vrij zoals IL‑1β, IL‑6 en TNF‑α. Het blokkeren van de IGF‑1R-receptor wist deze voordelen gedeeltelijk uit, wat toont dat IGF‑2 voornamelijk werkt door activering van de IGF‑1R/PI3K/AKT-keten in astrocyten. In levende muizen verminderde verhoging van IGF‑2 ook de activatie van microgliacellen, de immuurbewakers van de hersenen, en verlaagde het ontstekingssignalen in de bloedbaan.
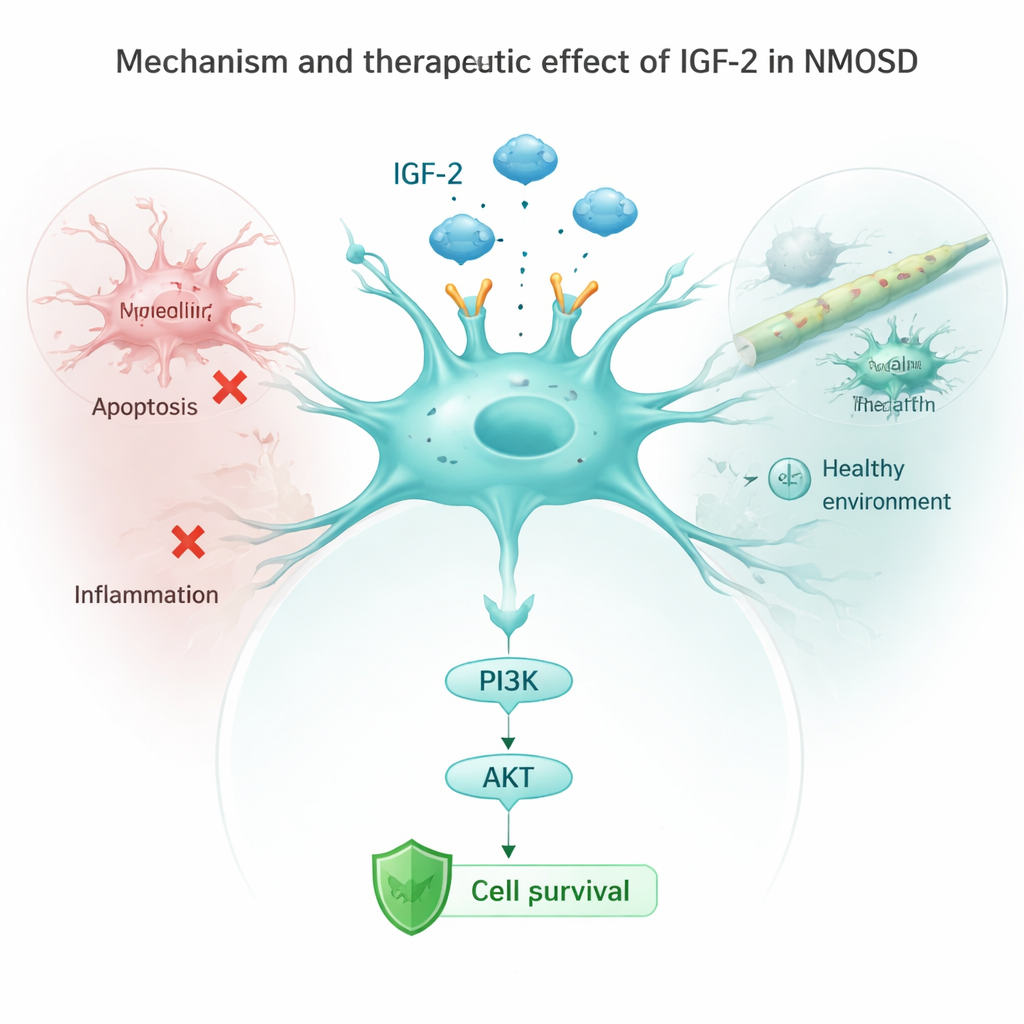
Wat dit voor patiënten zou kunnen betekenen
Gezamenlijk suggereren deze bevindingen dat laag IGF‑2 zowel een waarschuwingssignaal als een gemiste kans is bij NMOSD. Patiënten met minder IGF‑2 hebben vaak meer beperkingen en denken minder helder, terwijl het herstellen of verhogen van IGF‑2 in experimentele modellen helpt astrocyten te laten overleven, hersenontsteking vermindert en zenuwschade afneemt. Hoewel dit werk vroeg is en gebaseerd op kleine patiëntengroepen en dierstudies, wijst het op IGF‑2 als een veelbelovend doelwit voor toekomstige behandelingen die niet alleen de immuunaanwval verminderen maar ook kwetsbare hersencellen direct beschermen.
Bronvermelding: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Trefwoorden: neuromyelitis optica, astrocyten, IGF-2, neuroinflammatie, neuroprotectie