Clear Sky Science · nl
Metabolomische beoordeling onthult uitputting van aminozuren en energiemetabolieten in skeletspier na ischemische acute nierschade bij muizen
Waarom gewonde nieren uw kracht kunnen uitputten
Mensen met plotselinge nieruitval merken vaak iets dat in eerste instantie niets met urine- of bloedtesten lijkt te maken te hebben: hun spieren voelen zwak aan en herstel verloopt traag. Deze studie stelt een eenvoudige maar belangrijke vraag — wat gebeurt er precies in de brandstof- en bouwstofvoorraden van onze spieren wanneer de nieren plotseling beschadigd raken? Met een gedetailleerd chemisch onderzoek van muizen spieren laten de onderzoekers zien dat acute nierschade een lichaamsbrede aantasting veroorzaakt van belangrijke voedingsstoffen en energiemoleculen, waardoor de skeletspier in een uitgeputte, energieloze staat achterblijft.
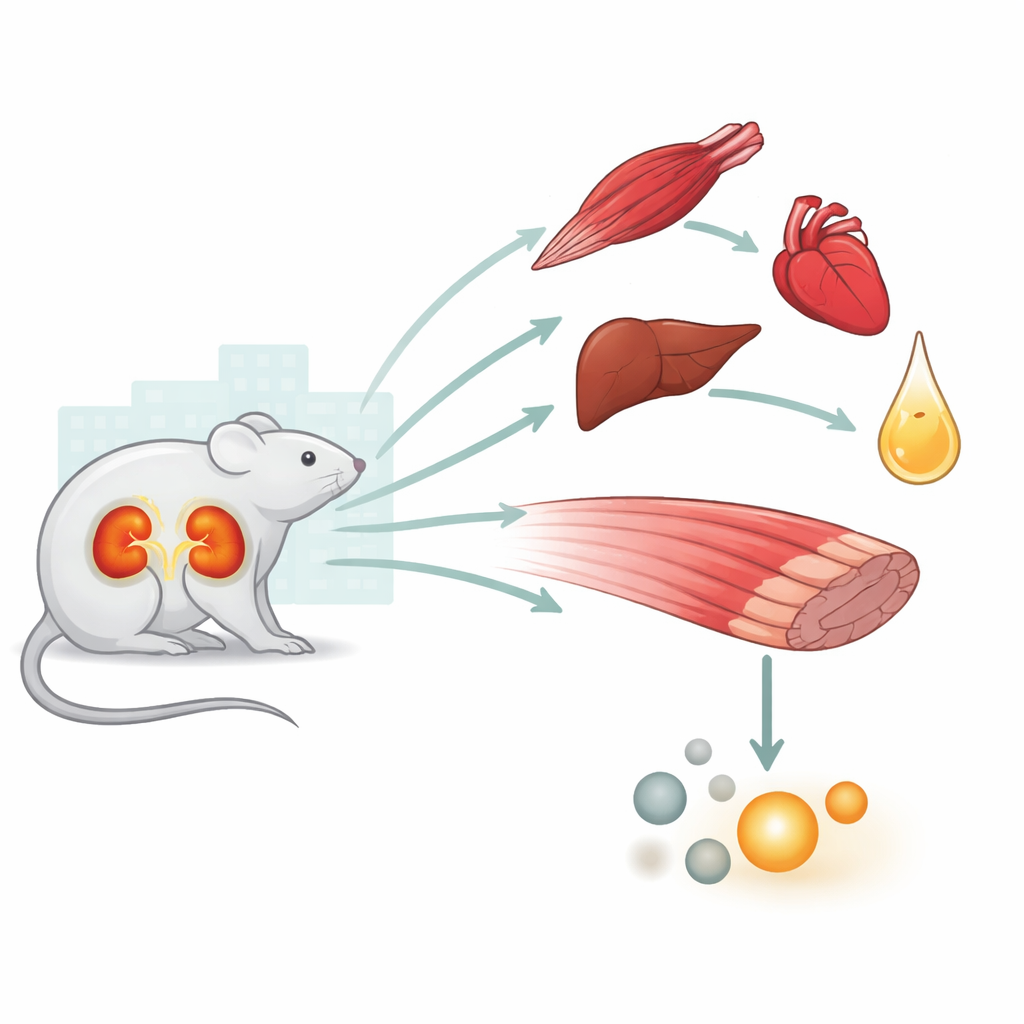
Een crisis voor het hele lichaam, niet alleen een nierprobleem
Acute nierschade (AKI) komt vaak voor bij opgenomen en kritiek zieke patiënten en hangt sterk samen met een grotere kans op overlijden. Artsen merken al langer dat AKI zich gedraagt als een toestand van stress voor het hele lichaam, met gevolgen voor hart, longen, lever, hersenen en spieren. Eerder werk van deze groep toonde aan dat na tijdelijke onderbreking van de bloedtoevoer naar de nieren bij muizen het hart, de lever, de longen en de nieren zelf chemische tekenen van lage energie en oxidatieve stress vertoonden. Voortbouwend daarop richt de huidige studie zich op de skeletspier, een belangrijke opslagplaats van koolhydraten en aminozuren waarop het lichaam kan terugvallen tijdens ernstige stress.
Hoe de studie bij muizen werd uitgevoerd
Onderzoekers veroorzaakten ischemische AKI bij jonge volwassen mannelijke muizen door kort de bloedtoevoer naar beide nieren af te knijpen en daarna de bloedstroom te herstellen. Zij vergeleken deze dieren met schijnoperatie-muizen en volledig onbewerkte controles. Na 24 en 72 uur namen ze een belangrijke beenspier (de gastrocnemius) en gebruikten een niet-gerichte metabolomica-benadering — een ultrasensitieve chemische scan — om 175 kleine moleculen te meten, waaronder aminozuren, antioxidanten en energierelateerde verbindingen. Statistische en patroonherkenningsmethoden werden gebruikt om te bepalen welke moleculen het meest veranderden en hoe de spierchemie tussen de groepen verschilde.
Brandstof en antioxidanten in de spier raken op
De meest opvallende veranderingen ontstonden 24 uur na nierschade. Ongeveer twee vijfde van alle gedetecteerde metabolieten was veranderd, en het algemene patroon was duidelijk: veel belangrijke verbindingen in de spier waren uitgeput in vergelijking met schijnoperatie. Essentiële en niet-essentiële aminozuren zoals alanine, valine, lysine, methionine en tyrosine daalden, evenals meerdere moleculen in de ureumcyclus (arginine, citrulline, ornithine, argininosuccinaat) die helpen bij de verwerking van stikstofafval en de ondersteuning van creatineproductie. Het belangrijkste cellulaire antioxidant, glutathion, en diens bouwstenen (waaronder methionine en een cysteïne-glycine dipeptide) waren ook verminderd, wat wijst op verhoogde oxidatieve stress. Energierelateerde moleculen, waaronder creatine en tussenproducten van centrale energiepaden, vertoonden eveneens een dalende trend, wat suggereert dat de spier zijn eigen reserves opgeeft om de rest van het lichaam te ondersteunen.
De verbinding tussen spier en andere organen
Om het grotere geheel te zien vergeleek het team spiergegevens met eerder verzamelde metabolomische profielen van nier, lever, hart en bloedplasma op hetzelfde 24-uurs tijdstip. Over al deze locaties herkenden ze terugkerende thema’s: wijdverspreide uitputting van glutathion en zijn voorlopers, lagere alaninewaarden en consistente verstoring van arginine- en ureumcyclus-gerelateerde chemie. Tegelijkertijd stegen sommige afbraakproducten, zoals allantoin (een marker voor oxidatieve stress), in meerdere organen en in de bloedbaan. Creatine en zijn hoogenergetische vorm, fosfocreatine, waren relatief verhoogd in lever, nier en bloed, zelfs terwijl arginine en aminozuren in spier en plasma afnamen, wat suggereert dat skeletspier mogelijk substraten exporteert zodat andere organen — en vooral de beschadigde nieren — onder stress energie kunnen blijven produceren.
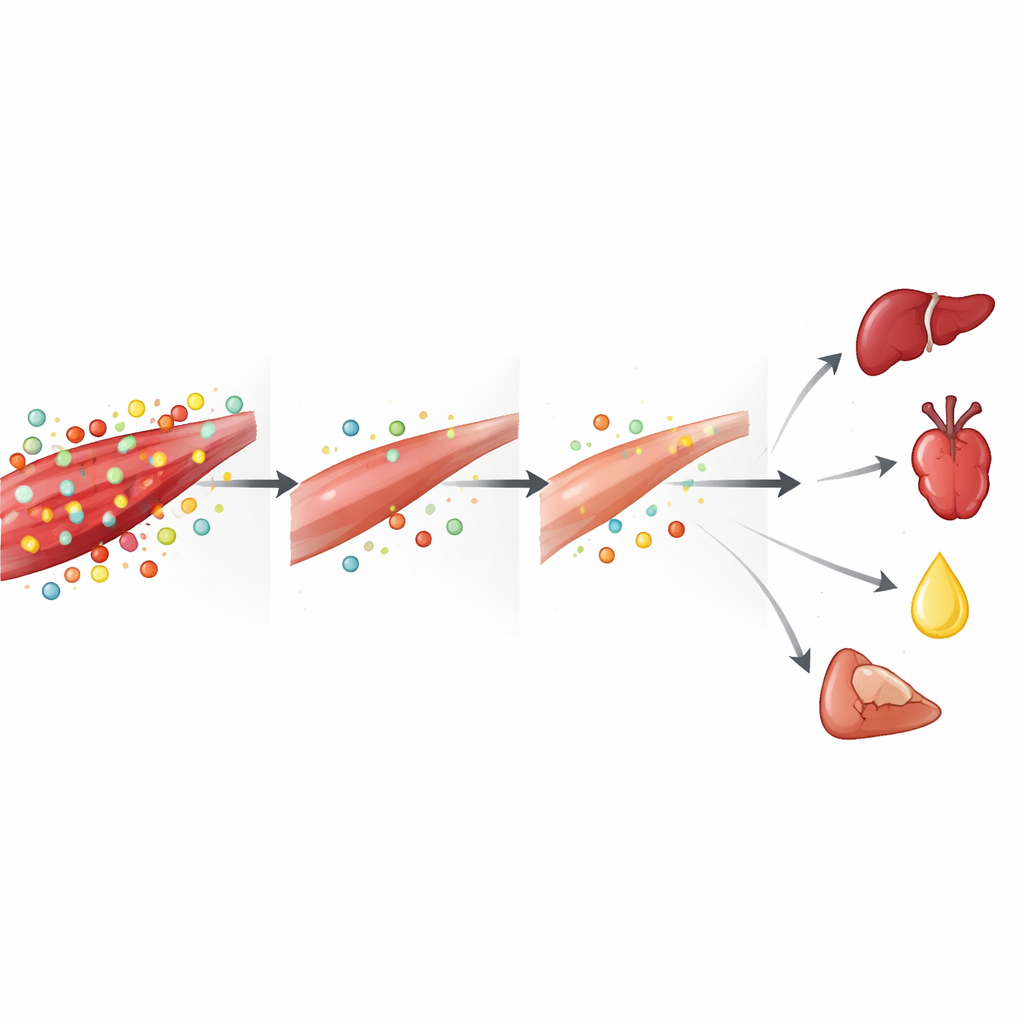
Wat dit betekent voor patiënten en toekomstige therapieën
In gewone bewoordingen portretteert de studie AKI als een metabole "cash‑out" gebeurtenis voor het lichaam: skeletspier breekt eiwit- en antioxidantvoorraden af om vitale organen van energie en bescherming te voorzien, waardoor de spieren zelf tekort komen aan brandstof en verdediging. Dit helpt verklaren waarom mensen met ernstige nierschade vatbaar zijn voor spierverlies, zwakte en een slecht functioneel herstel. Het werpt ook de mogelijkheid op dat zorgvuldig gerichte voedingsondersteuning — in het bijzonder aminozuren en verbindingen die glutathion- en creatine-fosfocreatinesystemen versterken — ooit zou kunnen helpen om zowel nieren als spieren te beschermen tijdens acute ziekte. Hoewel deze bevindingen afkomstig zijn van muizen en gebaseerd zijn op chemische momentopnamen in plaats van directe tracerstudies van stromen, bieden ze een gedetailleerde kaart van hoe spierchemie verstoord raakt door nierschade en wijzen ze op nieuwe strategieën om kracht te behouden en uitkomsten te verbeteren wanneer de nieren plotseling falen.
Bronvermelding: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Trefwoorden: acute nierschade, metabolisme van skeletspier, uitputting van aminozuren, oxidatieve stress, metabolomics