Clear Sky Science · nl
Analyse van systolische hartfunctie in PERM1-knockout muizen met behulp van grote cohorten dieren
Waarom kleine muizenharten van belang zijn voor de menselijke gezondheid
Hartfalen wordt vaak omschreven als een uitgeputte pomp, maar wat een hart zwak maakt is verrassend complex. In deze studie gebruikten wetenschappers een ongewoon grote groep muizen om één gerichte vraag te stellen: verandert het uitzetten van een enkel gen, PERM1, dat bekendstaat als helper bij de energieproductie in hartcellen, de kracht waarmee het hart samentrekt? Door de harten van meer dan 170 muizen zorgvuldig te scannen laten ze zien dat dit gen het hart subtiel hervormt en de pompkracht verlaagt, terwijl de dieren in grote lijnen van buitenaf gezond blijven. Hun bevindingen helpen een debat in het veld te beslechten en bieden een routekaart voor het ontwerpen van betere hartexperimenten in de toekomst.
Een gen dat brandstofgebruik koppelt aan hartcontractie
PERM1 werd eerst geïdentificeerd als een schakelaar die de energieproductie in spiercellen, inclusief het hart, verhoogt. Eerder werk toonde aan dat PERM1-niveaus dalen in falende harten bij zowel muizen als mensen, wat de mogelijkheid opwerpt dat lage PERM1 daadwerkelijk bijdraagt aan zwakkere hartslagen. Maar studies met PERM1-knockoutmuizen — dieren die zodanig zijn geconstrueerd dat ze het gen missen — gaven tegenstrijdige antwoorden over de vraag of hun harten echt minder effectief pompen. Omdat PERM1 wordt beschouwd als een potentiële doelwit voor nieuwe hartfalenbehandelingen, wilden de auteurs het effect op hartfunctie testen met voldoende dieren en strikte statistiek om een duidelijk ja-of-nee-antwoord te geven.
Een groot-aantal blik op kleine harten
Het team verzamelde echocardiogramgegevens — dezelfde ultrasone techniek die in hartklinieken wordt gebruikt — van elke PERM1-knockoutmuis en zijn gezonde nestgenoot die in hun laboratorium werd gebruikt gedurende een periode van 18 maanden. Deze retrospectieve verzameling leverde 84 normale (wild-type) en 88 knockoutdieren op, een steekproefgrootte veel groter dan gebruikelijk in muizenhartstudies. Vanuit de echobeelden maten ze standaardindicatoren van hoe goed de linkerhartkamer, de belangrijkste pompkamer, werkt. De sleutelmeting was de ejectiefractie, het percentage bloed dat bij elke slag wordt weggepompt, samen met gerelateerde maten zoals hoeveel de diameter van de kamer krimpt bij contractie, hoe dik de wanden zijn en de totale hoeveelheid bloed die per minuut wordt weggepompt.
Zwakkere samentrekking, grotere kamer, vergelijkbare output
De resultaten tonen een consistent patroon. Gemiddeld daalde de ejectiefractie van ongeveer 65% bij normale muizen naar 54% bij PERM1-knockouts, een verschil dat klinisch relevant zou zijn bij menselijke patiënten en ondersteund wordt door zeer sterke statistiek. Andere maatstaven van contractie, zoals fractionele verkorting en wandverdikking, namen ook af. Tegelijkertijd waren de linkerkamers van de knockouts merkbaar groter, vooral aan het einde van de contractie, wat aangeeft dat er meer bloed in de kamer achterbleef. Ondanks deze zwakkere samentrekking daalde de totale hoeveelheid bloed die per minuut werd weggepompt slechts licht — met ongeveer 6% — omdat de vergrote kamers aanvankelijk meer bloed konden bevatten. Met andere woorden, het hart compenseerde deels voor de verminderde contractiekracht door zijn hoofdkamer uit te rekken.
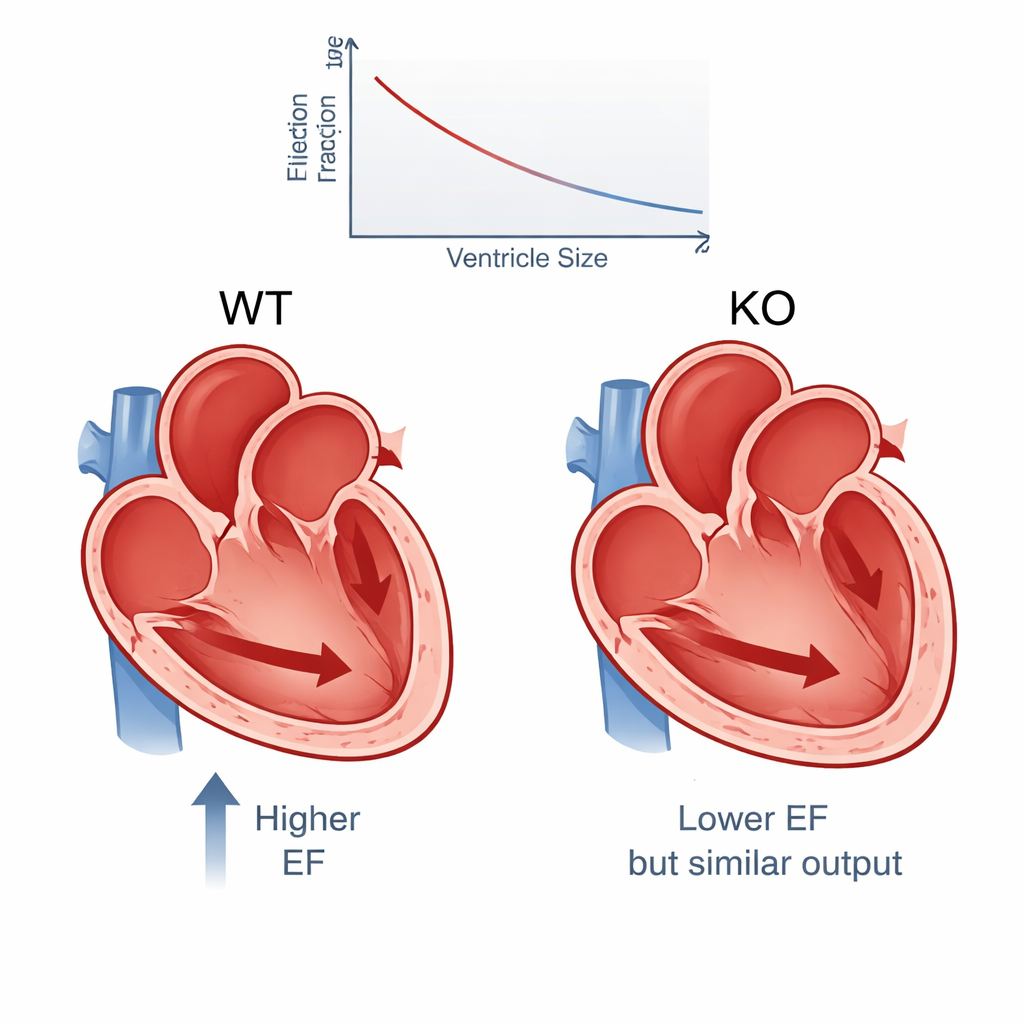
Verborgen diversiteit in “identieke” harten
Omdat de studie zoveel dieren omvatte, konden de onderzoekers verder kijken dan gemiddelden en bestuderen hoe individuele harten varieerden. Zelfs onder genetisch identieke, gezonde muizen zagen ze een verrassend brede spreiding in ejectiefractie. Het uitzetten van PERM1 verschuift de gehele verdeling naar beneden — meer harten met lagere pompsterkte — maar maakte de spreiding zelf niet groter. Ongeveer 7% van de knockoutmuizen had een ejectiefractie onder 40%, een niveau dat bij mensen zou kwalificeren als hartfalen met verminderde ejectiefractie, en toch handhaafden deze muizen nog grotendeels een bijna normale bloedoutput. Statistische analyses lieten zien dat geslacht, leeftijd en lichaamsgewicht slechts een klein deel van de variabiliteit verklaren; de meeste verschillen komen waarschijnlijk voort uit moeilijker meetbare biologische factoren zoals subtiele omgevingsinvloeden of epigenetische veranderingen.
Wat dit betekent voor toekomstig hartonderzoek
Om andere wetenschappers te helpen betere experimenten te ontwerpen, gebruikten de auteurs hun grote dataset om te berekenen hoeveel dieren doorgaans nodig zijn om betekenisvolle veranderingen in elke hartparameter te detecteren. Ze vonden dat de bescheiden groepsgroottes die vaak in het veld worden gebruikt gemakkelijk echte maar matige effecten kunnen missen, vooral voor subtiele maten zoals slagvolume of hartminuutvolume. Over het geheel genomen levert de studie sterke aanwijzingen dat het verlies van PERM1 een specifieke remodelering van het hart veroorzaakt — grotere kamers, zwakkere contractie — in plaats van een volledige uitval, en dat deze remodelering deels wordt gecompenseerd door structurele veranderingen die helpen de bloedstroom te behouden. Voor niet‑specialisten is de conclusie dat een enkel gen dat de energiehuishouding regelt het hart in een nieuwe bedrijfstoestand kan duwen, één die van buiten gezond lijkt maar subtiele verschuivingen in de opbouw en inspanning van de pomp met zich meebrengt.
Bronvermelding: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Trefwoorden: hartfalen, cardiale contractiliteit, mitochondriale energetica, muismodellen, echocardiografie