Clear Sky Science · nl
GJB2 c.109G > A-mutatue die IFI27-gemedieerde mitochondriale apoptoseweg activeert en leidt tot erfelijke niet-syndromale gehoorverlies
Waarom kleine oorcellen belangrijk zijn voor de toekomst van kinderen
Aangeboren gehoorverlies treft wereldwijd miljoenen kinderen en beïnvloedt vaak hoe ze leren praten, slagen op school en contact maken met anderen. Een van de meest voorkomende genetische oorzaken is het gen GJB2, maar artsen hebben niet helemaal kunnen doorgronden hoe wijzigingen in dit gen het binnenoor daadwerkelijk beschadigen. In deze studie gebruiken de onderzoekers zebravissen en menselijke cellen om de keten van gebeurtenissen te volgen van een enkele DNA-verandering in GJB2 tot de dood van kwetsbare geluidssensorische cellen, en wijzen ze op een nieuw molecuul, IFI27, als een mogelijke doelwit voor toekomstige behandelingen.
Een veelvoorkomende genverandering achter stil jeugd
De onderzoekers begonnen met het screenen van bloedmonsters van 1.199 kinderen met vermoedelijk erfelijk gehoorverlies in de provincie Fujian, China. Ze richtten zich op enkele bekende doofheidsgenen en vonden dat veranderingen in GJB2 de overhand hadden en goed waren voor 85% van alle gedetecteerde mutaties. Onder deze vondsten was een specifieke verandering, c.109G>A (ook bekend als p.Val37Ile), het meest voorkomend. Deze variant komt relatief vaak voor in de algemene bevolking maar is sterk verrijkt bij mensen met gehoorverlies, wat erop wijst dat ze een belangrijke rol speelt bij niet-syndromaal gehoorverlies—gehoorproblemen die optreden zonder andere medische verschijnselen.
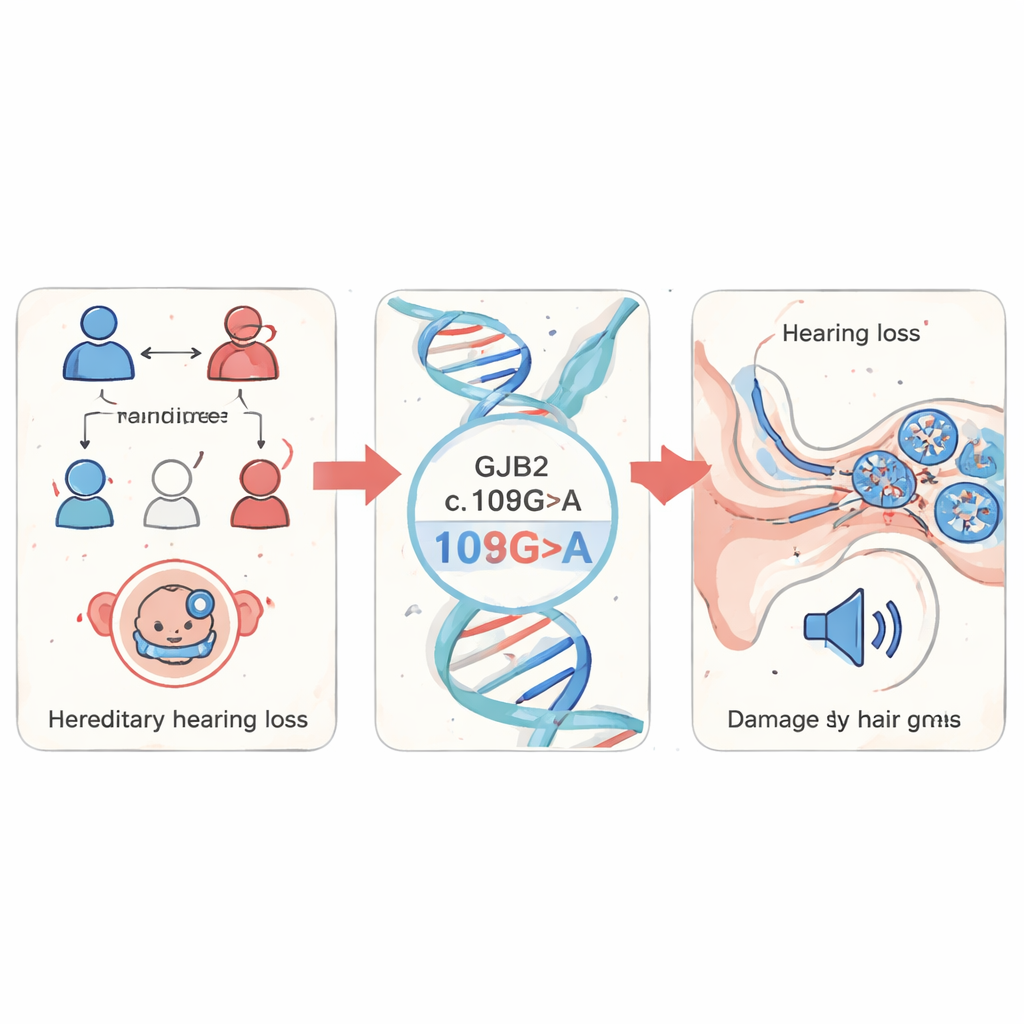
De schade volgen in een transparante vis
Om te zien wat deze mutatie in een levend organisme doet, gebruikte het team zebravissen, een kleine zoetwatervis waarvan de embryo’s doorzichtig zijn en die veel genen en oorstructuren met mensen deelt. Ze hielpen zebravis-embryo’s om ofwel normaal menselijk GJB2 ofwel de c.109G>A-mutantversie te produceren, en gebruikten daarnaast een “knockdown”-benadering om het eigen gjb2-gen van de vis te verminderen. Embryo’s met de mutant of het gereduceerde gen vertoonden vertraagde groei, gekromde staarten en zwelling rond het hart, tekens dat de ontwikkeling verstoord was. Het belangrijkste was dat hun binnenoortjes duidelijk afwijkend waren: sleutelstructuren genaamd otolieten waren kleiner en verder uit elkaar geplaatst, en het met vloeistof gevulde cochleaire gebied was verkleind. Toen de wetenschappers naast de mutant ook normale GJB2 toevoegden, verbeterden veel van deze structurele problemen, wat aangeeft dat de mutatie zelf de defecten veroorzaakte.
Van defecte oren naar slechter gehoor bij gedragstests
Aangezien gehoor afhankelijk is van kleine “haarcellen” die geluidstrillingen omzetten in zenuwsignalen, kleurde het team deze cellen in de zebravissen. Vissen met de GJB2-mutatie of knockdown hadden veel minder haarcellen zowel in het binnenoor als langs het lichaamsoppervlak, waar zebravissen ook waterbewegingen waarnemen. De onderzoekers testten vervolgens hoe goed de vissen op geluid reageerden. Met een geautomatiseerd volgsysteem maten ze hoe ver en hoe snel vijf dagen oude larven zwommen als ze werden blootgesteld aan korte geluidspulsen. Normale en wildtype GJB2-vissen reageerden door meer en sneller te zwemmen, terwijl mutant- en knockdown-vissen hun gedrag nauwelijks veranderden, wat duidt op verminderd gehoor. Ook hier herstelde het toevoegen van normale GJB2 deels zowel het aantal haarcellen als het geluidgestuurde bewegen.
Een dodelijke route in de stroomhuizen van de cel
Om te begrijpen wat er binnen in de cellen gebeurde, gebruikten de wetenschappers RNA-sequencing om de genactiviteit te vergelijken tussen normale zebravissen en vissen met verminderd gjb2. Een reeks genen die gekoppeld is aan de “mitochondriële apoptoseweg”—een zelfvernietigingsroute gecentreerd in de energiecentrales van de cel—was sterk geactiveerd. Met name meerdere leden van de IFI27-familie vielen op, samen met bekende celsterfte-spelers zoals Bax, cytochroom c, Apaf1 en caspases. Vervolgexperimenten in menselijke HEK293-cellen bevestigden het patroon: cellen met het mutant GJB2 produceerden meer reactieve zuurstofsoorten (ROS, een vorm van oxidatieve stress), zetten meer cytochroom c vrij uit mitochondriën en schakelden apoptose-eiwitten aan, wat leidde tot verhoogde celdood. Toen de onderzoekers IFI27 in cellen met het mutante gen uitschakelden, daalden de ROS-niveaus, werden de doodssignalen afgezwakt en ondergingen minder cellen apoptose.
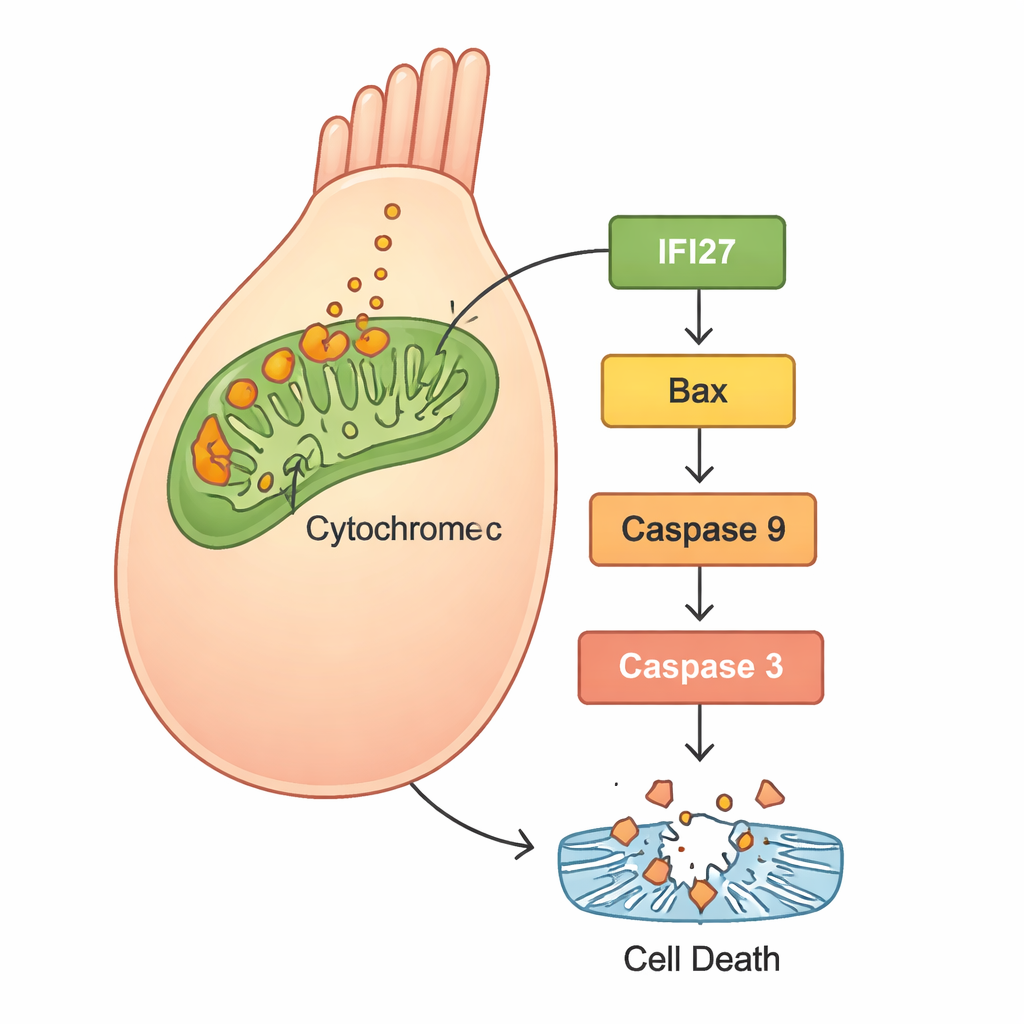
Wat dit betekent voor toekomstige behandelingen
Al met al suggereren de bevindingen een duidelijk verhaal: de GJB2 c.109G>A-mutatie verstoort de normale ontwikkeling en functie van het binnenoor, niet alleen door celcommunicatie te veranderen, maar ook door stress in de mitochondriën te veroorzaken. Deze stress verhoogt IFI27 en verwante genen, leidt tot vrijgave van cytochroom c en activeert een cascade van eiwitten die haarcellen richting geprogrammeerde celdood duwen. Omdat haarcellen bij mensen niet gemakkelijk teruggroeien, leidt hun verlies tot blijvende gehoorachterstanden. Door aan te tonen dat het terugschakelen van IFI27 deze destructieve cascade in menselijke cellen kan verzachten, benadrukt de studie IFI27 als een veelbelovend doelwit voor geneesmiddelen of gengebaseerde therapieën. Hoewel zulke behandelingen nog ver weg zijn—en waarschijnlijk zeer vroeg in het leven toegediend moeten worden—biedt dit werk een concreet moleculair stappenplan om een ooit mysterieuze genmutatie te veranderen in een mogelijk te voorkomen oorzaak van kinderdoofheid.
Bronvermelding: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
Trefwoorden: genetisch gehoorverlies, GJB2-mutatie, zebravis-model, mitochondriale apoptose, IFI27