Clear Sky Science · nl
Efficiënte apoptose via DNA-dubbeldraadsbreuken in humane epitheelcellen geïnduceerd door niet-thermisch effect van hoog-veld breedband terahertzgolven
Nieuw licht op het doden van kankercellen
Kankerbehandelingen balanceren vaak: ze moeten tumorcellen vernietigen zonder gezond weefsel of het immuunsysteem ernstig te schaden. Deze studie onderzoekt een ongebruikelijk instrument voor die taak — intense terahertz (THz)-golven, een type onzichtbaar licht tussen microgolven en infrarood. De onderzoekers tonen aan dat zorgvuldig afgestemde, hoog-veld THz-pulsen kankercellen gecontroleerd tot zelfdoding kunnen aanzetten, zonder het weefsel te verhitten of de rommelige celdood te veroorzaken die tot ontsteking leidt.
Waarom zachte celdood ertoe doet
Veel gebruikelijke kankertherapieën dwingen cellen tot dood, maar vaak met bijwerkingen. Medicijnen en biologische middelen kunnen hun effectiviteit verliezen naarmate tumoren resistentie ontwikkelen, en ze kunnen het immuunsysteem verzwakken. Fysische methoden zoals röntgenstraling, radioactiviteit of warmte-gebaseerde ablatie kunnen omliggend gezond weefsel beschadigen en veroorzaken vaak necrose — een gewelddadige vorm van celdood die ontsteking en pijn opwekt. Een methode die in plaats daarvan apoptose aanstuurt, een nette zelfvernietigingsprocedure waarbij cellen zichzelf stilletjes ontwarren, zou een veel minder traumatische manier kunnen bieden om tumoren te verkleinen, vooral oppervlakkige tumoren dicht bij de huid.
Terahertzgolven en borstkankercellen
Het team richtte zich op menselijke borstkankercellen (MCF‑7), een type epitheelcel dat vaak in laboratoriumonderzoek wordt gebruikt. Ze bestraalden deze cellen met zeer sterke, breedband gepulseerde THz-golven tot vier uur, terwijl de temperatuur van de cellen op normale lichaamstemperatuur werd gehouden. De veldsterktes bereikten enkele miljoenen volt per centimeter, veel hoger dan in alledaagse apparaten. Onder deze omstandigheden nam het aandeel cellen dat apoptose onderging gestaag toe met de belichtingstijd. Bij de hoogste geteste THz-intensiteit trad bij bijna 99% van de kankercellen apoptose op, terwijl minder dan 1% door necrose stierf. Deze massale, zuivere golf van geprogrammeerde celdood suggereert dat de THz-pulsen meer doen dan alleen de cellen verwarmen.
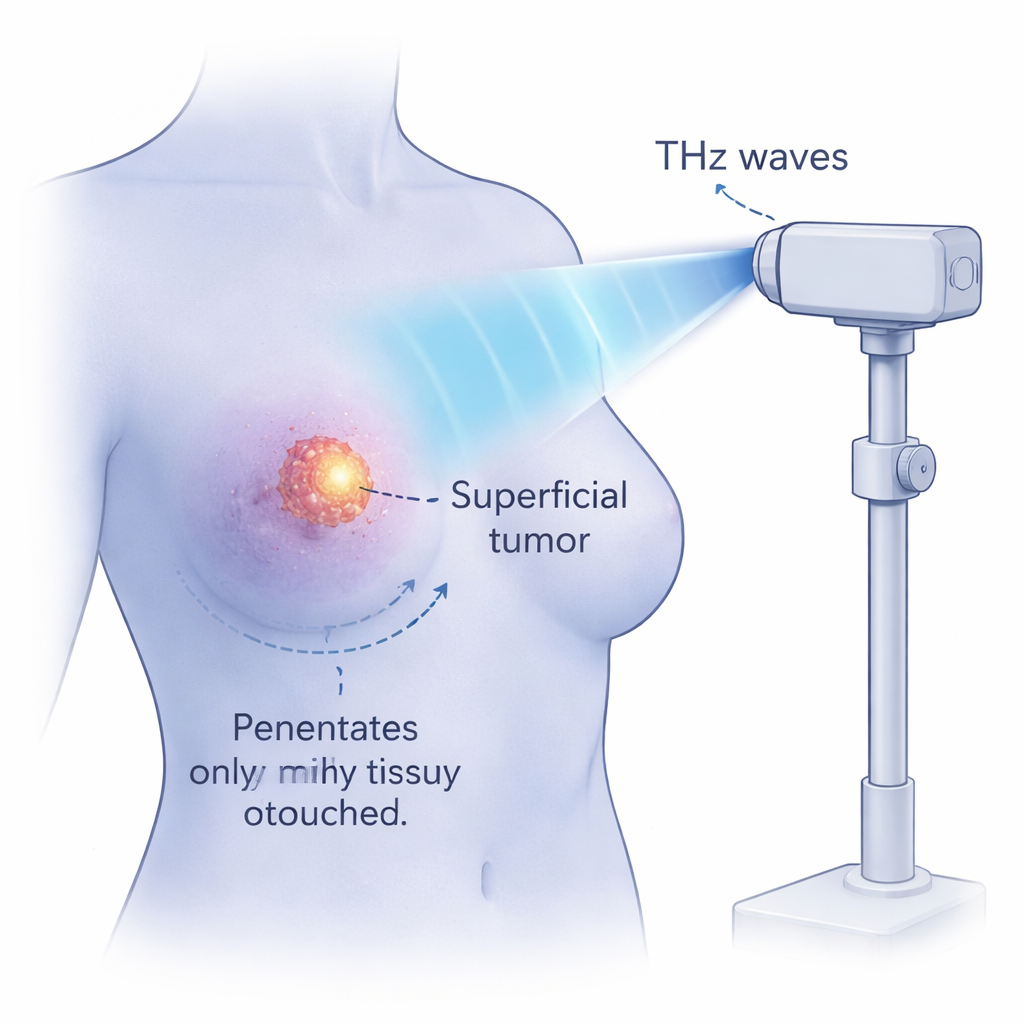
Niet-verwarmende effecten en veilige temperatuurgrenzen
Omdat water sterk THz-straling absorbeert, is de voor de hand liggende zorg onbedoelde verwarming. De wetenschappers gebruikten thermografie om temperatuurveranderingen tijdens bestraling te volgen. Zelfs na vier uur bij matige intensiteit stegen de temperaturen van de kankercellen slechts ongeveer 3 °C, en bleef necrose onder 4%. Aparte controles waarin cellen eenvoudigweg vier uur werden verwarmd lieten zien dat temperaturen onder 41 °C vrijwel geen celdood veroorzaakten, terwijl boven 43 °C een scherpe toename van necrose optrad. Zelfs bij hun meest intense THz-instellingen hielden de onderzoekers celtemperaturen op of onder die 43 °C-drempel en zagen toch bijna volledige apoptose met minimale necrose. Door de herhalingsfrequentie van de pulsen te verlagen, toonden ze aan dat de temperatuur beheersbaar blijft terwijl sterke antitumoreffecten behouden blijven, wat benadrukt dat een niet-thermisch mechanisme aan het werk is.
DNA uit elkaar laten trillen en doodsgenen inschakelen
Om dat mechanisme te vinden keek de groep binnen in de cellen. Onder elektronenmicroscopie toonden THz-behandelde cellen klassieke vroege tekenen van apoptose: gecondenseerd genetisch materiaal, veranderde kernen en intacte buitenmembranen. Met een fluorescent marker genaamd γ‑H2AX detecteerden ze uitgebreide dubbeldraadsbreuken in het DNA — schade die veel frequenter was in bestraalde cellen dan in onbehandelde of licht verwarmde controles. Het schadepatroon volgde het intensiteitsprofiel van de THz-bundel, en werd sterker naar het centrum toe. Gen- en proteïneanalyses toonden aan dat een set stress- en schade-responsieve moleculen, zoals GADD45B en c‑Jun, sterk geactiveerd waren, terwijl bekende spelers in traditionele celdoodroutes, waaronder p53 en veel caspases, niet veel veranderden. De auteurs stellen voor dat intense THz-velden gewelddadige vibrationale “resonanties” in DNA kunnen opwekken, waardoor de dubbele helix fysiek wordt belast en breekt en vervolgens een duidelijke, p53- en caspase-onafhankelijke apoptoseweg activeert.
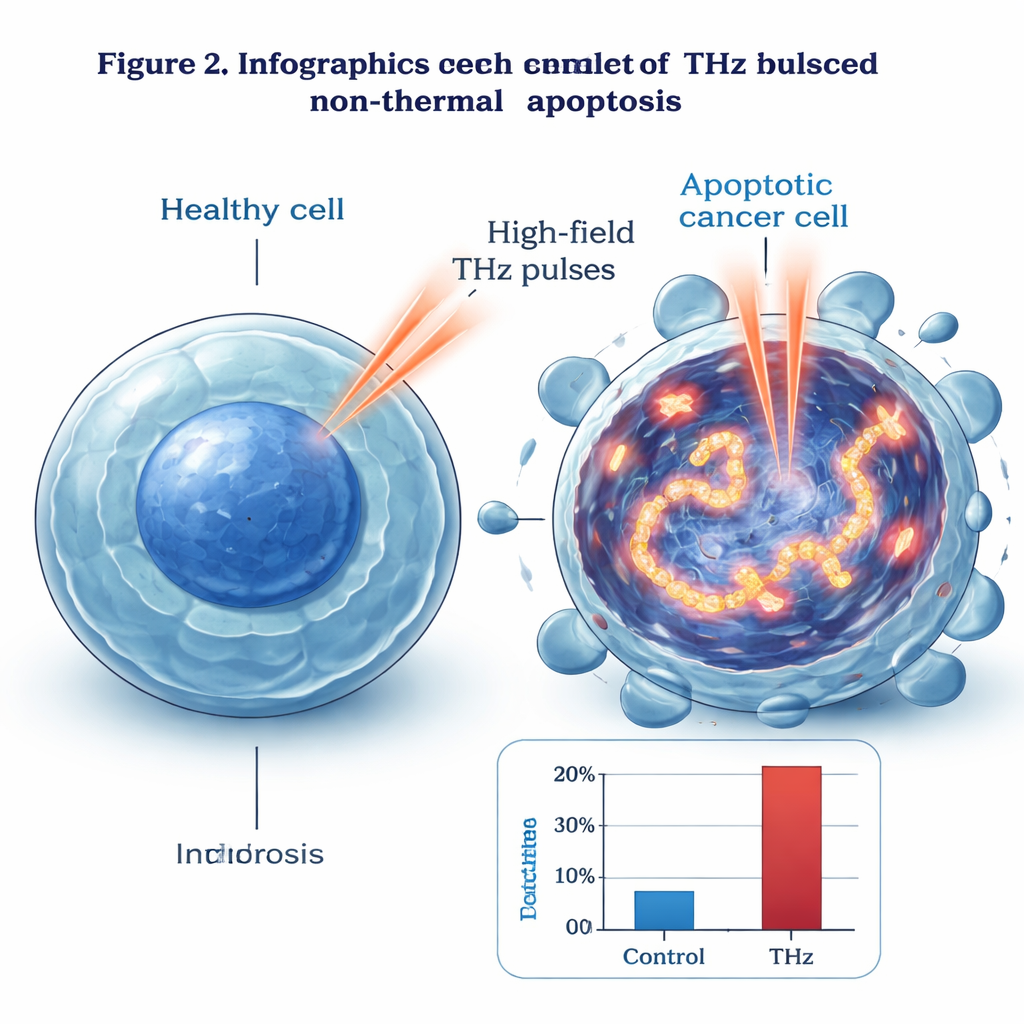
Van petrischaal naar toekomstige therapieën
Hoewel deze experimenten in celculturen werden uitgevoerd, wijzen ze op een nieuwe stijl van fysieke kankertherapie. Hoog-veld THz-golven lijken enkele millimeters in vochtig weefsel te kunnen doordringen — voldoende om oppervlakkige tumoren te bereiken — terwijl ze snel in sterkte afnemen, wat mogelijk dieper liggende organen spaart. Omdat het effect grotendeels niet-thermisch is, zou het in principe kankercellen laag voor laag kunnen doden zonder omliggend weefsel te verbranden of sterke ontstekingsreacties te veroorzaken. Er blijft veel werk: het voorgestelde DNA-“resonantie”-mechanisme moet bevestigd worden, de veiligheid voor normale cellen vereist grondige tests, en dier- en klinische studies zijn noodzakelijk. Toch opent dit onderzoek de deur naar het idee dat zorgvuldig ontworpen lichtpulsen, afgestemd op de natuurlijke bewegingen van biomoleculen, ooit een precieze en relatief zachte manier kunnen bieden om bepaalde vormen van kanker te ableren.
Bronvermelding: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Trefwoorden: terahertz-kankergeneeskunde, niet-thermische apoptose, DNA-dubbeldraadsbreuken, borstkankercellen, fysische tumorablatie