Clear Sky Science · nl
Gegeneraliseerde bloedvatmodellen voor op magnetische nanopartikelen gebaseerde oncologie: geometrische en microfluïdische eigenschappen
Gidsen van kleine magneten door het lichaam
Stel je voor dat je kankermedicijnen met een magneet rechtstreeks in een tumor kunt trekken, waardoor de rest van het lichaam gevrijwaard blijft van zware bijwerkingen. Deze studie onderzoekt hoe kleine magnetische deeltjes zich door bloedvatenachtige netwerken verplaatsen en stelt een bedrieglijk eenvoudige vraag: kunnen magneten onder realistische stromingscondities deze deeltjes daadwerkelijk sturen naar de plekken waar artsen ze willen hebben?
Waarom vaatgeometrie en stroming ertoe doen
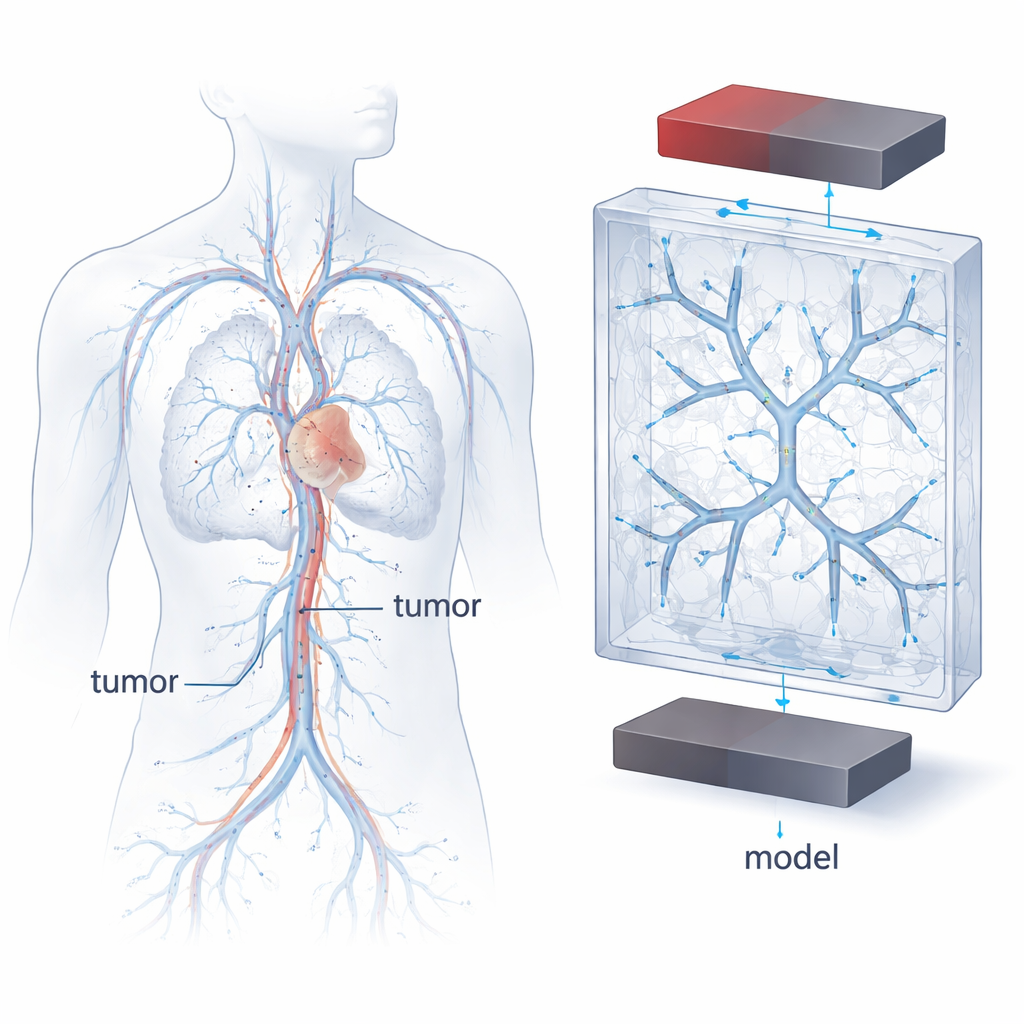
Magnetische kankertherapieën vertrouwen op superparamagnetische ijzeroxide-nanodeeltjes (SPIONs) die door een magnetisch veld kunnen worden aangetrokken terwijl ze medicijnen door de bloedbaan vervoeren. Maar bloedvaten zijn geen eenvoudige rechte buizen: ze takken af, vernauwen, kronkelen en splitsen, en de bloedstroomsnelheid neemt toe of af als reactie daarop. Deze veranderingen in vorm en snelheid beïnvloeden hoe deeltjes bewegen, waar ze zich ophopen en of ze lang genoeg de vatwand raken om te hechten. De bloedvaten van echte patiënten zijn extreem variabel, wat het moeilijk maakt experimenten te vergelijken of te voorspellen hoe een nieuwe therapie zal functioneren. De auteurs zetten zich daarom in om een sterk gecontroleerde, herhaalbare “modelvasculatuur” te bouwen die toch de essentiële kenmerken van tumorvoedende bloedvaten vastlegt.
Het bouwen van geïdealiseerde tumor-bloednetwerken
Om deze modelvaten te ontwerpen, baseerde het team zich op klassieke regels die beschrijven hoe echte slagaders vertakken. Een dergelijke regel, de wet van Murray, koppelt de diameters van ouder- en dochtervaten in een energie-efficiënt netwerk. Met klinische metingen van borstkankertumoren en deze schaalwetten genereerden de onderzoekers wiskundig vertakende bomen die nabootsen hoe tumorvoedende vaten krimpen richting het haarvatbed. Vervolgens gebruikten ze hoogresolutie 3D-printen om holle kanaalnetwerken met twee, drie of vier vertakkingniveaus in heldere plastic blokken in te bedden. De kanalen volgden een symmetrisch vertakkingspatroon en strekten zich in drie dimensies uit, wat een vereenvoudigd maar fysiologisch geïnspireerd landschap bood om de deeltjesbeweging te bestuderen.
Magnetische deeltjes in actie bekijken
Door deze geprinte netwerken pompte het team water als plaatsvervanger voor bloed, injecteerde vervolgens stroomopwaarts SPION-houdende vloeistof en bracht rondom het model een statisch magnetisch veld aan. Hoge-snelheidsopnamen leverden een filmachtig verslag van hoe de donkere deeltjeswolken door verschillende takken trokken, terwijl computeranalyse helderheidsveranderingen omzet in tijdsafhankelijke signalen die de lokale aanwezigheid van deeltjes weerspiegelen. Door de achtergrondstroomsnelheid, deeltjesconcentratie, de complexiteit van vertakkingen en de aanwezigheid of afwezigheid van een magneet te variëren, konden de onderzoekers uitzoeken hoe elk van deze factoren deeltjesdistributie, verblijftijd en uiteindelijke afzetting op kanaalwanden bepaalde.
Wanneer magneten helpen — en wanneer niet
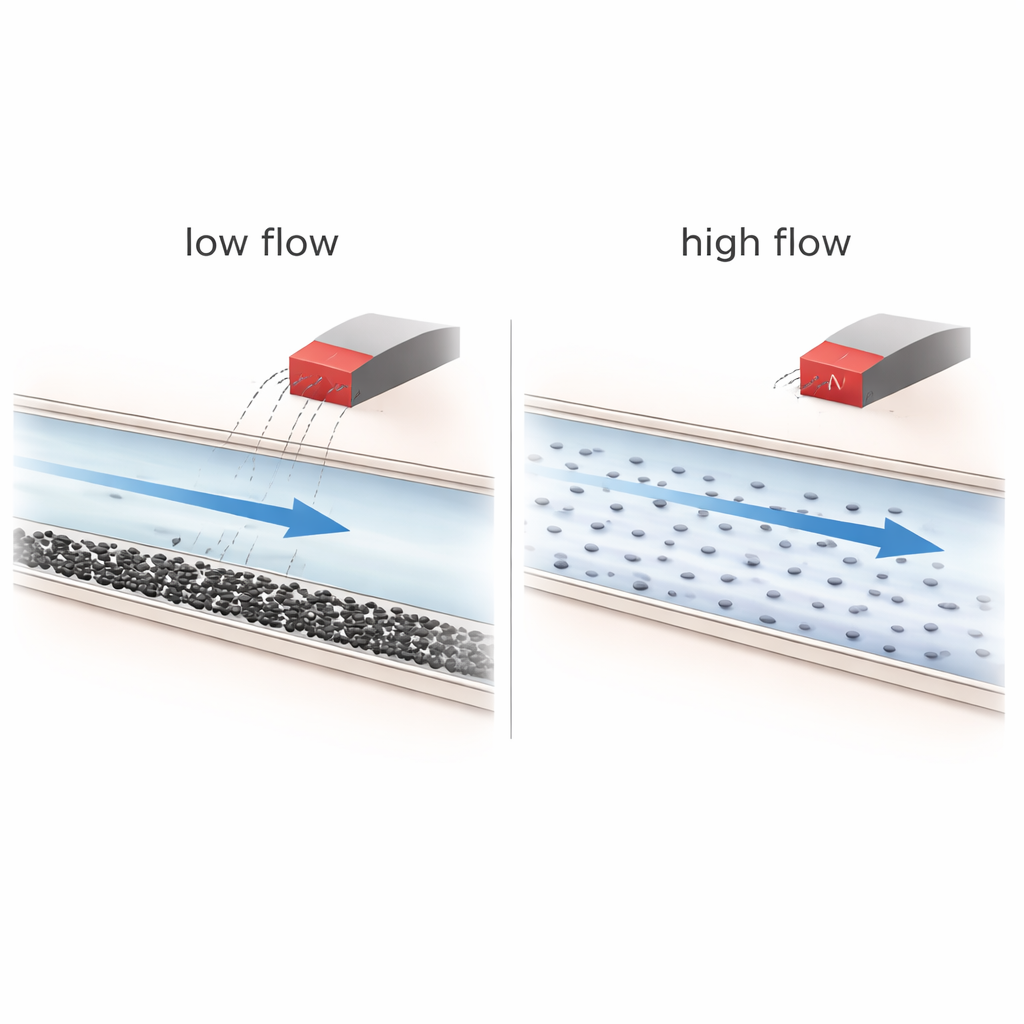
De experimenten laten zien dat stromingscondities de overhand hebben. Bij hogere stroomsnelheden wordt de vloeistof goed gemengd en bewegen de nanodeeltjes snel; onder deze omstandigheden heeft het magneetveld vrijwel geen invloed en volgen de deeltjes eenvoudig de stroomlijnen door het netwerk. Bij lage stroomsnelheden zorgen zwaartekracht en concentratie-effecten er echter voor dat deeltjes naar de bodem van de kanalen bezinken, waardoor gelaagde structuren en soms losse clusters ontstaan. In deze al onevenwichtige situatie kan de magneet meer deeltjes naar bepaalde takken duwen en hun verblijftijd enigszins verlengen, met name in complexere, sterk vertakte netwerken. Berekeningen laten echter zien dat de magnetische kracht op een enkel 40-nanometer deeltje vele ordes van grootte zwakker is dan de viskeuze weerstand van de stromende vloeistof, waardoor echte “sturing van individuele deeltjes” fysisch onrealistisch is onder de geteste omstandigheden.
Wat dit betekent voor toekomstige kankertherapieën
Voor een niet-specialist is de belangrijkste conclusie dat magneten op zichzelf niet betrouwbaar vrij zwevende nanodeeltjes uit een snelstromende bloedbaan kunnen trekken. Merkbare magnetische effecten treden alleen op wanneer deeltjes al vertraagd, bezonken of geclusterd zijn—situaties die hun magnetische reactie effectief vergroten. De gegeneraliseerde, 3D-geprinte vaatmodellen die hier worden geïntroduceerd, bieden een gestandaardiseerde manier om dergelijke effecten te onderzoeken over verschillende netwerkgeometrieën en stromingsregimes. Voor toekomstige magnetische medicijndoelstelling suggereert dit werk dat succesvolle strategieën waarschijnlijk gebruik zullen moeten maken van collectief gedrag—zoals gecontroleerde aggregatie of dragersystemen— in plaats van te vertrouwen op het sturen van geïsoleerde nanodeeltjes door grote, snel geperfuseerde vaten.
Bronvermelding: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Trefwoorden: magnetische medicijndoelstelling, nanodeeltjes, tumorvasculatuur, microfluïdische modellen, medicijnbezorging