Clear Sky Science · nl
Een tri-omics- en machine learning-kader identificeert prognostische biomarkers en metabole handtekeningen bij sepsis
Waarom dit van belang is voor mensen met ernstige infecties
Sepsis is een levensbedreigende reactie op een infectie die het immuunsysteem in overdrive kan brengen en tot orgaanfalen kan leiden. Artsen weten dat het vroeg herkennen van sepsis en het afstemmen van de behandeling op de individuele patiënt levens kan redden, maar de huidige bloedtests zijn grove instrumenten: ze zeggen vaak weinig over wie zal herstellen en wie het hoogste risico loopt. Deze studie gebruikt een krachtige combinatie van drie soorten moleculaire metingen en moderne machine learning om preciezere waarschuwingssignalen in het bloed van sepsispatiënten te vinden.
Het bloed bekijken door drie verschillende lenzen
In plaats van te focussen op één type molecuul, brachten de onderzoekers dezelfde patiënten op drie manieren tegelijk in kaart. Ze maten welke genen aan- of uitgezet waren (transcriptomica), welke eiwitten daadwerkelijk aanwezig en actief waren (proteomica) en welke kleine metabole moleculen circuleerden (metabolomica). Ze verzamelden bloed van 21 sepsispatiënten en 10 gezonde vrijwilligers en gebruikten geavanceerde statistiek om te zien hoe die drie lagen samen veranderden bij ziekte. Dit "tri-omics"-perspectief helpt een belangrijk probleem te overwinnen: bij sepsis kunnen genactiviteit en eiwitniveaus ontkoppeld raken, waardoor het kijken naar slechts één laag misleidend kan zijn.
Algoritmen leren risicopatronen te herkennen
Uit duizenden genen en eiwitten gebruikte het team eerst een netwerkmethode om groepen te vinden die samen verschilden bij sepsis. Ze controleerden die groepen vervolgens met eiwitten die duidelijk verschilden tussen patiënten en gezonde controles en kwamen uit op 32 sterke kandidaten. Om deze lijst verder in te perken, zetten ze machine learning in, waarbij twee complementaire algoritmen zwakkere signalen weghaalden en alleen de meest informatieve overlieten. Toen ze testten hoe deze overgebleven genen samenhingen met overleving in een grote openbare sepsis-dataset, vielen twee eruit: TPR en ERN1. Patiënten met hogere TPR-niveaus hadden doorgaans een betere overleving, terwijl hogere ERN1 geassocieerd was met slechtere uitkomsten.
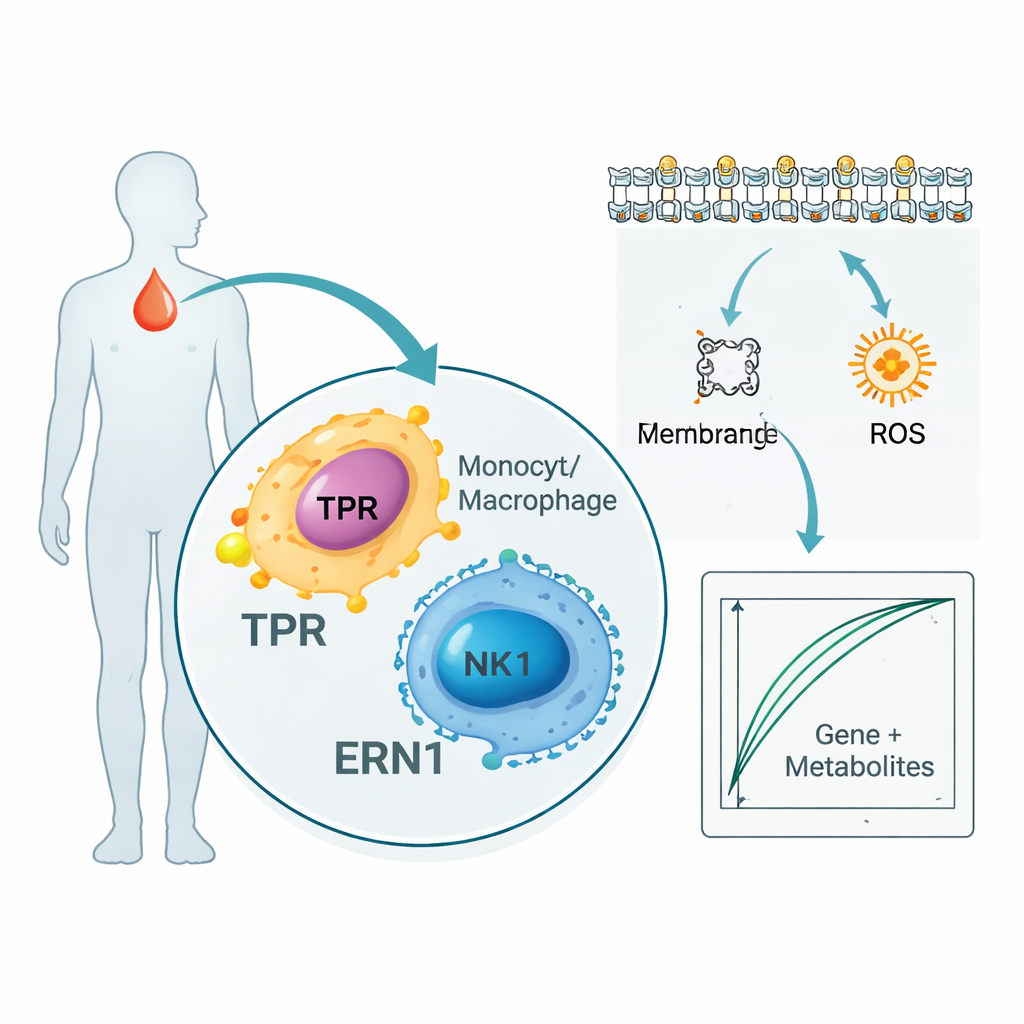
De koppeling tussen immuuncellen en verstoorde stofwisseling
De studie bleef niet bij genen en eiwitten. Door duizenden metabolieten in het bloed van patiënten te scannen, vonden de onderzoekers 136 kleine moleculen die sterk meetrokken met TPR en ERN1. Veel daarvan hoorden bij routes die membranen vetten en vetzuren verwerken, processen die cruciaal zijn voor hoe immuuncellen signaleren en hoe ontsteking zich verspreidt. Tegelijkertijd toonde een single-cell-analyse — die individuele immuuncellen in het bloed bekijkt in plaats van ze te mengen — dat TPR en ERN1 vooral actief zijn in monocyten, macrofagen en natural killer-cellen. Samen suggereren deze resultaten dat de twee markers op het kruispunt zitten tussen de infectiebestrijdende cellen van het lichaam en de manier waarop die cellen vetten en energie gebruiken en herstructureren tijdens sepsis.
Het bouwen van een proof‑of‑concept-bloedtest
Om te verkennen hoe deze ontdekkingen in de praktijk zouden kunnen werken, combineerden de auteurs de twee genen met vijf van de meest informatieve metabolieten om eenvoudige computermodellen te trainen die sepsispatiënten van gezonde personen scheiden. In hun kleine interne dataset konden deze gecombineerde "gen-plus-metaboliet"-handtekeningen bijna perfect aangeven wie sepsis had. De onderzoekers bekeken ook grote openbare databases die bloedproteïnen koppelen aan ziekte-risico’s in tienduizenden mensen en vonden dat TPR- en ERN1-eiwitniveaus consequent geassocieerd waren met sepsisgerelateerde aandoeningen, wat een extra steunlaag biedt. De auteurs benadrukken echter dat dit modellen in een vroeg stadium zijn, bedoeld om hypothesen te genereren en geen kant-en-klare bedidentests.
Plantaardige verbindingen als vroege aanwijzingen, geen geneesmiddelen
In een laatste stap onderzochten de onderzoekers of natuurlijke moleculen TPR of ERN1 zouden kunnen beïnvloeden. Ze doorzochten een gespecialiseerde database met bijna 500 gezuiverde verbindingen uit traditionele Chinese medicijnen, elk met een eigen genactiviteitsprofiel. Verschillende verbindingen leken deze twee genen in gekweekte cellen sterk omhoog of omlaag te duwen, wat suggereert dat ze onderzoekers ooit kunnen helpen de biologie van sepsis te onderzoeken of nieuwe geneesmiddelen te ontwerpen. Deze bevindingen zijn echter uitsluitend afkomstig van computermatching: ze tonen niet aan dat een van deze stoffen veilig of effectief is voor mensen met sepsis.
Wat dit werk ons echt vertelt
Deze studie biedt eerder een gedetailleerde kaart dan een afgeronde oplossing. Door drie moleculaire lagen, single-cell-gegevens en machine learning te verweven, benadrukken de auteurs TPR en ERN1 — en de daaraan verbonden metabole veranderingen — als veelbelovende wegwijzers voor hoe het immuunsysteem en de stofwisseling uit balans raken bij sepsis. Voor een lezer zonder achtergrond is de kernboodschap dat sepsis geen eenduidige ziekte is maar een verschuivend patroon van immuun- en metabole toestanden, en dat slimmere bloedtests artsen mogelijk in de toekomst kunnen helpen zien in welke toestand een patiënt verkeert en de behandeling daarop aan te passen. Voordat dat gebeurt, moeten deze vroege signalen worden getest en bevestigd in veel grotere, diverse patiëntengroepen en in laboratoriumexperimenten die oorzaak en gevolg kunnen aantonen.
Bronvermelding: Li, X., Ke, G., Hu, Y. et al. A tri-omics and machine learning framework identifies prognostic biomarkers and metabolic signatures in sepsis. Sci Rep 16, 6648 (2026). https://doi.org/10.1038/s41598-026-37342-z
Trefwoorden: sepsis biomarkers, multi-omics, machine learning in medicine, immune metabolism, precision diagnostics