Clear Sky Science · nl
Het richten op de Akt–EphA2-as en cel‑cel hechting verhoogt de gevoeligheid voor anoïkis in kankercellen
Waarom vrij zwevende kankercellen ertoe doen
Wanneer kankercellen losraken van een tumor en via de bloedbaan reizen, zouden ze normaal gesproken sterven omdat ze het contact met het omringende weefsel verliezen. Dit ingebouwde beveiligingsprogramma, detachement‑geïnduceerde celdood genoemd, voorkomt dat cellen onbedoeld groeien op plaatsen waar ze niet thuishoren. Metastatische kankercellen leren dit signaal echter vaak te negeren en blijven in leven terwijl ze zweven, waardoor ze gemakkelijker nieuwe tumoren kunnen vormen. Deze studie stelt een deceptief eenvoudige vraag: als we een cruciaal mechanisch “gevoel voor aanraking” herstellen in agressieve borstkankercellen, kunnen we die zwervende cellen dan dwingen te sterven, en zo niet, welke reserve‑trucs gebruiken ze om te overleven?
Een verloren gevoel voor aanraking heractiveren
Cellen testen voortdurend hoe stijf hun omgeving is door te trekken aan de structuren die ze verankeren. In gezond weefsel leidt het verlies van contact of het landen op een zeer zachte ondergrond vaak tot zelfdestructie. Het eiwit Tropomyosin 2.1 (Tpm2.1) is een belangrijk onderdeel van dit interne spanningsmechanisme en ontbreekt of is vaak verminderd in kankercellen. De onderzoekers gebruikten een veel bestudeerde metastatische borstkankercellijn en implementeerden extra Tpm2.1, waarmee een groot deel van deze stijfheidswaarneming werd hersteld. Toen deze gemodificeerde cellen gedwongen werden te groeien in speciale niet‑klevende schalen die hechting verhinderen, ondergingen ze wel meer celdood, groeiden ze langzamer en bewogen ze minder dan ongewijzigde kankercellen. Toch was na meerdere dagen in suspensie nog steeds ongeveer 70% van de Tpm2.1‑expressing cellen levensvatbaar, wat suggereert dat het alleen herstellen van hun gevoel voor aanraking het probleem niet volledig oplost.
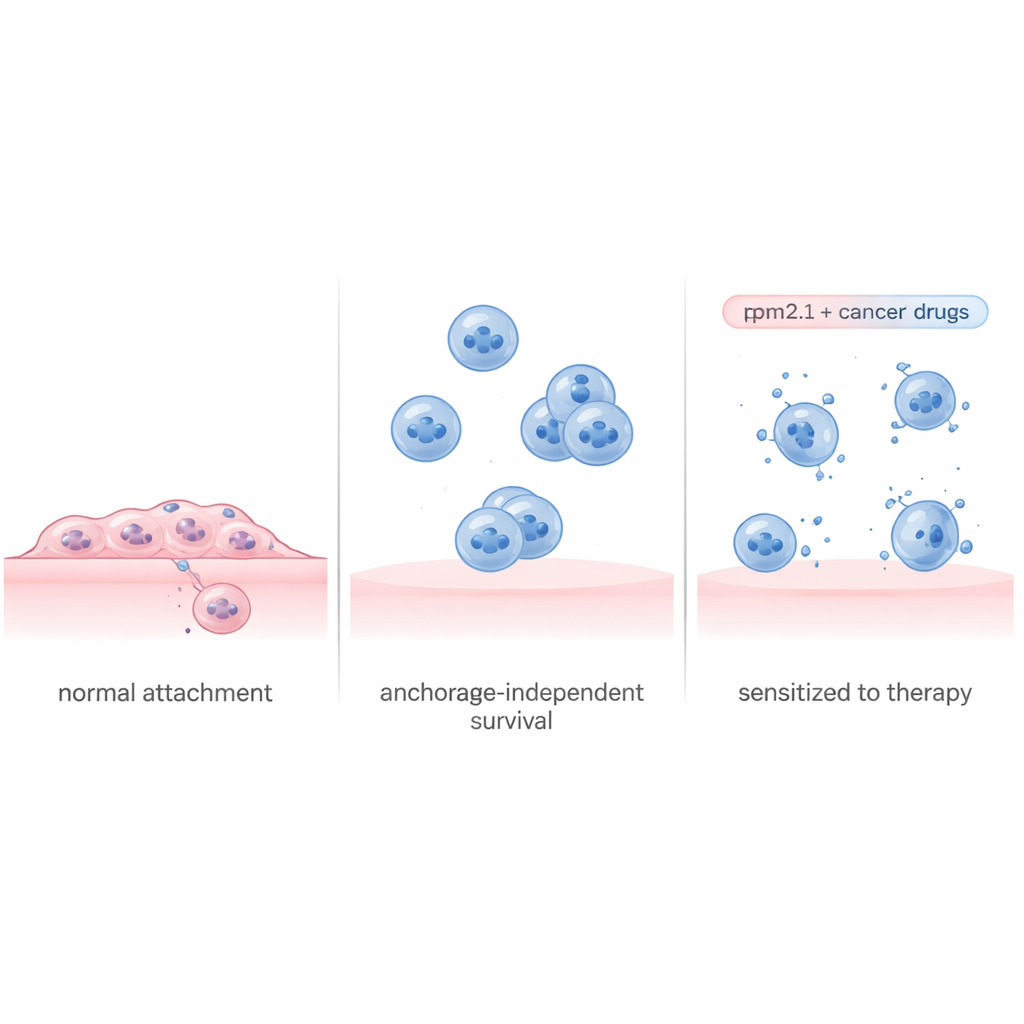
Het overlevingsspelboek van kankercellen lezen
Om te begrijpen waarom sommige cellen stierven terwijl andere bleven leven, scheidde het team de zwevende Tpm2.1‑expressing cellen in twee groepen: degenen die vroege tekenen van celdood toonden en degenen die er gezond uitzagen. Ze maten vervolgens welke genen in elke groep aan‑ of uitgeschakeld waren gedurende vier dagen. De stervende cellen lieten een brede stillegging zien van programma’s die betrokken zijn bij celdeling, DNA‑herstel en hechting, samen met stresssignalen die op een eenrichtingsweg naar zelfvernietiging leken. Daarentegen activeerden de overlevende cellen een gecoördineerd overlevingsplan. Vroeg na loslating schakelden ze ontstekings‑ en immuungerelateerde routes aan en later tilden ze grote groei‑ en overlevingscircuiten op, waaronder een bekende route gecentreerd rond het eiwit Akt. Tegelijkertijd verhoogden ze sterk genen die cellen helpen aan elkaar te hechten, zodat ze beschermende clusters kunnen vormen, zelfs zonder zich aan de omringende matrix vast te klampen.
Sterkte in aantallen: hoe celclust ers weerstand bieden tegen dood
Omdat de genexpressiegegevens wezen op verhoogde cel‑cel hechting, testten de onderzoekers of eenvoudige opeenhoping cellen kan helpen te overleven in suspensie. Wanneer Tpm2.1‑expressing cellen bij hoge dichtheid werden gekweekt, waar clustering gemakkelijk was, stierven veel minder cellen dan wanneer ze dun waren verspreid. Eén adhesiemolecuul, ICAM1, sprong eruit als bijzonder verhoogd in de overlevende cellen en staat al bekend om te helpen bij de vorming van clusters van circulerende tumorcellen die zich in verre weefsels nestelen. Het blokkeren van ICAM1 met een kleine molecule‑remmer zorgde ervoor dat meer van de Tpm2.1‑expressing cellen in suspensie stierven, terwijl het weinig effect had op standaard aangehechte kweekcondities. Deze bevindingen ondersteunen het idee dat, zodra hun interne mechanica gedeeltelijk is hersteld, kankercellen alsnog aan de dood kunnen ontsnappen door letterlijk aan elkaar vast te houden in plaats van aan hun omgeving.
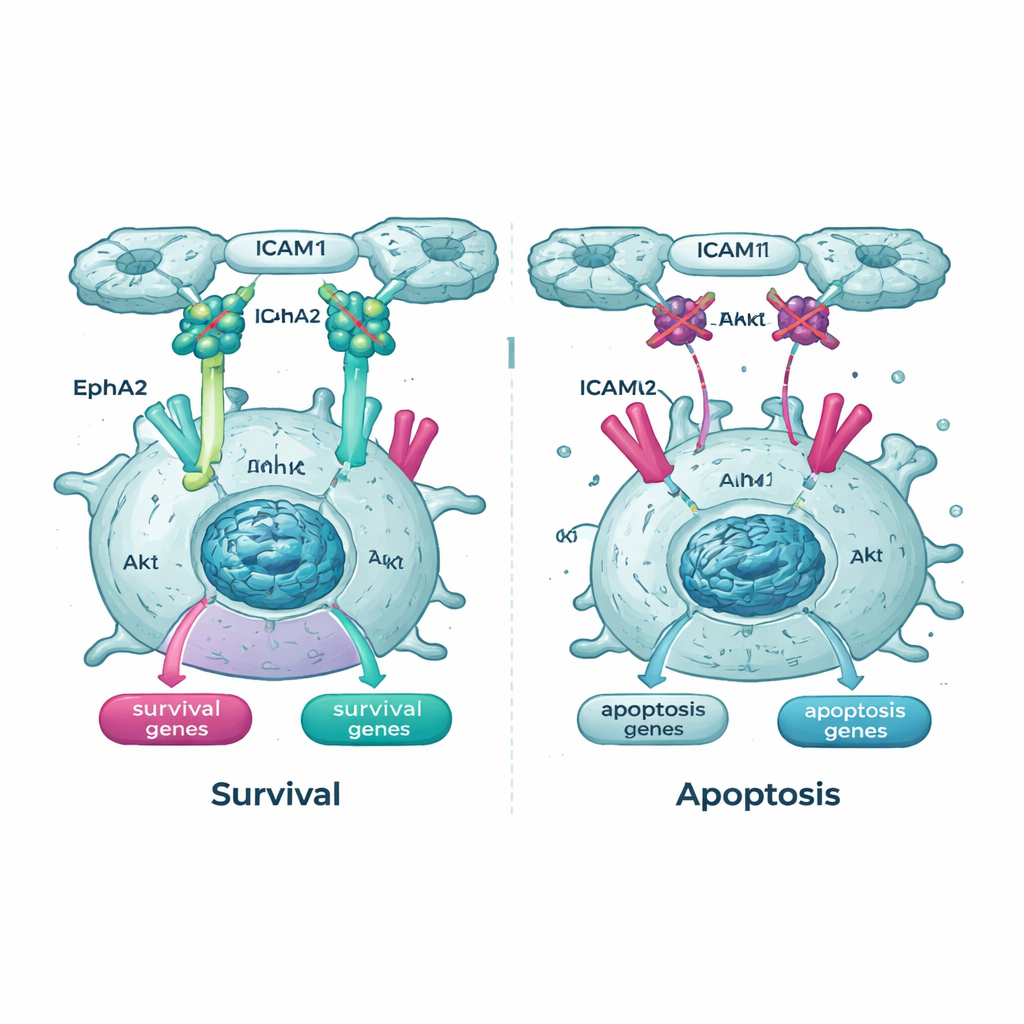
Belangrijke levenslijnen binnenin de cel doorknippen
De genetische onderzoeken belichtten ook de Akt‑route en een van zijn partners, een receptor genaamd EphA2, als belangrijke levenslijnen voor zwevende kankercellen. In Tpm2.1‑expressing cellen was de actieve, gefosforyleerde vorm van Akt in suspensie lager dan in controlecellen, en de niveaus en activiteit van EphA2 waren eveneens verminderd. Toen het team cellen behandelde met geneesmiddelen die Akt of EphA2 blokkeren, werden zowel normale als Tpm2.1‑expressing kankercellen veel gevoeliger voor celdood in suspensie. Opmerkelijk genoeg waren de cellen met herstelde stijfheidswaarneming na verloop van tijd bijzonder gevoelig voor deze middelen, wat suggereert dat zodra hun mechanische beveiligingschecks deels opnieuw ingeschakeld zijn, ze sterker afhankelijk worden van de resterende overlevingssignalen.
Een geprimede toestand omzetten in een dodelijke zwakte
Voor niet‑specialisten is de kernboodschap dat het repareren van één kapotte veiligheidschakelaar in kankercellen — hun vermogen om te voelen en te reageren op het verlies van contact — noodzakelijk maar niet voldoende is om ze tot zelfvernietiging te dwingen. De cellen die overleven doen dat door zich samen te sluiten en hun interne bedrading om te leiden via alternatieve groei‑ en overlevingspaden. Dit werk toont dat het herstellen van stijfheidswaarneming met Tpm2.1 metastatische borstkankercellen in een “geprimede” toestand brengt waarin ze dichter bij de dood staan maar nog niet toezeggen. Door vervolgens de Akt–EphA2‑route te blokkeren en cel‑cel hechting via ICAM1 te verstoren, kunnen onderzoekers deze geprimede cellen over de rand duwen en detachement‑geïnduceerde celdood sterk vergroten. Praktisch gezien schetst de studie een strategie voor toekomstige combinatietherapieën gericht op het uitroeien van vrij zwevende tumorcellen voordat ze nieuwe metastasen kunnen zaaien.
Bronvermelding: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Trefwoorden: borstkanker‑metastase, celhechting, anoïkis, Akt‑signalering, stijfheidswaarneming