Clear Sky Science · nl
Invloed van de gedefinieerde Oligo-MM12-microbiota op darmkolonisatie en verspreiding van Listeria monocytogenes
Waarom de microben in je darm ertoe doen
Veel mensen kennen Listeria monocytogenes als een gevaarlijke voedseloverdraagbare bacterie die verband houdt met besmette kant-en-klaarproducten en ernstige ziekte bij kwetsbare personen. Minder duidelijk is dat of deze bacterie voet aan de grond krijgt in het lichaam niet alleen afhangt van ons immuunsysteem, maar ook van de drukke gemeenschap van microben die al in onze darmen woont. Deze studie gebruikt speciaal ontworpen muismodellen en een miniatuur “kunstmatige dikke darm” om een eenvoudige maar belangrijke vraag te stellen: hoe beïnvloedt de complexiteit van het darmmicrobioom Listeria’s vermogen om de darm te koloniseren en zich door het lichaam te verspreiden?
Een verhaal van twee microbieel wijken
Om deze vraag te onderzoeken vergeleken de onderzoekers twee soorten muizen. De ene groep, SPF-muizen genoemd, droeg een rijke, natuurlijke mix van darmbacteriën die lijkt op wat in veel laboratoriumdieren voorkomt. De andere groep, Oligo-MM12-muizen, huisvestte een veel eenvoudiger gemeenschap bestaande uit slechts 12 goed gekarakteriseerde bacteriestammen. Omdat elk lid van deze gemeenschap bekend is en stabiel over generaties, zijn Oligo-MM12-muizen een krachtig hulpmiddel om uit te zoeken welke microben helpen indringers te blokkeren en welke mogelijk gaten in onze verdediging laten. Door deze muizen te contrasteren kon het team testen hoe een dicht, divers darmecosysteem zich onderscheidt van een gestroomlijnd, minimalistisch systeem bij het omgaan met een infectieuze uitdaging.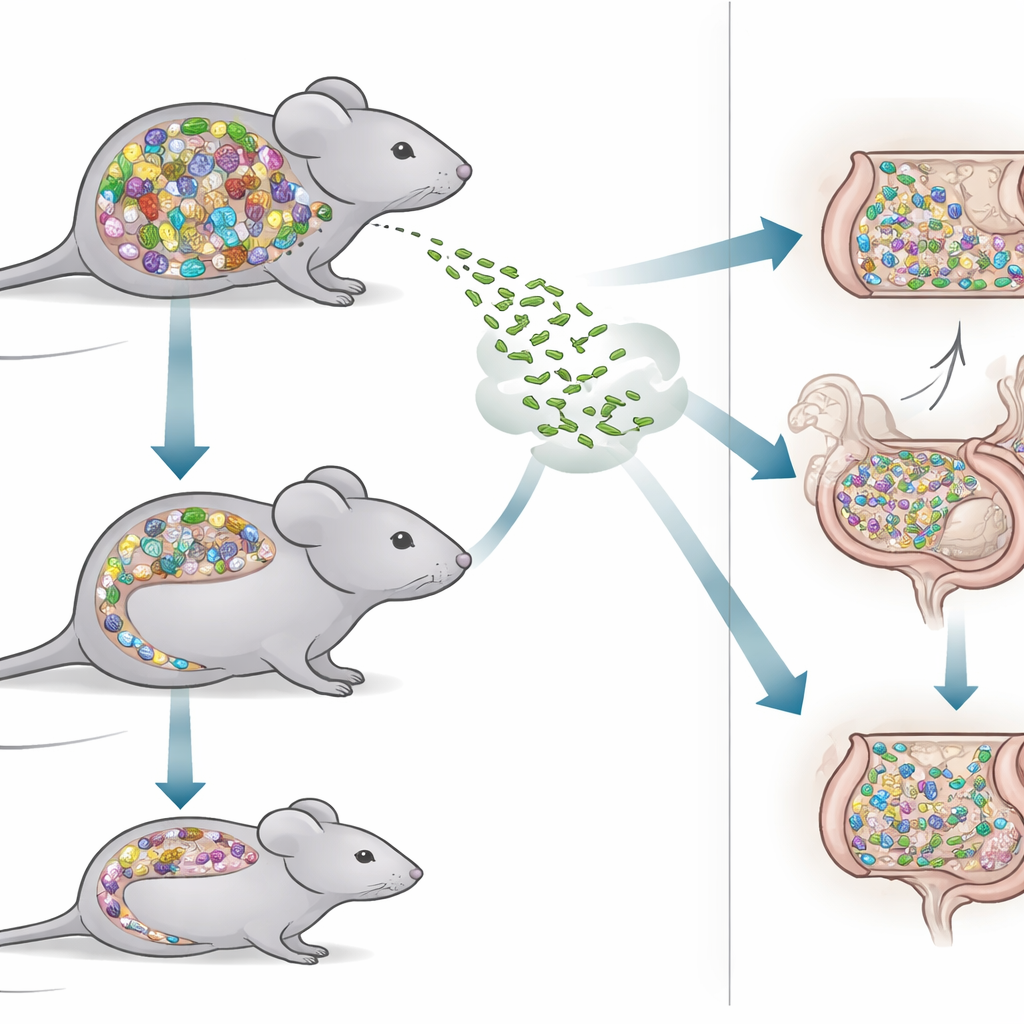
Listeria volgen door de darm en verder
De wetenschappers infecteerden beide muistypen met dezelfde orale dosis Listeria en volgden hoeveel bacteriën er in de ontlasting en inwendige organen verschenen over drie dagen. Interessant genoeg leek de eenvoudigere Oligo-MM12-gemeenschap aanvankelijk beter in het onder controle houden van Listeria: op de eerste dag na infectie scheidden deze muizen minder Listeria-cellen uit in hun stoelgang dan de SPF-muizen. Die vroege voorsprong vervaagde echter. Op de derde dag scheidden Oligo-MM12-muizen meer Listeria uit, terwijl SPF-muizen de aantallen geleidelijk wisten terug te dringen. Ondanks deze duidelijke verschillen in de darm waren de aantallen Listeria in inwendige organen zoals de lever, milt en lymfeklieren vergelijkbaar tussen de twee muismodellen, wat suggereert dat zodra Listeria dieper weefsels bereikt, de complexiteit van het microbioom een kleinere rol speelt.
De dikke darm simuleren in een gecontroleerde doos
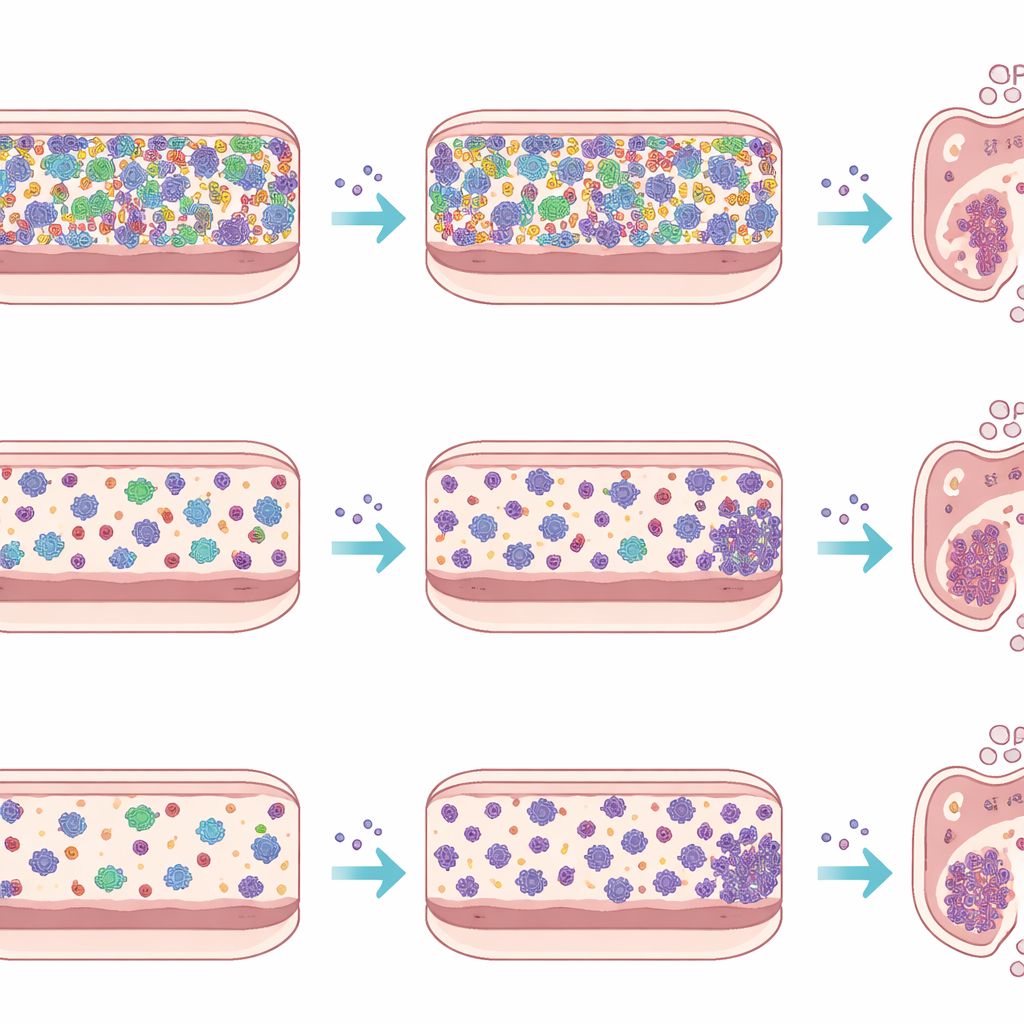
Om de effecten van gastheerweefsels en immuniteit te scheiden van het gedrag van de microben zelf, voerde het team ook een ex vivo-experiment uit met een apparaat genaamd de micro-Matrix-bioreactor. Ze maakten fecale suspensies van elk muistype, voegden die toe aan een voedingsrijk medium in afgesloten, zuurstofvrije wells, en introduceerden Listeria in sommige van deze miniatuurculturen terwijl anderen als controle dienden. Gedurende vijf dagen maten ze Listeria-aantallen en sequentieerden bacterieel DNA om te volgen hoe de gemeenschappen evolueerden. In deze kunstmatige dikke darm groeide Listeria tot vergelijkbare niveaus ongeacht of het geconfronteerd werd met de complexe SPF-microbiota of de eenvoudigere Oligo-MM12-gemeenschap, en haar aanwezigheid veroorzaakte slechts bescheiden verschuivingen in de algehele samenstelling van de gemeenschap. Dit contrast met de levende dieren benadrukt hoe sterk het immuunsysteem, de darmwand en de stromen van gal en slijm de infectie in de echte darm vormen.
Belangrijke microbieel winnaars, verliezers en toeschouwers
Door te kijken welke bacteriegroepen tijdens de infectie in aantal toenamen of afnamen, identificeert de studie kandidaten die mogelijk invloed hebben op Listeria’s succes. In Oligo-MM12-muizen daalden de niveaus van Akkermansia, een slijmgeassocieerde bacterie die vaak wordt gelinkt aan darmgezondheid, op de tweede dag en veerden ze sterk terug op dag drie. Bij SPF-muizen namen verschillende genera die bekendstaan om het produceren van gunstige metabolieten of het ondersteunen van de barrièrefunctie, zoals Blautia en Bacteroides, af tijdens de infectie, terwijl bepaalde Prevotella-achtige bacteriën complexe stijgingen en dalingen lieten zien die mogelijk wijzen op directe targeting door Listeria’s eigen antimicrobiële verbindingen. Ex vivo waren deze patronen grotendeels afgezwakt, wat het idee versterkt dat veel van de waargenomen verschuivingen voortkomen uit driehoeksinteracties tussen pathogeen, resident-microben en de gastheeromgeving in plaats van uit eenvoudige microbe–microbecompetitie alleen.
Wat dit betekent voor de bescherming van mensen
Voor niet-specialisten is de kernboodschap dat niet alle gezond-ogende microbiomen op dezelfde manier beschermen tegen infectie, en dat “meer diversiteit” niet altijd op elk moment beter is. De vereenvoudigde Oligo-MM12-gemeenschap gaf een sterke vroege weerstand tegen Listeria in de darm, maar na verloop van tijd deed het meer ingewikkelde SPF-microbioom het beter in het uitroeien van de indringer. Het werk toont aan dat zorgvuldig ontworpen, laag-complexe microbiotamodellen, gecombineerd met beheersbare ex vivo-systemen, kunnen onthullen welke bacteriegroepen en omgevingsfactoren cruciaal zijn voor het blokkeren van gevaarlijke voedselpathogenen. Uiteindelijk zouden zulke inzichten kunnen leiden tot gerichte probiotica of microbioom-gebaseerde therapieën die de juiste microbiële bondgenoten op het juiste moment versterken om ernstige Listeria-infecties bij risicopatiënten te voorkomen.
Bronvermelding: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Trefwoorden: Listeria-infectie, darmmicrobioom, kolonisatieweerstand, muismodel, probiotica