Clear Sky Science · nl
Een deep learning-ensemble raamwerk voor multi-subtypering van niertumoren met behulp van contrastversterkte CT
Waarom het vroeg ontdekken van niertumoren belangrijk is
Nierkanker kan jaren stil blijven, met weinig symptomen totdat het zich al heeft verspreid. Met moderne beeldvorming worden veel niermassa’s echter toevallig ontdekt tijdens scans voor rugklachten of andere problemen. De centrale vraag wordt dan: is de massa levensbedreigende kanker die operatief verwijderd moet worden, of een goedaardige aandoening die volstaan kan worden met afwachtend beleid? Deze studie onderzoekt hoe kunstmatige intelligentie artsen kan helpen CT-scans nauwkeuriger te beoordelen, zodat onnodige ingrepen worden verminderd terwijl agressieve tumoren tijdig worden opgespoord.
Vijf typen nierknobbels, één lastige afweging
Niet alle niertumoren zijn hetzelfde. Sommige, zoals angiomyolipoom (AML) en renaal oncocytoom (RO), zijn goedaardig en kunnen mogelijk nooit een levensbedreiging vormen. Andere, gegroepeerd onder renaalcelcarcinoom (RCC), zijn kwaadaardig en kunnen uitzaaien naar andere organen. Onder de kwaadaardige nierkankers is clear cell RCC (ccRCC) het meest voorkomend en het meest geneigd te metastaseren; papillaire RCC (pRCC) en chromofobe RCC (chRCC) zijn over het algemeen minder agressief maar nog steeds ernstig. Op gewone scans kunnen deze subtypen echter verrassend gelijkend zijn, zodat artsen vaak op een biopsie of operatie vertrouwen voor een definitieve diagnose. De auteurs wilden nagaan of een geavanceerd computersysteem deze vijf tumorsoorten betrouwbaar kon onderscheiden met alleen contrastversterkte CT-beelden.
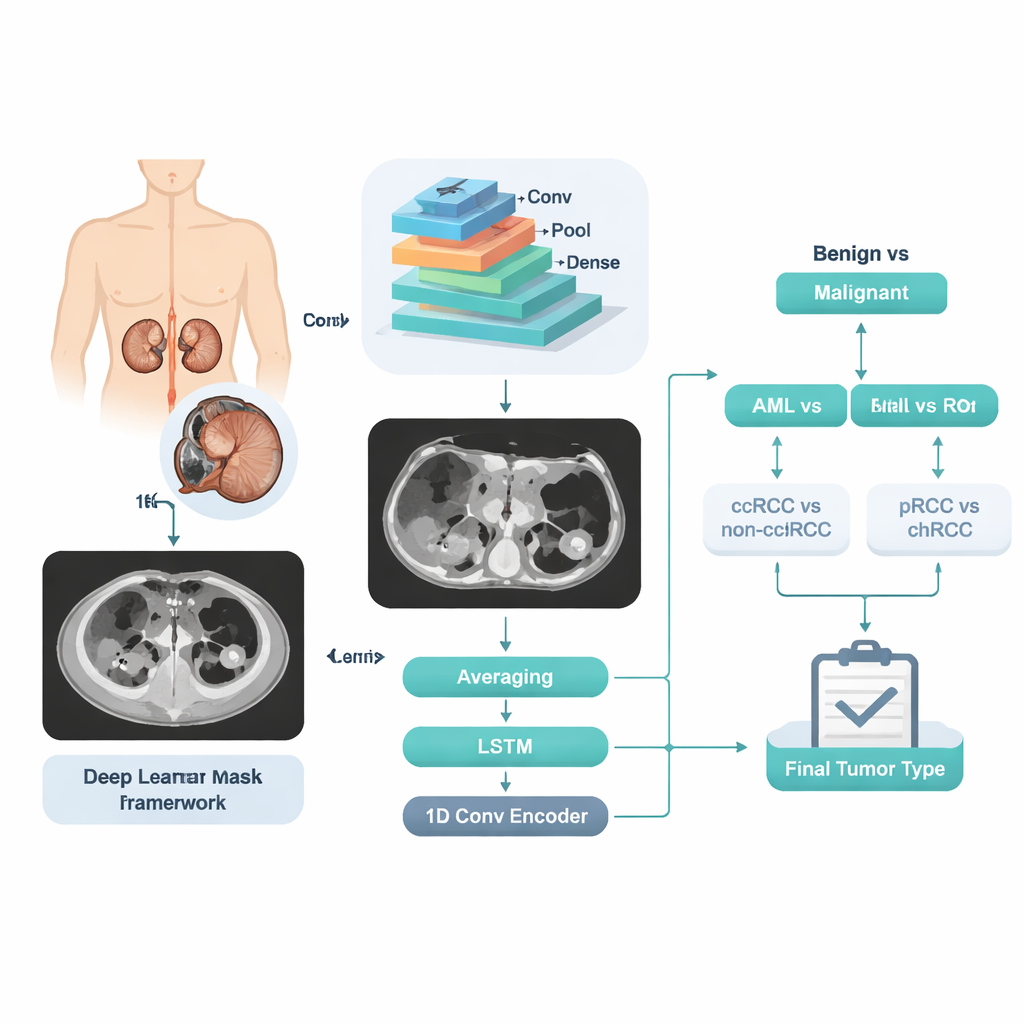
CT-scans omzetten in leerbare patronen
Het team verzamelde contrastversterkte CT-scans van 280 patiënten bij wie de niertumoren al door weefselanalyse waren bevestigd. Ervaren radiologen tekenden elke tumor zorgvuldig met de hand af, plakje voor plakje, om nauwkeurige “grondwaarheid”-regio’s te bieden waar het systeem van kon leren. Er werd slechts één CT-fase gebruikt — de porta-veneuze fase, die gangbaar is in de dagelijkse praktijk — wat benadrukt dat de methode met standaard ziekenhuisbeeldvorming moet werken. De dataset bevatte uiteindelijk vijf duidelijk gelabelde groepen: 84 ccRCC-, 36 pRCC-, 48 chRCC-, 72 AML- en 40 RO-gevallen, verdeeld over een ruime leeftijdsspreiding en beide geslachten. De auteurs verdeelden de gevallen vervolgens per patiënt in trainings-, validatie- en testsets, zodat beelden van dezelfde persoon nooit in meer dan één groep voorkwamen.
Een stapsgewijs digitaal second opinion
In plaats van het systeem rechtstreeks van beeld naar één van vijf labels te laten springen, ontwierpen de onderzoekers een stapsgewijze beslispijplijn die het redeneren van een arts weerspiegelt. Eerst bepaalt het systeem of een tumor goedaardig of kwaadaardig is. Bij goedaardig volgt een tweede beslissing om AML van RO te scheiden. Bij kwaadaardig splitst een volgende beslissing ccRCC van de andere RCC-types, gevolgd door een laatste stap die pRCC van chRCC onderscheidt. In elke stap analyseert een krachtig beeldanalyse‑model, een convolutioneel neuraal netwerk, vele plakjes van dezelfde patiënt. De interne numerieke “features” worden vervolgens op drie verschillende manieren verwerkt: door eenvoudige middelen van de voorspellingen per plakje, door een sequentiebewust model dat kijkt hoe de tumor over de plakjes verandert, en door een compacte encoder die de hele stapel samenvat tot één signatuur. De drie adviezen worden samengevoegd tot één eindkans voor die fase.
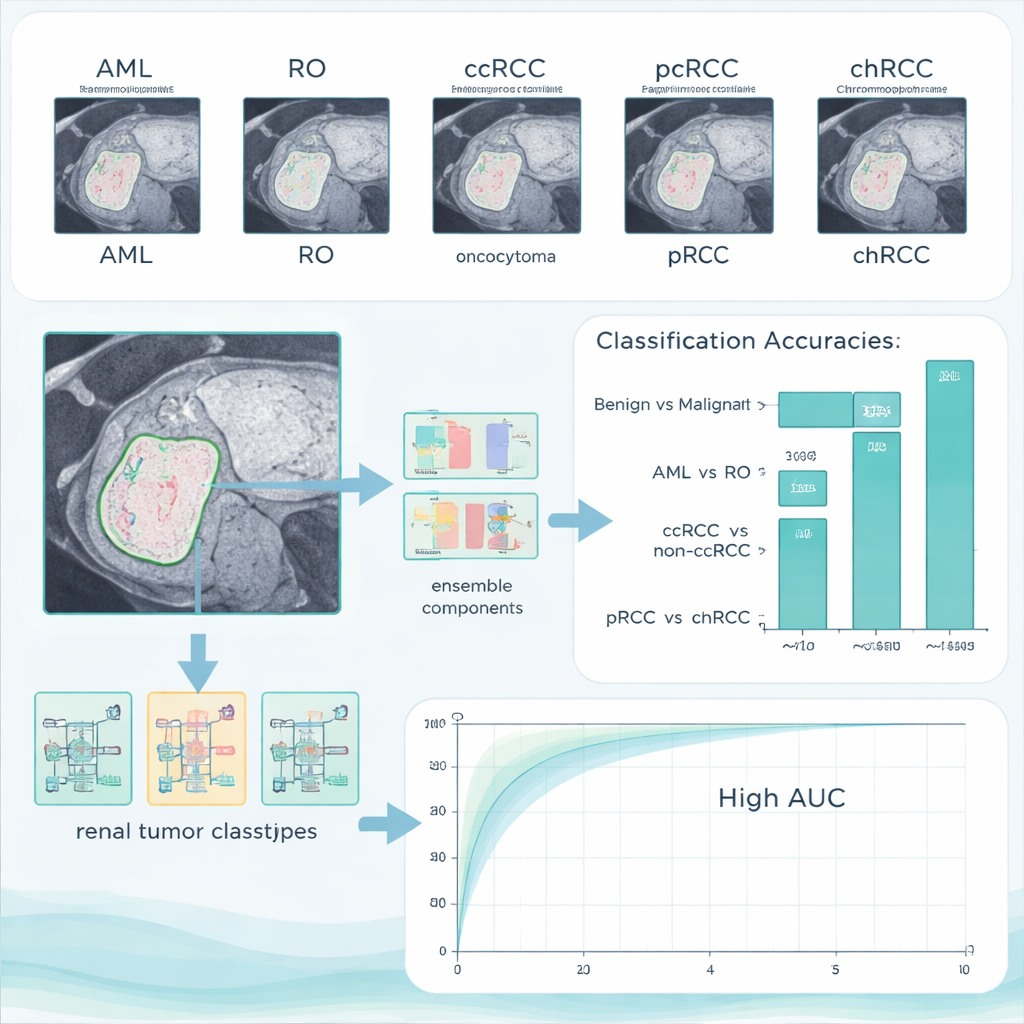
Hoe goed het AI-systeem presteerde
Op hun hoofdtestset bereikte het gecombineerde systeem 96,4% nauwkeurigheid bij het scheiden van goedaardige en kwaadaardige tumoren, zonder dat goedaardige gevallen ten onrechte als kanker werden gelabeld en met slechts een klein aantal gemiste kankergevallen. Bij het onderscheiden van de twee goedaardige types behaalde het een perfecte 100% nauwkeurigheid. De subtielere taken — het onderscheiden van ccRCC van de andere RCC-types en het scheiden van papillaire van chromofobe kankers — waren moeilijker, maar het systeem behaalde nog steeds nauwkeurigheden boven de 90%. Belangrijk is dat de auteurs hun getrainde model ook testten op een geheel andere openbare dataset die elders was verzameld. De prestaties bleven hoog, wat suggereert dat de methode niet enkel één ziekenhuisbeeldreeks uit het hoofd leert maar kan generaliseren naar nieuwe patiënten en scanners.
Wat dit kan betekenen voor patiënten
Simpel gezegd laat dit onderzoek zien dat een AI-"assistent" nier-CT-scans kan uitlezen op een manier die nauw aansluit bij, en in sommige opzichten de huidige handmatige methoden overtreft bij, het scheiden van ongevaarlijke en gevaarlijke tumoren en het identificeren van belangrijke kankersubtypen. Als verdere validatie volgt, zou zo’n systeem radiologen kunnen helpen onnodige biopsieën en operaties bij goedaardige tumoren te vermijden, terwijl het meer vertrouwen geeft bij vroege behandelbeslissingen voor agressieve kankers. Voor patiënten kan dat betekenen: minder invasieve procedures, snellere antwoorden en meer gepersonaliseerde zorg op basis van de precieze aard van hun niertumor.
Bronvermelding: Abdeltawab, H., Alksas, A., Ghazal, M. et al. A deep learning ensemble framework for multi-subtype renal tumor classification using contrast-enhanced CT. Sci Rep 16, 6657 (2026). https://doi.org/10.1038/s41598-026-37283-7
Trefwoorden: nierkanker, beeldvorming van niertumoren, deep learning, CT-scan, computerondersteunde diagnose