Clear Sky Science · nl
Geïntegreerde analyse van globale regulatoren en effluxgenen geassocieerd met het terugdraaien van antimicrobiële resistentie in multiresistente Klebsiella pneumoniae
Waarom deze ziekenhuiskiemen zo moeilijk te doden zijn
In ziekenhuizen wereldwijd zijn bepaalde stammen van de bacterie Klebsiella pneumoniae berucht omdat ze moeilijk te behandelen zijn. Ze negeren meerdere antibiotica die vroeger betrouwbaar werkten en veranderen routinematige infecties in levensbedreigende situaties. Deze studie kijkt onder de microbiële motorkap om een belangrijke truc te begrijpen die deze bacteriën gebruiken: microscopische pompen die antibiotica weer uit de cel gooien, en de genetische schakelaars die die pompen lijken op of neer te regelen.
Superbugs en hun moleculaire vluchtroutes
Multiresistente Klebsiella pneumoniae wordt nu in veel ziekenhuizen aangetroffen, waaronder het Iraakse medisch centrum waar dit onderzoek werd uitgevoerd. Deze bacteriën kunnen meerdere belangrijke antibioticagroepen tegelijk overleven, zoals fluoroquinolonen, aminoglycosiden en derde generatie cefalosporinen. Een manier waarop ze dit doen is door krachtige "effluxpompen" in hun celomhulsel te installeren. Een van de belangrijkste systemen is AcrAB‑TolC, dat de bacteriële membranen overspant en werkt als een kleine dompelpomp: het grijpt antibioticamoleculen binnen in de cel en duwt ze weer naar buiten voordat de middelen ernstige schade kunnen aanrichten. Wanneer deze pompen sterk actief zijn, stijgt de antibioticaconcentratie binnen de bacterie nooit hoog genoeg om dodelijk te zijn.
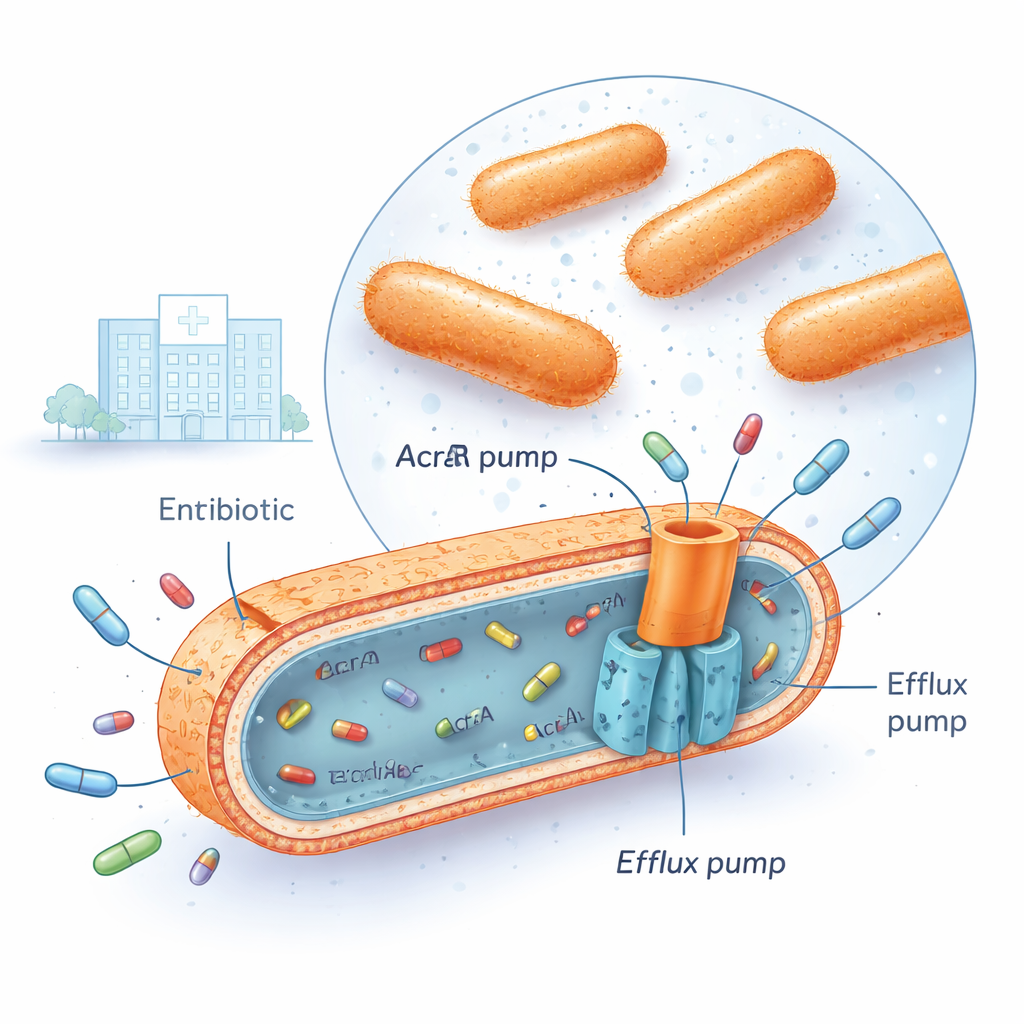
Genenschakelaars die samen met pompoverspanning optreden
De onderzoekers verzamelden 30 multiresistente klinische isolaten van Klebsiella pneumoniae en vergeleken die met 10 antibioticagevoelige isolaten en een standaard referentiestam. Met een techniek genaamd kwantitatieve real‑time PCR maten ze hoeveel bepaalde genen aan stonden. Ze concentreerden zich op drie "globale regulatoren"—genen met de namen marA, soxS en rob—samen met de drie onderdelen van de AcrAB‑TolC‑pomp zelf (acrA, acrB en tolC). In de resistente stammen waren twee regulatoren, marA en soxS, typisch vier- tot vijfvoudig hoger uitgedrukt vergeleken met gevoelige bacteriën, terwijl acrB, een centraal pompcomponent, bijna acht keer zo hoog was. Statistische analyse toonde aan dat wanneer marA en soxS hoog waren, acrB meestal ook hoog was, en die stammen neigden veel hogere doses fluoroquinolonantibiotica zoals ciprofloxacine te weerstaan. Een derde regulator, rob, veranderde weinig en correleerde niet met pompactiviteit, wat suggereert dat die een kleinere rol speelt onder de geteste omstandigheden.
De pompen uitschakelen om resistentie te verzwakken
Het vinden dat pomp‑ en regulatorgenen samen actief zijn is veelzeggend maar niet voldoende om te bewijzen dat ze daadwerkelijk de resistentie aansturen. Om te testen of de pompen functioneel belangrijk waren, gebruikte het team een chemisch hulpmiddel genaamd PAβN. Deze verbinding wordt niet als geneesmiddel bij patiënten gebruikt, maar in het laboratorium kan het AcrAB‑TolC‑achtige pompen blokkeren en voorkomen dat ze antibiotica uitwerpen. De onderzoekers kozen tien resistente isolaten met bijzonder hoge expressie van het acrB-gen en maten hoeveel ciprofloxacine nodig was om hun groei te remmen, met en zonder PAβN. In acht van deze tien stammen verlaagde het blokkeren van de pomp de vereiste ciprofloxacinedosis minstens viermaal, en soms tot zestienmaal. Deze daling toont aan dat actieve effluxpompen in veel van deze superbugs inderdaad een belangrijke reden zijn waarom ze hoge antibiotica doses kunnen verdragen.
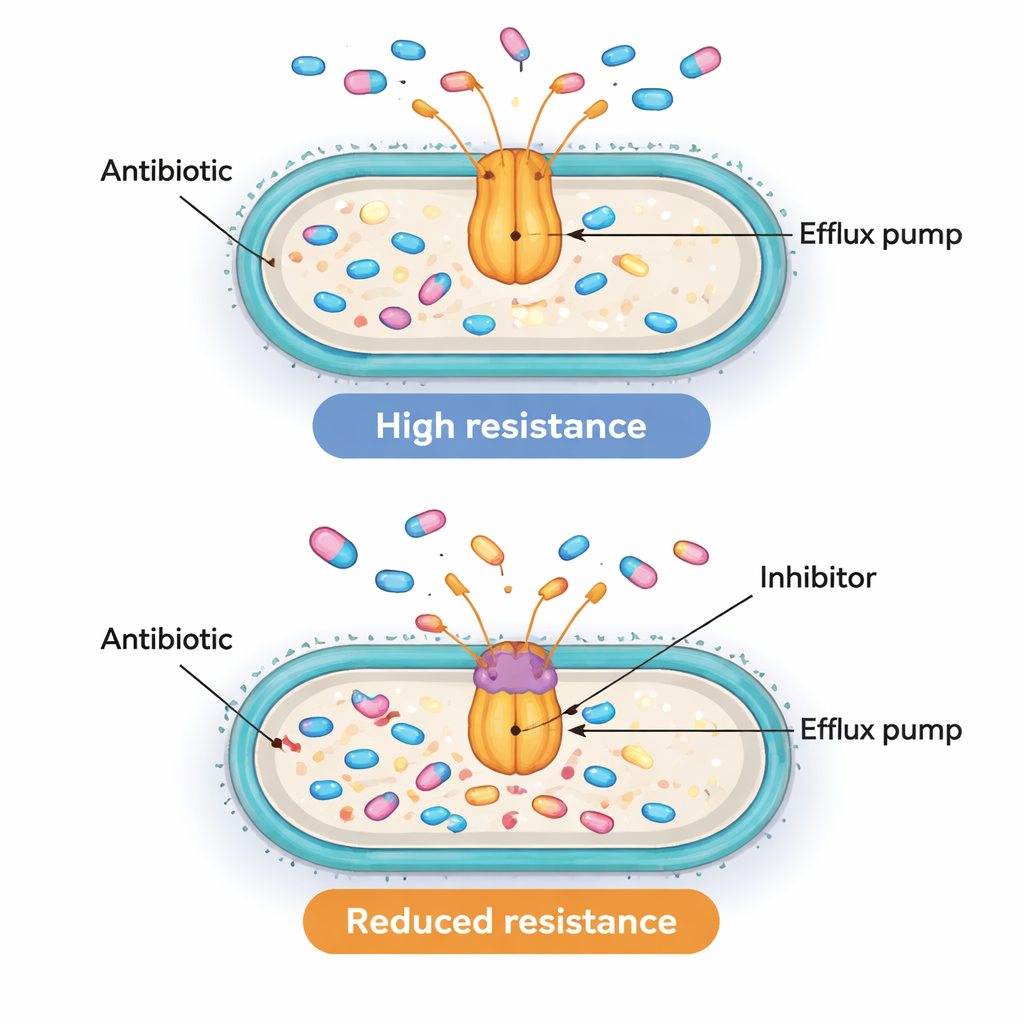
Een complex resistentie‑puzzel met veelbelovende doelwitten
Niet elke stam gedroeg zich hetzelfde. Sommige bacteriën met sterk geëxprimeerde pompgenen herkregen slechts gedeeltelijk gevoeligheid toen de pompen werden geblokkeerd, wat impliceert dat andere resistentieroutes—zoals veranderingen aan het doelwit van het antibioticum binnen de cel, productie van enzymen die medicijnen afbreken, of alternatieve pompen—ook bijdragen. Gentamicine, een aminoglycoside‑antibioticum, bijvoorbeeld, bleef grotendeels onaangetast door de patronen die gezien werden in de marA/soxS en AcrAB‑TolC‑genen, wat benadrukt dat multiresistentie meestal is opgebouwd uit meerdere overlappende verdedigingsmechanismen in plaats van één enkel mechanisme.
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat sommige ziekenhuisbacteriën antibiotica niet alleen kunnen blokkeren of afbreken, maar ze actief naar buiten gooien. Deze studie koppelt een hogere activiteit van twee genische "schakelaars", MarA en SoxS, aan actievere effluxpompen en sterkere resistentie tegen een veelgebruikte klasse antibiotica. Wanneer de pompen experimenteel worden geblokkeerd, worden veel van deze bacteriën ten minste gedeeltelijk weer gevoelig. Hoewel het werk nog niet exact aantoont hoe deze schakelaars de pompen regelen, benadrukt het zowel de regulatoren als de pompen als aantrekkelijke doelwitten. Op de lange termijn zou het combineren van conventionele antibiotica met veilige pompblokkers—of geneesmiddelen die deze globale regulatoren naar beneden bijstellen—kunnen helpen de bruikbaarheid van bestaande behandelingen te herstellen tegen anderszins ontmoedigende multiresistente infecties.
Bronvermelding: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Trefwoorden: antibioticaresistentie, effluxpompen, Klebsiella pneumoniae, fluoroquinolonen, weerstandsreversie