Clear Sky Science · nl
Downregulatie van het deubiquitinerende enzym USP10 correleert met neuronale apoptose bij HTLV-1-geassocieerde myelopathie
Waarom dit van belang is voor mensen met virale zenuwaandoeningen
Sommige virussen veroorzaken niet alleen kortdurende infecties; ze kunnen het zenuwstelsel jarenlang stilletjes beschadigen. Human T‑cell leukemia virus type 1 (HTLV‑1) is zo’n virus en kan leiden tot een chronische aandoening van het ruggenmerg die bekendstaat als HTLV‑1‑geassocieerde myelopathie (HAM). Mensen met HAM verliezen geleidelijk kracht en controle in hun benen, naast problemen met de blaas en het gevoel. Deze studie stelt een eenvoudige maar cruciale vraag: waarom gaan de zenuwcellen in het ruggenmerg bij deze aandoening dood, en kan één beschermend molecuul helpen verklaren wie het beter of slechter vergaat?
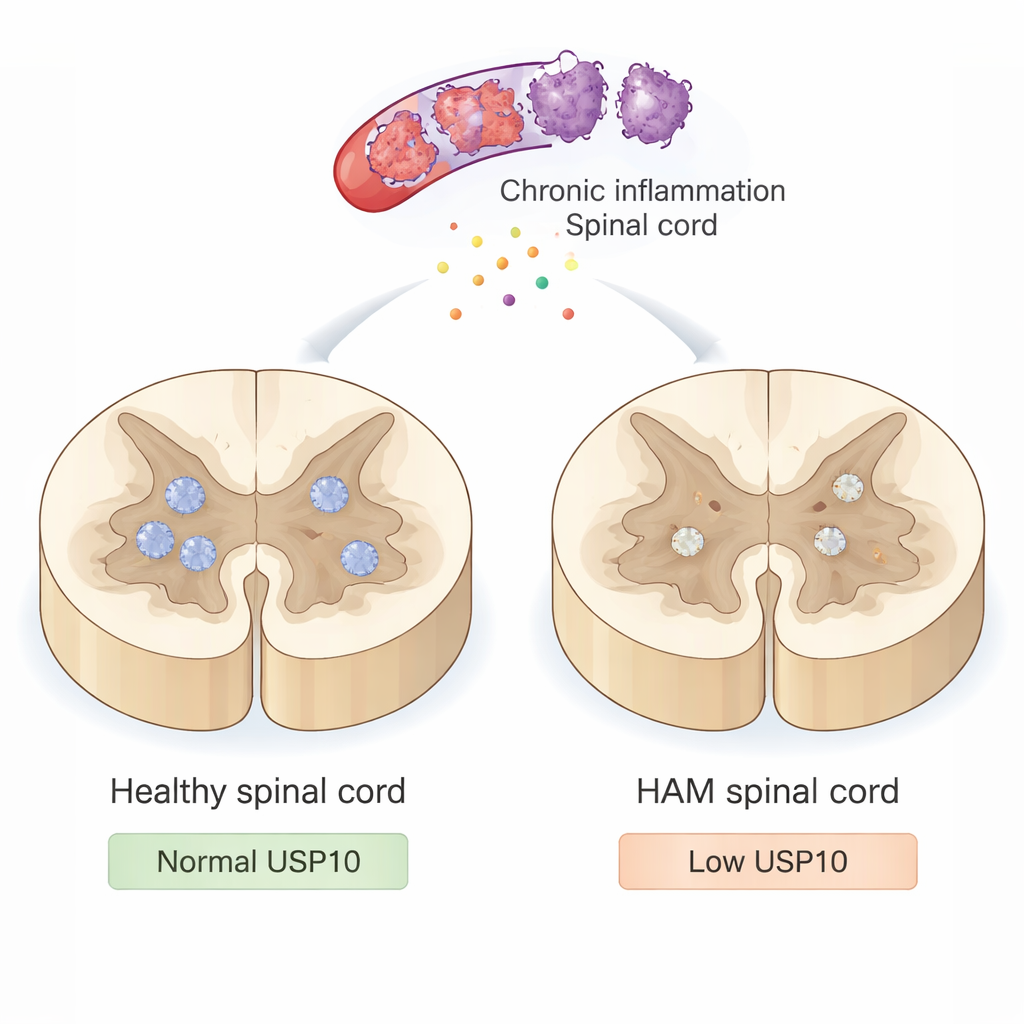
Een langzaam aanhoudende aanval op het ruggenmerg
HAM wordt niet veroorzaakt doordat het virus rechtstreeks zenuwcellen infecteert. In plaats daarvan infecteert HTLV‑1 immuuncellen die het ruggenmerg binnendringen en langdurige ontsteking uitlokken. Deze overactieve immuuncellen geven toxische stoffen en ontstekingssignalen af die, hoewel bedoeld om de infectie te beheersen, ook naburige neuronen en hun isolerende myeline beschadigen. In de loop van de tijd leidt deze smeulende aanval tot stijve, zwakke benen en moeilijkheden met lopen. Toch begrijpen artsen nog niet volledig waarom sommige neuronen bezwijken onder deze ontstekingsomgeving terwijl andere decennialang overleven.
Een cellulair "opruim"-enzym onder verdenking
De onderzoekers concentreerden zich op een eiwit genaamd USP10, een enzym dat helpt het eiwitkwaliteitscontrolesysteem van de cel te beheren en waarvan bekend is dat het cellulaire stress en geprogrammeerde celdood (apoptose) beperkt. USP10 is actief in veel weefsels, waaronder de hersenen en het ruggenmerg, en eerder werk bij de ziekte van Parkinson, beroerte en andere aandoeningen suggereert dat het neuronen helpt bestand te zijn tegen oxidatieve en inflammatoire schade. Met ruggenmergmonsters van acht mensen die overleden aan HAM en twee neurologisch gezonde controles gebruikte het team kleuringstechnieken om te zien waar USP10 aanwezig was en hoe sterk het in zenuwcellen tot expressie kwam.
Minder USP10, meer stervende neuronen
In gezonde ruggenmergen was USP10 duidelijk zichtbaar in veel neuronen. In de meeste HAM‑gevallen was de USP10‑kleuring in neuronen echter duidelijk verminderd en bij één patiënt was het vrijwel afwezig. De wetenschappers zochten vervolgens naar kenmerken van apoptose met twee methoden: een TUNEL‑test die gefragmenteerd DNA detecteert en kleuring voor actieve caspase‑3, een eiwit dat vroeg betrokken is bij celdood. Bij de controles toonden vrijwel geen neuronen deze doodssignalen. Daarentegen waren bij HAM‑patiënten een groot deel van de neuronen TUNEL‑positief en velen toonden actieve caspase‑3. Belangrijk is dat monsters met lagere USP10‑expressie geneigd waren meer apoptotische neuronen en minder overlevende neuronen te hebben, gemarkeerd door NeuN, een standaard neuronale marker. Eén opvallende patiënt met HAM die na 22 jaar nog met slechts een wandelstok liep, vertoonde sterke USP10‑expressie en relatief behouden aantallen neuronen, wat suggereert dat hogere USP10 mogelijk helpt beschermen tegen ernstige invaliditeit.
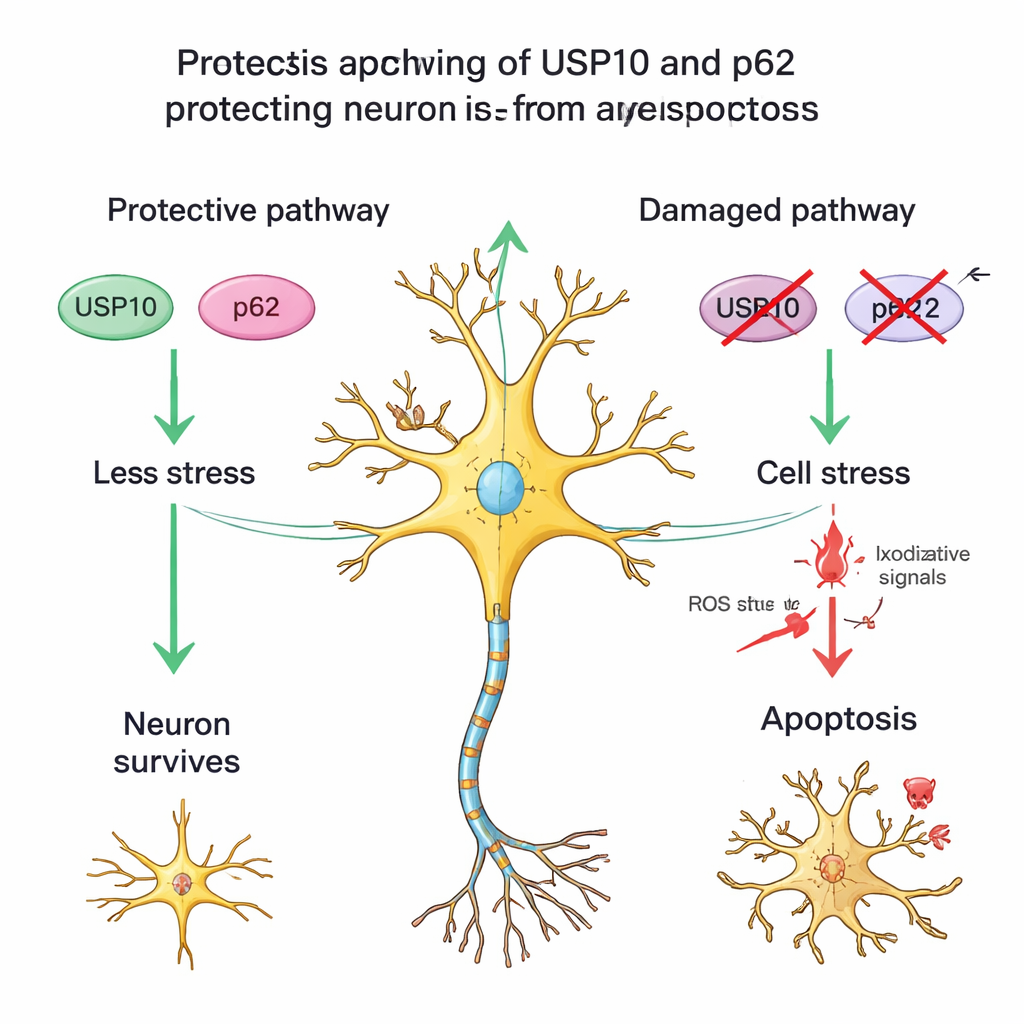
Een partner‑eiwit en gestreste maar overlevende cellen
Het team onderzocht ook een ander eiwit, p62, dat samenwerkt met USP10 bij het verwerken van beschadigde eiwitten en het reguleren van stress‑ en overlevingsroutes. In gezonde ruggenmergen was de p62‑kleuring matig; onder HAM‑patiënten hadden degenen met lage USP10 vaak ook zwakkere p62‑kleuring en minder overlevende neuronen. Dit patroon ondersteunt het idee van een USP10–p62‑samenwerking die neuronen helpt chronische ontsteking te doorstaan. De onderzoekers merkten bovendien veel neuronen in HAM‑weefsel op die de typische vorm van zenuwcellen behielden maar NeuN‑kleuring hadden verloren, een teken dat ook bij andere hersenletsels wordt gezien wanneer neuronen onder zware stress staan maar nog niet volledig dood zijn. Dit suggereert dat bij HAM sommige neuronen niet alleen volledig verloren gaan maar dat anderen in een beschadigde, kwetsbare staat blijven, mogelijk omdat USP10‑gerelateerde verdedigingsmechanismen verzwakt zijn.
Wat dit zou kunnen betekenen voor diagnose en behandeling in de toekomst
Deze studie bewijst niet dat verlies van USP10 direct neuronale dood veroorzaakt, omdat ze is gebaseerd op een klein aantal autopsiemonsters en geen veranderingen in de tijd kan volgen. Toch wijzen de consistente verbanden tussen lage USP10, verminderde p62, meer tekenen van apoptose en minder overlevende neuronen op een gemeenschappelijk pad dat chronische ontsteking en langzame neuronale degeneratie bij HAM zou kunnen verbinden. Voor patiënten roept dit een bemoedigende mogelijkheid op: het meten of versterken van USP10‑gerelateerde routes in het ruggenmerg — of mogelijk in toegankelijkere monsters zoals hersenvocht — zou op een dag kunnen helpen degenen met een hoger risico op snelle progressie te identificeren, monitoring te sturen of nieuwe behandelingen te inspireren die de eigen stressbeschermingssystemen van cellen versterken bij door virussen geïnduceerde neuro‑inflammatoire ziekten.
Bronvermelding: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Trefwoorden: HTLV-1-geassocieerde myelopathie, neuroinflammatie, neurale apoptose, USP10, degeneratie van het ruggenmerg