Clear Sky Science · nl
Antibacteriële werking en cytotoxiciteit van tricalciumsilicaat‑gebaseerde cementen met verschillende antibacteriële toevoegingen
Waarom dit belangrijk is voor uw volgende vulling
Bij een diepe cariës proberen tandartsen tegenwoordig zo veel mogelijk natuurlijk tandweefsel te behouden in plaats van alles weg te boren. Dat betekent vaak dat er een dunne laag verweekt, bacteriën bevattend dentine onder de vulling achterblijft. Deze studie stelt een eenvoudige maar cruciale vraag: kunnen we een veelgebruikt tandreparatiecement verbeteren zodat het stilletjes resterende microben doodt zonder de levende cellen in de tand te schaden?
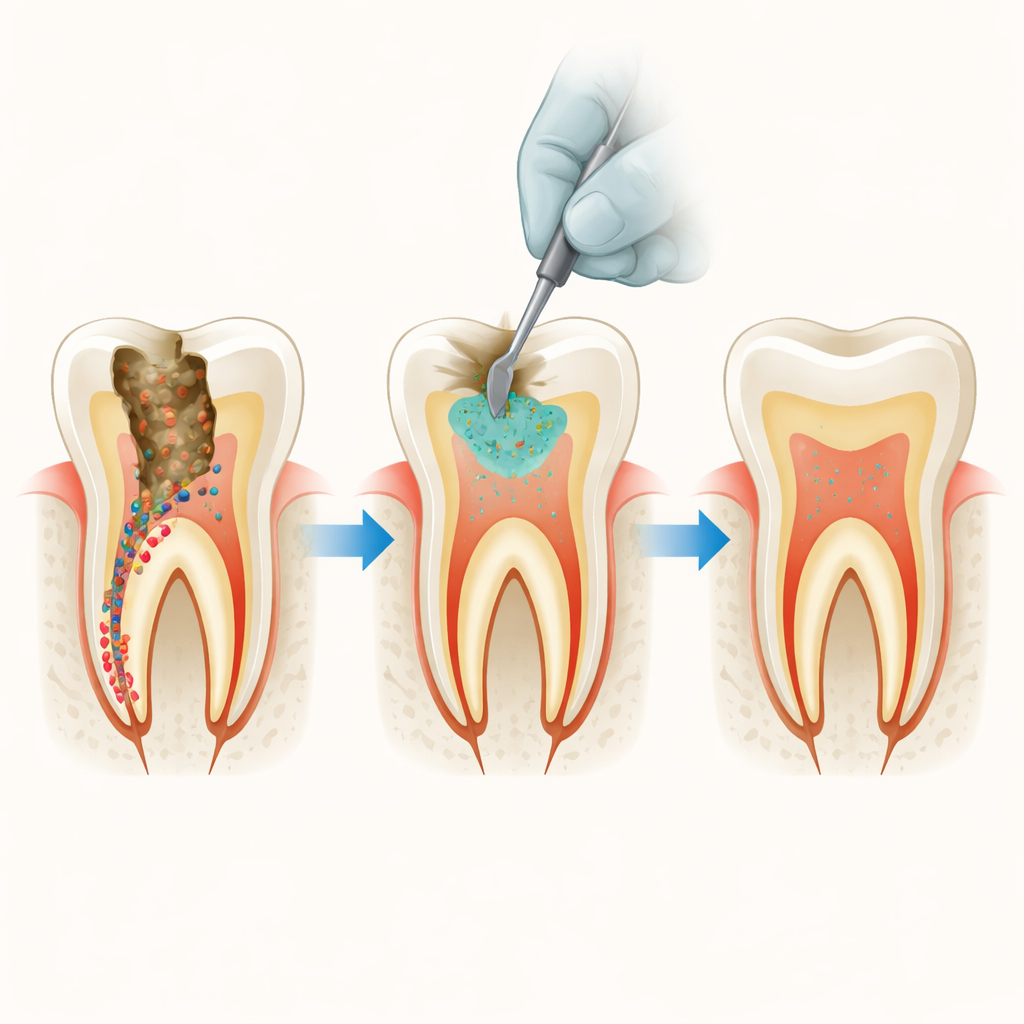
Diepe cariës en verborgen microben
Moderne 'minimaal boren'-technieken hebben als doel om het zachte binnenste van de tand, de pulpa, niet bloot te leggen door dentine achter te laten dat zich weer kan verharden. Het nadeel is dat sommige cariësveroorzakende bacteriën, zoals Streptococcus mutans en soorten Lactobacillus, in die laag kunnen blijven zitten. Na verloop van tijd kunnen deze bacteriën nieuwe achterliggende schade veroorzaken onder een ogenschijnlijk gezonde vulling. Tricalciumsilicaat‑gebaseerde cementen zijn populair voor het dichten van diepe caviteiten omdat ze helpen bij het heropbouwen van mineralen en een goede barrière vormen, maar op zichzelf zijn ze niet erg effectief tegen bacteriën.
Van een veelgebruikt cement een kiemdoder maken
De onderzoekers namen dit bekende cement en mengden er vijf verschillende antibacteriële toevoegingen in verschillende concentraties doorheen. Twee waren organische verbindingen die vaak in desinfectiemiddelen voorkomen (benzalkoniumchloride en cetrimide), en drie waren anorganische stoffen die in tandheelkundige producten of materialen worden gebruikt (titaniumdioxide, zinkoxide en tinfluoride). Ze persden deze mengsels in kleine schijfjes en plaatsten die op platen bedekt met vijf bacteriesoorten die verband houden met tandbederf en orale infecties. Door de heldere kringen rond elk schijfje te meten waar bacteriën niet konden groeien, konden ze zien hoe sterk elk recept bacteriën weghield.
De balans vinden tussen microben doden en cellen sparen
Aangezien een materiaal dat bacteriën doodt maar ook tandcellen vergiftigt in de mond nutteloos zou zijn, testte het team ook hoe de meest veelbelovende toevoegingen levende cellen beïnvloedden. Ze stelden twee menselijke celtypen bloot — fibroblasten, die veelvoorkomende steunende cellen zijn, en tandpulpa‑stamcellen, die bij het herstel van tandweefsel helpen — aan de cementen op indirecte wijze. Een kleurveranderingstest mat hoeveel cellen actief bleven, en speciale fluorescente kleurstoffen toonden levende (groene) en dode (rode) cellen onder de microscoop. Deze opzet beeldde de werkelijke situatie in een diepe caviteit na, waarbij het cement door een dunne dentinelaag van de pulpa gescheiden is en stoffen afgeeft die naar de cellen diffunderen.
Wat het beste werkte en wat te hard was
De resultaten toonden aan dat het type en de hoeveelheid toevoeging veel uitmaakten. Benzalkoniumchloride gaf het sterkste en breedste antibacteriële effect, met grote kiemvrije zones tegen alle geteste soorten, vooral de Lactobacillus‑stammen die vaak in diepe cariës voorkomen. Cetrimide hielp ook, maar had over het algemeen hogere concentraties nodig om de prestatie van benzalkonium te benaderen. De drie anorganische middelen verbeterden het antibacteriële effect van het cement alleen bij de hogere gedoteerde doses, en zelfs dan voornamelijk tegen bepaalde bacteriën zoals S. mutans en Actinomyces. Wat betreft veiligheid was het basiscement op zichzelf vriendelijk voor beide celtypen en leek het zelfs de gezondheid van fibroblasten te ondersteunen. Toevoeging van benzalkoniumchloride bleef onschadelijk voor fibroblasten tot ongeveer 1%, werd licht schadelijk bij 2–4%, en duidelijk schadelijk bij 7%. Tandpulpa‑stamcellen waren over het algemeen gevoeliger: zowel benzalkoniumchloride als cetrimide verminderden hun overleving, waarbij cetrimide vanaf 2% matig toxisch werd.
Wat dit kan betekenen voor toekomstige tandheelkundige zorg
Samengevoegd wijzen de bevindingen op één bijzonder veelbelovend recept: tricalciumsilicaat‑gebaseerd cement met 1% benzalkoniumchloride. Op dit niveau onderdrukte het materiaal schadelijke bacteriën sterk terwijl het fibroblasten volledig in leven hield en tandpulpa‑stamcellen grotendeels levensvatbaar liet. In gewone bewoordingen suggereert dit dat toekomstige diepe vullingen gemaakt zouden kunnen worden van een cement dat stilletjes resten van microben onder het oppervlak bestrijdt, terwijl het nog steeds zacht genoeg is voor het levende weefsel in de tand. Er is meer onderzoek nodig — vooral onder complexe, realistische mondomstandigheden — maar deze uitgebalanceerde samenstelling zou kunnen helpen tandartsen beter te beschermen bij tanden die volgens minimaal invasieve technieken behandeld zijn.
Bronvermelding: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Trefwoorden: diepe tandbederf, antibacterieel tandcement, tricalciumsilicaat, benzalkoniumchloride, biocompatibiliteit van pulpacellen