Clear Sky Science · nl
Beelden van intercellulaire biomoleculen met fluorescente proteïne-indicatoren met lipide-PEG-ankers
Cellen live zien communiceren
Onze hersenen en lichamen vertrouwen op een constante chemische conversatie tussen cellen. Ionen en neurotransmitters dragen boodschappen over kleine spleten, maar deze snelle, vluchtige signalen zijn moeilijk te zien zonder ze te verstoren. Deze studie introduceert een eenvoudige manier om levende cellen te "beschilderen" met gloeiende sensoren die zich aan hun buitenoppervlak hechten, waardoor wetenschappers deze boodschappen — met name kaliumionen en de neurotransmitter glutamaat — in realtime en met detail kunnen volgen. 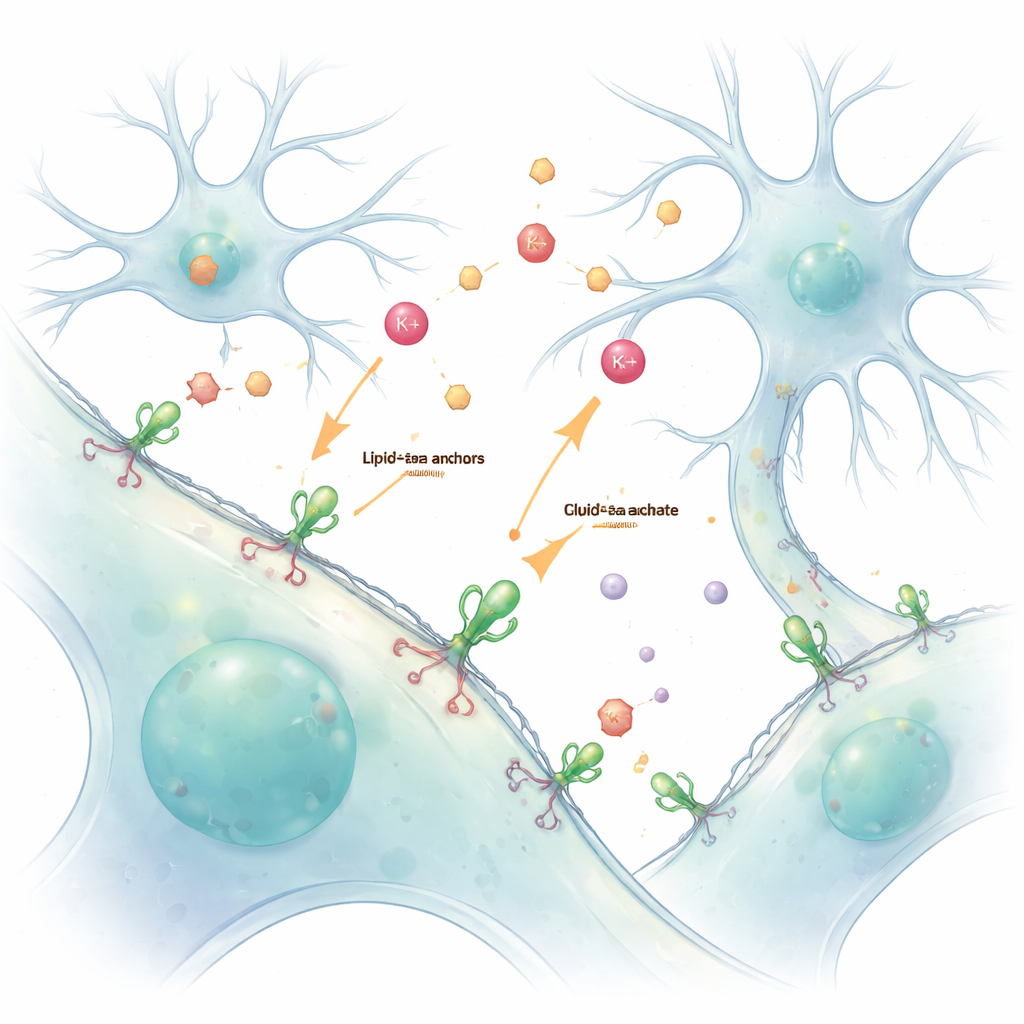
Een nieuwe manier om het celoppervlak te labelen
Traditioneel laten onderzoekers cellen fluorescente proteïnesensoren maken via genetische manipulatie. Hoewel krachtig, plaatst deze genetische aanpak de sensoren vaak binnenin de cel, waardoor het lastig is om onderscheid te maken tussen wat binnen en buiten gebeurt. De auteurs losten dit op met een chemische handgreep genaamd een lipide–PEG-anker. Het ene uiteinde van dit molecuul nestelt zich in het buitenmembraan, terwijl het andere uiteinde chemisch aan een fluorescerend proteïnesensor is gekoppeld. Wanneer deze voorbereide sensoren aan levende cellen worden toegevoegd, bedekken ze spontaan het buitenoppervlak en vormen ze een stabiele, gloeiende laag die rapporteert wat er in het omgevende vocht gebeurt.
Kalium en glutamaat zichtbaar maken
Het team paste twee bestaande fluorescente indicatoren aan: GINKO2, dat reageert op kaliumionen, en R-iGluSnFR1, dat reageert op glutamaat. Ze zuiverden deze proteïnen uit bacteriën en bevestigden vervolgens de lipide–PEG-ankers. In gekweekte humane cellen vormde de geankerde kaliumsensor een duidelijke rand langs het celoppervlak en werd helderder wanneer extracellulair kalium toenam, om daarna weer te dimmen wanneer de concentratie daalde. Belangrijk was dat de lichtgevende eigenschappen en gevoeligheid sterk overeenkwamen met de originele, ongewijzigde sensor in reageerbuisexperimenten, wat aantoonde dat verankering de prestatie niet aantastte. Hetzelfde gold voor de glutamaatsensor, die na verankering responsief bleef en glutamaat duidelijk markeerde in de ruimte net buiten de cellen.
Neuronen beluisteren in kweek en in plakjes
De onderzoekers gingen vervolgens over op zenuwcellen uit de hippocampus van muizen, een hersengebied dat belangrijk is voor leren en geheugen. Ze bedekten deze neuronen met de lipide–PEG-geankerde glutamaatsensor en vulden tegelijkertijd het inwendige van dezelfde cellen met een aparte calciummarker die elektrische activiteit rapporteert. Met total internal reflection-microscopie konden ze rode flitsen van glutamaat aan het celoppervlak zien terwijl groene signalen binnenin de cellen vuurgebeurtenissen aangaven. Deze tweekleurige weergave toonde aan dat de geankerde sensoren spontane neurotransmitterafgifte konden volgen zonder enige genetische modificatie van de neuronen zelf.
Chemische golven in hersenweefsel in kaart brengen
Vervolgens testte het team de methode in acute hersenplakjes, die de natuurlijke bedrading van de hippocampus behouden. Ze brachten de geankerde kaliumsensor aan op plakjes en stimuleerden zenuwvezels elektrisch. De geankerde sensor gaf duidelijke, herhaalbare fluorescentietoenames na elke stimulus, terwijl niet-geankerde sensoren snel weg diffundeerden en zwakke, onstabiele signalen gaven. Door de plakjes te baden in oplossingen met bekende kaliumconcentraties en rekening te houden met de zwakke eigen gloed van het weefsel, bouwden de auteurs een kalibratiecurve en schatten de werkelijke extracellulaire kaliumconcentraties. Basale niveaus lagen rond 2,5 millimolair en stegen tot ongeveer 3,4 millimolair bij bescheiden stimulatie, in lijn met klassieke elektrodemetingen. Geankerde sensoren voor zowel kalium als glutamaat toonden hoe deze signalen zich verschillend verspreiden: veranderingen in glutamaat bleven dicht bij actieve synapsen, terwijl kaliumstijgingen zich honderden micrometers uitstrekten, wat wijst op bredere effecten op netwerkexcitabiliteit. 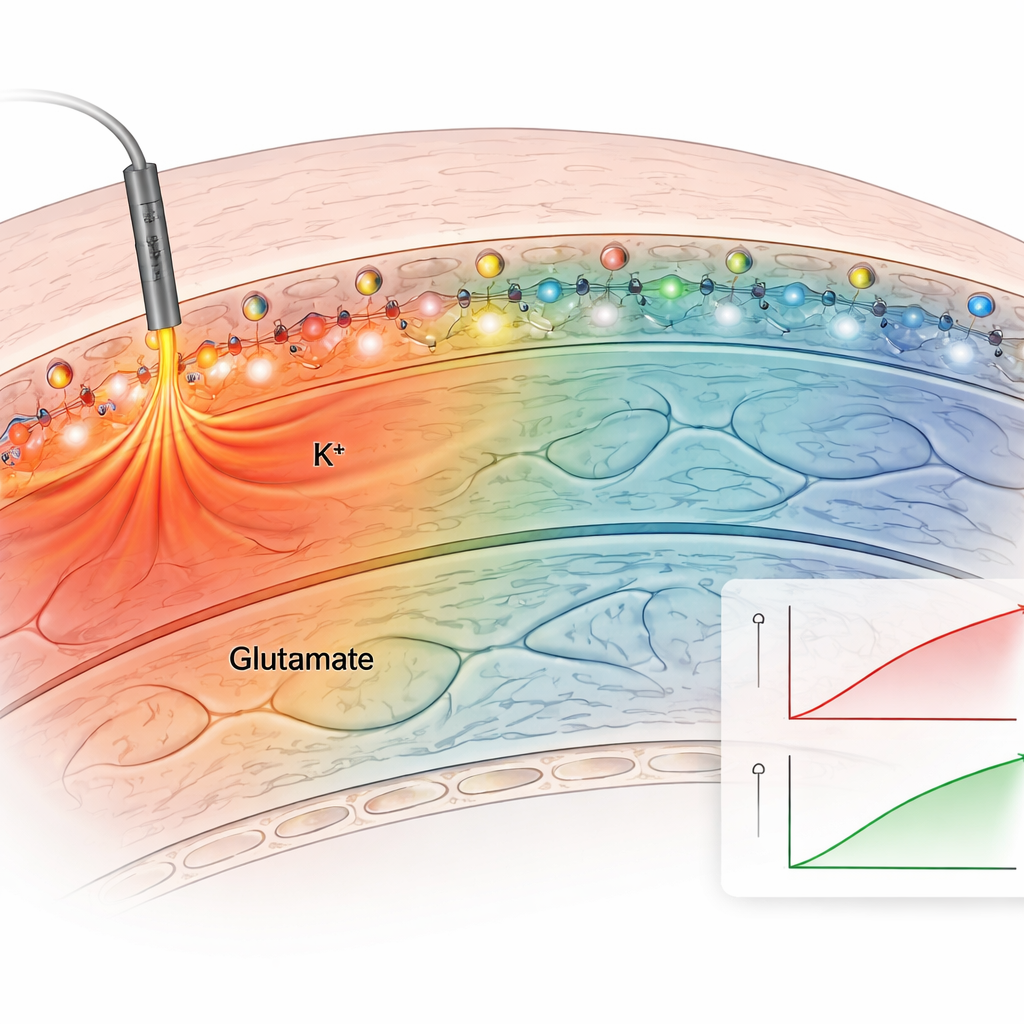
Onderzoeken hoe de hersenen signalen genereren en opruimen
Aangezien de sensoren op het celoppervlak vastzitten, konden de auteurs ontleden welke processen deze extracellulaire golven vormen. Het blokkeren van glutamaattransporters, die normaal glutamaat opruimen, zorgde ervoor dat de geankerde glutamaatsensor grotere en langduriger signalen liet zien, wat bevestigt dat lokale opname de verspreiding van glutamaat beperkt. Het blokkeren van AMPA-type glutamaatreceptoren verminderde zowel elektrische responsen als kaliumsignalen, wat aangeeft dat het merendeel van de kaliumstijging afkomstig is van postsynaptische neuronen die door synaptische input worden geactiveerd. Het blokkeren van natriumkanalen met tetrodotoxine maakte de kaliumveranderingen bijna volledig onzichtbaar, waarmee ze direct aan actiepotentialen werden gekoppeld. Gezamenlijk laten deze experimenten zien hoe geankerde sensoren complexe, verspreide chemie kunnen omzetten in intuïtieve films en kaarten.
Waarom dit belangrijk is voor toekomstig hersenonderzoek
Voor niet-specialisten is de kernboodschap dat dit werk een snelle, niet-genetische manier biedt om levende cellen en weefsels te bedekken met zeer gevoelige moleculaire rapporteurs. In plaats van elke celtype opnieuw te herprogrammeren, kunnen onderzoekers kant-en-klare sensorproteïnen van buitenaf toevoegen en onmiddellijk visualiseren hoe ionen en neurotransmitters in realtime aan het celoppervlak veranderen. Deze aanpak verbetert controle, reproduceerbaarheid en ruimtelijke precisie en vermijdt de uitdagingen van genafgifte, vooral in kwetsbare bereidingen zoals acute hersenplakjes. Naarmate meer fluorescente indicatoren voor verschillende chemicaliën worden ontwikkeld, kan dezelfde lipide–PEG-verankeringsstrategie uitgroeien tot een veelgebruikt gereedschapskistje om de chemische taal van cellen door het hele lichaam te observeren.
Bronvermelding: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Trefwoorden: extracellulaire signalering, fluorescente biosensoren, glutamaatbeeldvorming, kaliumdynamiek, hippocampale neuronen