Clear Sky Science · nl
Classificatie van Alzheimerstadia op basis van MRI-neuroimaging met een deep neural network met convolutional block attention module en GAN-stijl ruisinjectie
Waarom vroegtijdige hersenscans ertoe doen
De ziekte van Alzheimer berooft langzaam het geheugen en de zelfstandigheid, vaak lang voordat symptomen duidelijk zijn. Families, artsen en patiënten willen allemaal een manier om de ziekte vroeg te signaleren, wanneer behandelingen en aanpassingen in levensstijl het meest effect kunnen hebben. Deze studie beschrijft een nieuw computersysteem dat routinematige hersenscans leest en mensen met opvallende nauwkeurigheid in vier stadia van Alzheimer-gerelateerde geheugenverlies kan indelen, wat clinici potentieel een snellere, goedkopere en consistenter tweede opinie kan bieden.
Een nadere blik in de hersenen
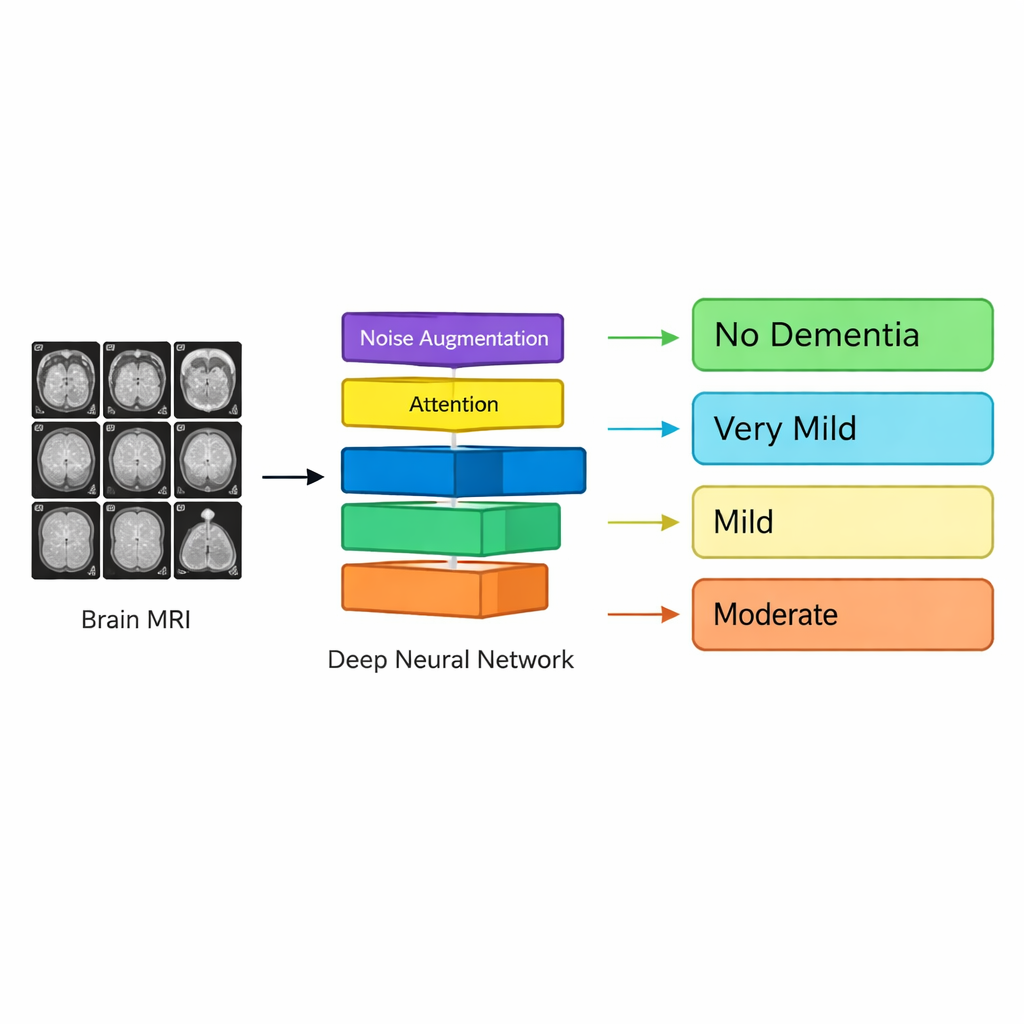
De onderzoekers richten zich op MRI-scans, die gedetailleerde beelden van de hersenstructuur tonen zonder operatie of radioactiviteit. Ze gebruiken gegevens uit een groot internationaal project genaamd het Alzheimer’s Disease Neuroimaging Initiative (ADNI), waarbij vrijwilligers tussen 55 en 90 jaar regelmatig geheugentests en beeldvorming ondergaan. Uit deze scans haalt het team 2D-snedes van de hersenen en verdeelt die in vier groepen: mensen zonder dementie en mensen met zeer milde, milde of matige dementie. Dit weerspiegelt hoe Alzheimer zich doorgaans ontwikkelt in de praktijk, waar kleine veranderingen in geheugen en denken geleidelijk verslechteren.
Een computer leren subtiele veranderingen te zien
In plaats van menselijke experts te vragen hersengebieden en kenmerken handmatig te selecteren, trainen de auteurs een deep-learningsysteem—vergelijkbaar met systemen voor gezichtsherkenning of zelfrijdende auto’s—om rechtstreeks van de beelden te leren. Hun model, Neuro_CBAM-ADNet genoemd, is een type convolutioneel neuraal netwerk dat uitstekend is in het herkennen van patronen in afbeeldingen. Terwijl de MRI-afbeelding door het netwerk stroomt, wordt deze verwerkt door opeenvolgende lagen die randen, texturen en complexere vormen detecteren totdat het systeem patronen kan onderscheiden die correleren met verschillende dementiestadia, waarvan veel te subtiel zijn voor het blote oog.
Het systeem helpen zich te concentreren op wat belangrijk is
Een belangrijke innovatie is een ’attention’-mechanisme dat het netwerk zachtjes aanspoort zich te concentreren op de meest informatieve delen van de scan. In praktische termen leert het model welke locaties en interne kenmerken van de hersenen neigen te veranderen naarmate Alzheimer vordert—zoals gebieden die met geheugen en denken te maken hebben—terwijl minder relevante achtergrond wordt genegeerd. De onderzoekers pakken ook een veelvoorkomend probleem in medische data aan: sommige ziektefasen zijn veel zeldzamer dan andere, zodat het model anders naar de meerderheidsgroep kan neigen. Om dit tegen te gaan genereren ze extra trainingsbeelden voor ondervertegenwoordigde groepen door gecontroleerd ruis toe te voegen aan bestaande scans, waardoor de natuurlijke variabiliteit bij echte patiënten wordt nagebootst zonder de onderliggende anatomie te vervormen.
Het systeem op de proef stellen
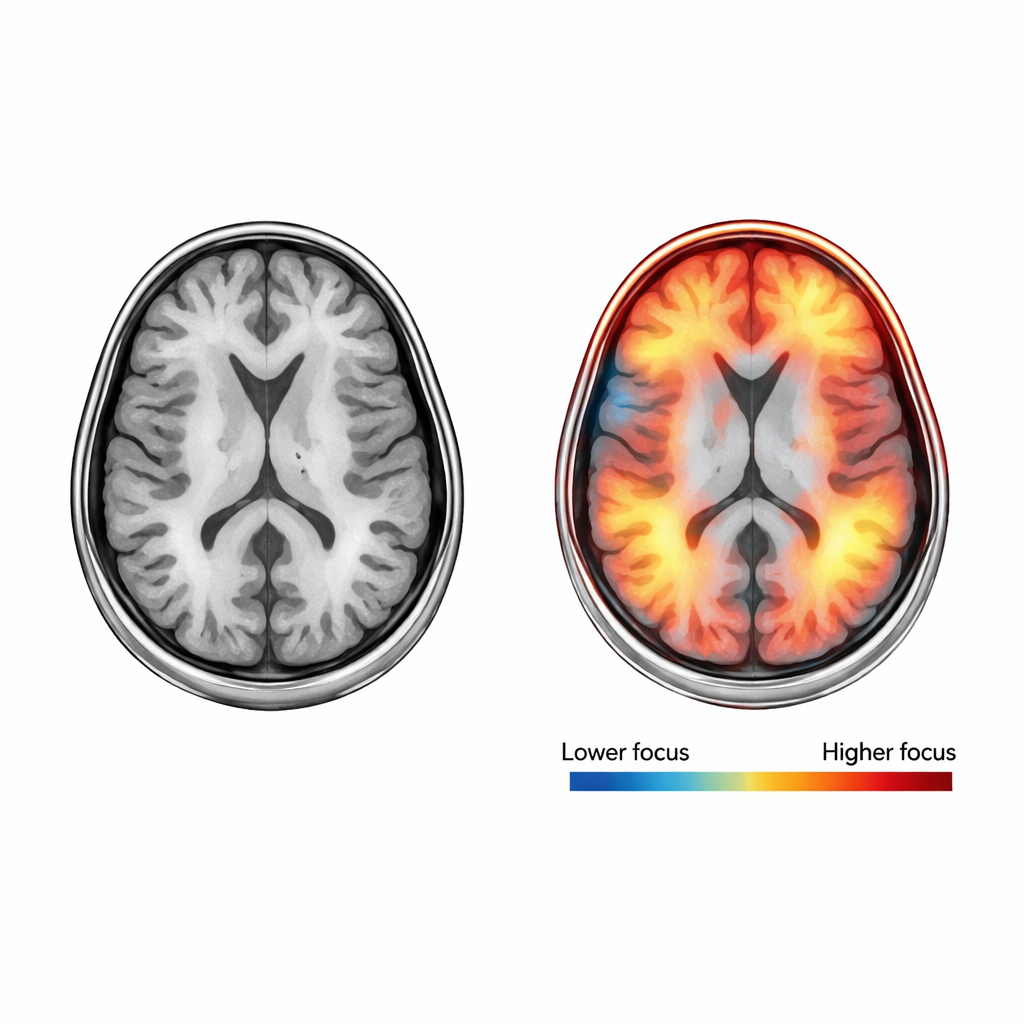
Om te controleren hoe betrouwbaar hun systeem is, trainen en testen de onderzoekers het herhaaldelijk op verschillende deelverzamelingen van de data, een proces dat cross-validatie wordt genoemd. Over vijf onafhankelijke rondes classificeert Neuro_CBAM-ADNet het dementiestadium correct in ongeveer 98 procent van de gevallen, met vergelijkbaar hoge scores voor sensitiviteit (aangetaste gevallen herkennen), precisie (vals alarm vermijden) en een gecombineerde maat genaamd F1-score. Het systeem is bijzonder sterk in het onderscheiden van duidelijk verschillende groepen, zoals matige dementie versus geen dementie, en de meeste fouten doen zich voor tussen aangrenzende stadia zoals geen dementie en zeer milde dementie, waar zelfs specialisten het vaak oneens zijn. Extra hulpmiddelen genaamd Grad-CAM heatmaps laten zien waar in de hersenen het model ’kijkt’ wanneer het een beslissing neemt, en bieden visuele aanwijzingen die vergeleken kunnen worden met bekende ziektekenmerken.
Wat dit betekent voor patiënten en artsen
In eenvoudige bewoordingen toont dit werk aan dat een goed ontworpen AI-systeem hersenscans kan lezen en mensen in vier stadia van Alzheimer-gerelateerde achteruitgang kan indelen met een consistentie die eerdere benaderingen evenaart en in sommige gevallen overtreft. Het wijst ook naar de hersengebieden die de beslissingen sturen, wat het vertrouwen van clinici kan vergroten. Hoewel het hulpmiddel nog bredere tests nodig heeft in verschillende ziekenhuizen en met verschillende scanners, suggereert het een toekomst waarin routinematige MRI-onderzoeken, gecombineerd met transparante AI, vroege hersenveranderingen kunnen signaleren, meer zelfverzekerde diagnoses kunnen ondersteunen en behandelbeslissingen kunnen sturen voordat de ziekte te ver gevorderd is.
Bronvermelding: Kumar, S., Shastri, S., Mansotra, V. et al. MRI neuroimaging-based Alzheimer’s disease stage classification using deep neural network with convolutional block attention module and GAN-style noise injection. Sci Rep 16, 6946 (2026). https://doi.org/10.1038/s41598-026-37226-2
Trefwoorden: Ziekte van Alzheimer, hersen-MRI, deep learning, vroegtijdige diagnose, medische beeldvorming AI