Clear Sky Science · nl
Dynamische graafconvolutie met uitgebreide snoei en GNN-classificatie voor precieze detectie van lymfeknoopmetastasen
Waarom kleine veranderingen in lymfeklieren ertoe doen
Wanneer borstkanker zich verspreidt, is de eerste halte vaak de lymfeklieren, kleine filters langs het drainagesysteem van het lichaam. Vaststellen of kankercellen deze knopen hebben bereikt is een van de belangrijkste aanwijzingen die artsen gebruiken bij de keuze van chirurgie, chemotherapie en bestraling. Toch kunnen zelfs ervaren pathologen zeer kleine groepjes kankercellen op digitale microscoopbeelden over het hoofd zien, vooral wanneer ze bijna niet van gezond weefsel te onderscheiden zijn. Deze studie introduceert een nieuw kunstmatig-intelligentie-kader dat weefsel als een netwerk van verbonden gebieden behandelt, waardoor het subtiele tekenen van verspreiding met opmerkelijke nauwkeurigheid kan opsporen.
Weefselbeelden omzetten in netwerken
De onderzoekers werken met enorme digitale preparaten van gekleurd weefsel, zogenaamde whole-slide images, afkomstig van lymfeknoopbiopten bij borstkankerpatiënten. Deze beelden bevatten miljoenen pixels en een verwarrende mix van celtypen, kleuren en texturen. Om deze complexiteit te beheersen, maakt het team de beelden eerst schoon: ze normaliseren helderheid en kleur, verminderen ruis en maken aangevulde kopieën door patches te roteren en te spiegelen, zodat de computer leert omgaan met natuurlijke variatie. Elk beeldpatch wordt vervolgens opgesplitst in kleine, redelijk uniforme regio's ("superpixels"), die de punten—of knopen—in een graaf vormen, terwijl de relaties tussen aangrenzende regio's de verbindende lijnen—of randen—vormen. Dit netwerkperspectief behoudt de onregelmatige vormen en layouts van echt weefsel beter dan traditionele rastergebaseerde beeldmethoden.
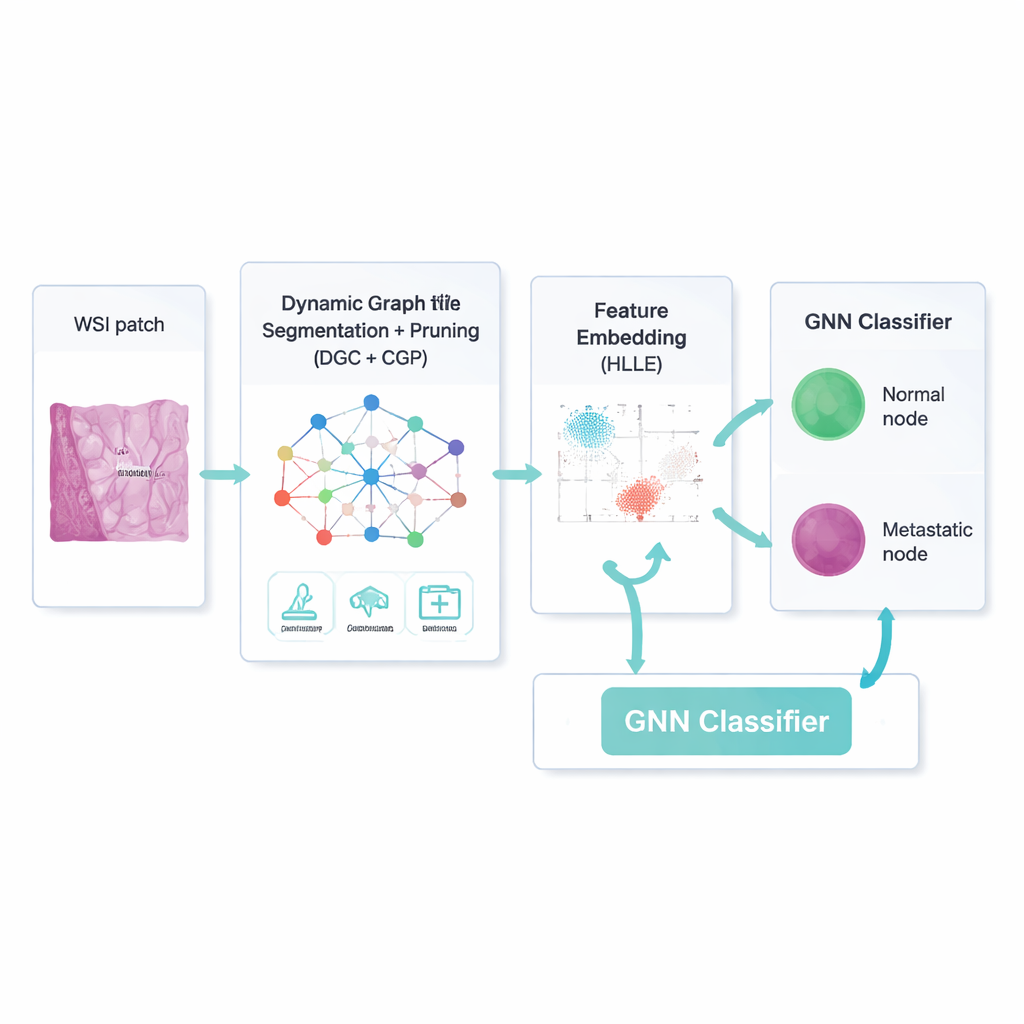
Een slimmer manier om op het belangrijke te focussen
Het is niet voldoende om alleen een netwerk te bouwen; veel verbindingen en beeldkenmerken zijn irrelevant of zelfs misleidend. Het kader gebruikt daarom een dynamische graafconvolutionele auto-encoder—een type neuraal netwerk dat zowel leert hoe elke regio eruitziet als hoe regio's elkaar beïnvloeden. Een aanvullende "attention"-mechaniek leert het model sommige beeldkanalen zwaarder te wegen dan andere, bijvoorbeeld door randen bij een tumorrand te benadrukken. Tegelijkertijd snoeit een strategie die Comprehensive Graph Gradual Pruning wordt genoemd gestaag onbruikbare onderdelen weg: zwakke verbindingen tussen regio's, minder nuttige numerieke kenmerken en modelgewichten met lage impact. Dit snoeien vindt plaats tijdens het trainen, niet erna, zodat het systeem leert meer te doen met minder en uiteindelijk zowel sneller als beter te interpreteren is.
Patronen comprimeren zonder hun vorm te verliezen
Nadat het model waarschijnlijk lymfeknoopgebieden van achtergrondweefsel heeft gescheiden, moet het elk gebied nog beschrijven op een manier die compact maar betekenisvol is. Hiervoor gebruiken de auteurs een techniek genaamd Hessian-based Locally Linear Embedding. In eenvoudige bewoordingen perst deze methode veel numerieke kenmerken samen tot een kleinere set, terwijl geprobeerd wordt de gekromde "vorm" te behouden waarin echte voorbeelden in de feature-ruimte zijn gerangschikt—bijvoorbeeld hoe kleine metastasen verschillen van normale immuuncellen langs subtiele textuur- of kleurpatronen. Deze gecomprimeerde beschrijvingen worden de invoer voor een graafneurale-netwerkclassifier, die opnieuw werkt op het netwerk van regio's en hun opgeschoonde verbindingen en voor elke knoop beslist of deze metastatisch is of niet.
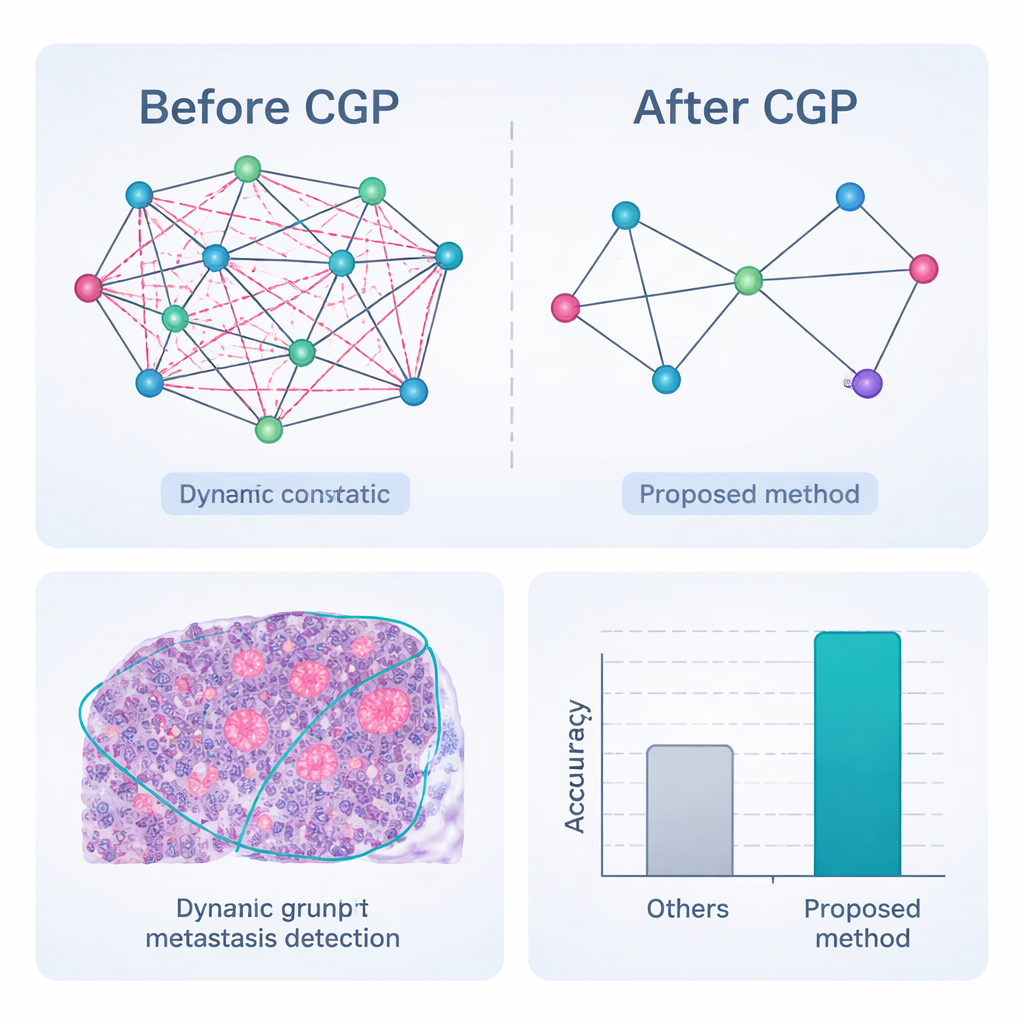
Het kader aan de tand voelen
De volledige pijplijn—voorverwerking, dynamische graafsegmentatie met snoei, feature-embedding en graafgebaseerde classificatie—werd geëvalueerd op CAMELYON17, een openbare verzameling van 1.000 deskundig geannoteerde lymfeknoopslides van borstkankerpatiënten. Vergeleken met een reeks sterke deep-learningconcurrenten, waaronder populaire convolutionele netwerken en hybride transformermodellen, behaalde de nieuwe methode de hoogste scores over bijna alle maatstaven. Het klassificeerde knopen correct als kankercellen of niet in 98,65% van de gevallen en toonde betere overeenstemming met deskundige contouren van tumorregio's, vooral bij zeer kleine of vage metastasen. Cruciaal is dat, doordat de graaf agressief wordt gesnoeid, het systeem deze resultaten bereikt met veel minder berekeningen en lager geheugenverbruik, waardoor het geschikter is voor realtimegebruik in drukke pathologielaboratoria.
Wat dit betekent voor patiënten en clinici
In gewone bewoordingen laat dit werk zien hoe het beschouwen van weefsel als een slim getrimd netwerk van verbonden regio's computers kan helpen fungeren als uiterst zorgvuldige tweede beoordelaars van lymfeknoopslides. Door aandacht en rekenkracht te richten op de meest informatieve structuren en ruis weg te gooien, is het kader beter in het opsporen van kleine zaadjes van kanker die anders gemist zouden kunnen worden, en doet het dat efficiënt genoeg om praktisch toepasbaar te zijn. Hoewel verdere klinische validatie nodig is, zouden dergelijke hulpmiddelen pathologen kunnen ondersteunen bij het nemen van snellere, consistentere beslissingen over de vraag of kanker zich heeft verspreid—informatie die direct behandelplannen en uiteindelijk de uitkomsten voor patiënten beïnvloedt.
Bronvermelding: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Trefwoorden: lymfoedeoknooppmetastasen, digitale pathologie, graafneurale netwerken, medische beeldsegmentatie, borstkanker