Clear Sky Science · nl
Structurele karakterisering van metaalbinding in menselijke tyrosylproteïne-sulfotransferase 2, TPST2
Waarom kleine metaalionen belangrijk zijn voor celsignalering
Binnen onze cellen stemmen talloze moleculaire machines geruisloos af hoe weefsels groeien, hormonen werken en immuuncellen communiceren. Een van die machines, een enzym TPST2 genoemd, voegt een klein sulfaatlabel toe aan bepaalde eiwitten terwijl ze door het verzendcentrum van de cel — het Golgi-apparaat — gaan. Deze studie onthult hoe eenvoudige metaalionen zoals natrium en mangaan TPST2 efficiënter laten werken door delen van zijn structuur subtiel te verstevigen — een inzicht dat mogelijk een verband legt tussen mineraalbalans in cellen en kanker- en hormoongerelateerde ziekten. 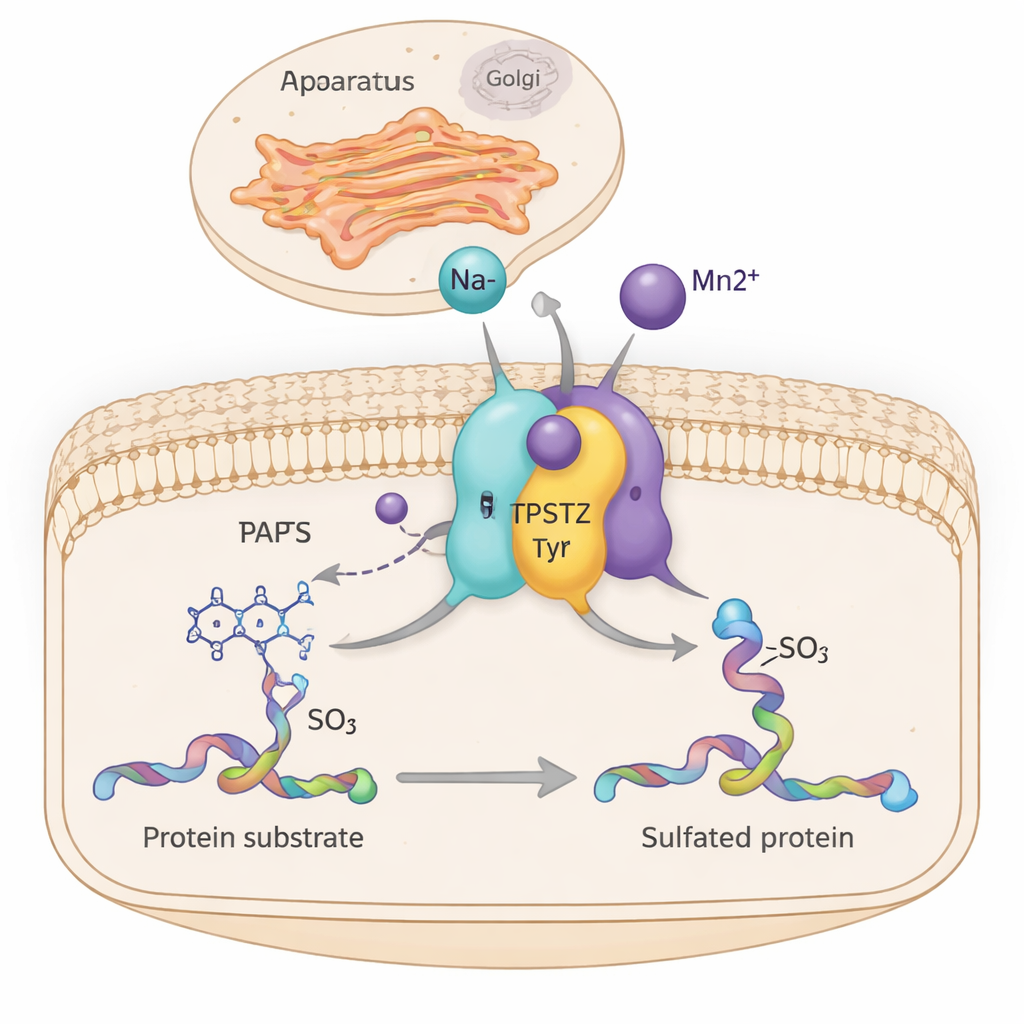
Een eiwit dat andere eiwitten siert
TPST2 behoort tot een familie van enzymen die “tyrosinesulfatering” uitvoeren, een chemische modificatie die aan specifieke tyrosine-eenheden op eiwitten wordt toegevoegd. Deze gesulfateerde eiwitten vervullen sleutelrollen buiten de cel: ze beïnvloeden bloedstolling, de beweging van witte bloedcellen, hormoon–receptorbinding en zelfs de manier waarop virussen cellen binnendringen. Bij mensen zijn er twee hoofd-enzymen voor sulfatering, TPST1 en TPST2, die in het Golgi-membraan liggen en eiwitten modificeren terwijl die worden klaargemaakt voor export. Muizenonderzoek laat zien dat het ontbreken van TPST2 de aanmaak van schildklierhormoon verstoort, de groei belemmert en mannelijke onvruchtbaarheid veroorzaakt, wat het belang voor normale fysiologie onderstreept.
Verbindingen met kanker en immuunontsnapping
Recente onderzoeken koppelen TPST2 rechtstreeks aan ziekte. Bij melanoom modificeert TPST2 een onderdeel van de interferonreceptor op een manier die immuunsignalering verzwakt, en het remmen van TPST2 vergroot het effect van immuuncheckpointtherapieën die PD-1 targeten. Bij alvleesklierkanker helpt een TPST2-afhankelijke route een eiwit (integrine β4) te stabiliseren dat tumorgroei en -uitzaaiing bevordert. Het remmen van TPST2 in deze modellen vertraagt deling en invasie van kankercellen. Omdat TPST2 inwerkt op eiwitten aan het celoppervlak, herschakelt het effectief hoe cellen hun omgeving waarnemen en erop reageren, waardoor het een aantrekkelijk doelwit is voor nieuwe therapieën.
Het vinden van de metalen "aan"-schakelaars
Biochemici wisten al lang dat TPST2 veel actiever wordt wanneer tweewaardige metalen zoals mangaan (Mn²⁺) aanwezig zijn, maar de structurele verklaring ontbrak. In deze studie brachten de auteurs de katalytische kern van menselijke TPST2 tot expressie en verkristalliseerden die samen met een reactiebijproduct en ofwel natrium (Na⁺) of mangaan. Met behulp van röntgenkristallografie met hoge resolutie ontdekten ze twee kleine metaalbindingspockets in het enzym, elk met een keurige zeszijdige (octaëdrische) rangschikking van omringende atomen. Door de röntgenwavelength af te stemmen op de unieke signatuur van verschillende metalen, bevestigden ze dat Mn²⁺ selectief deze plaatsen bezet, terwijl metalen zoals zink en koper ofwel zwak aan andere locaties binden of helemaal niet binden.
Verstevigen van belangrijke bewegende delen in plaats van het hele eiwit te herschikken
Verrassend genoeg zagen TPST2 met natrium en TPST2 met mangaan er over het algemeen vrijwel identiek uit; er was geen dramatische opening of sluiting van het eiwit. In plaats daarvan beïnvloedden de metalen voornamelijk twee flexibele regio’s vlakbij de ingang van het actieve centrum: een helix genaamd α3 en een nabije lus bekend als de α12–α13-lus. In metaalvrije of zwak gebonden toestanden wiebelen deze segmenten en zijn ze deels gedesordend. Wanneer Na⁺ bindt, worden ze meer geordend; Mn²⁺ verstevigt ze nog verder, zoals blijkt uit verminderde thermische beweging in de röntgengegevens en uit computeranalyses van flexibiliteit. Deze extra stijfheid verhoogt bescheiden de smelttemperatuur van het enzym en zou de "entropische" kost van het organiseren van het actieve centrum verlagen — waardoor het TPST2 gemakkelijker en sneller wordt gemaakt om substraten in de juiste positie voor sulfatering te leiden. 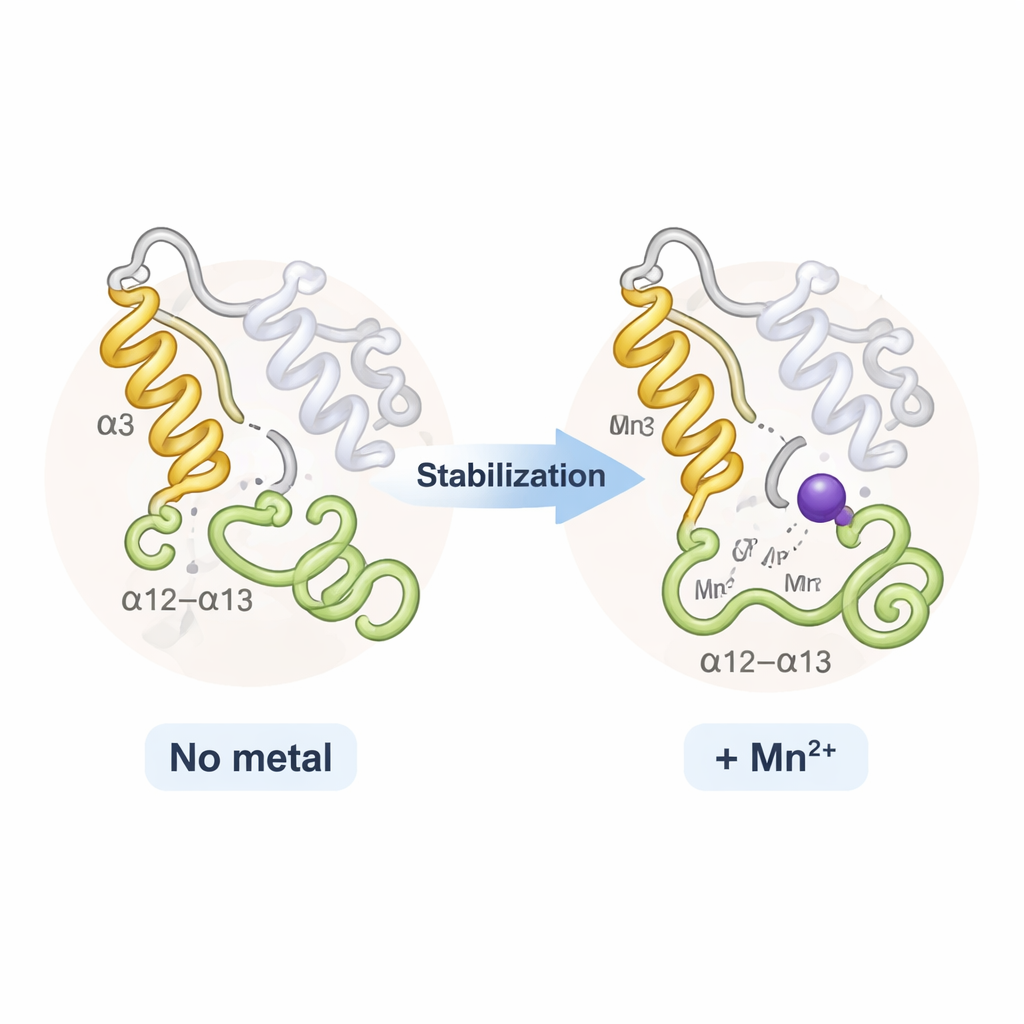
Van celmineralen naar signaalcontrole
De auteurs stellen een model voor van "activering-door-ordening." In afwezigheid van gebonden metaal is TPST2 slapper rond de ingang van het actieve centrum en werkt het inefficiënt. Natrium, overvloedig in cellen, kan aan dezelfde plaatsen binden en een deels geordende, matig actieve toestand creëren. Mangaan, aanwezig in zorgvuldig gecontroleerde micromolaire concentraties binnen het Golgi, bindt sterker en vergrendelt de sleutelregio’s in een optimaal gerangschikte toestand, waarmee de catalytische efficiëntie wordt gemaximaliseerd. Dit suggereert dat subtiele verschuivingen in Golgi-mangaanconcentraties kunnen bijsturen hoe sterk TPST2 zijn doelen modificeert. Omdat TPST2 invloed heeft op hormoonproductie en kankersignalering, benadrukt dit werk een mogelijk verband tussen metaalionbalans, eiwit"decoraties" en ziekte — en biedt het een structureel kader voor het ontwerpen van middelen die TPST2-activiteit moduleren door metaalbinding na te bootsen of te verstoren.
Bronvermelding: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Trefwoorden: tyrosinesulfatering, TPST2, mangaan, Golgi-apparaat, eiwitmodificatie