Clear Sky Science · nl
Interpreteerbaar hybride ensemble met aandacht-gebaseerde fusie en EAOO-GA optimalisatie voor longkankerdetectie
Waarom vroege opsporing van longkanker voor iedereen van belang is
Longkanker behoort tot de dodelijkste vormen van kanker, grotendeels omdat deze vaak te laat wordt ontdekt, wanneer behandelingsmogelijkheden beperkt zijn en de overlevingskansen sterk afnemen. Artsen vertrouwen steeds vaker op CT-scans en computerprogramma’s om verdachte gezwellen in de longen te vinden voordat symptomen optreden. Dit artikel presenteert een nieuw kunstmatig-intelligentiesysteem (AI) dat tot doel heeft die computergestuurde diagnosen niet alleen nauwkeuriger te maken, maar ook betrouwbaarder en begrijpelijker voor clinici.
Hoe computers longscans lezen
Moderne AI-systemen kunnen CT-beelden doorzoeken en patronen leren die een onschadelijk plekje onderscheiden van een gevaarlijke tumor. Deze systemen, opgebouwd uit diepe neurale netwerken, hebben al aangetoond dat ze in smalle taken kunnen concurreren met of zelfs betere resultaten behalen dan menselijke experts. Ze stuiten echter op drie belangrijke obstakels in echte ziekenhuizen: ze kunnen overfitten op één dataset en falen bij nieuwe patiënten, ze hebben moeite met ongebalanceerde data waarbij sommige ziekteclassificaties zeldzaam zijn, en ze functioneren vaak als ondoorzichtige “black boxes” waar clinici moeite hebben om op te vertrouwen. De auteurs richten zich op deze uitdagingen voor een veelgebruikte long-CT-dataset die drie soorten gevallen bevat: goedaardige noduli, kwaadaardige noduli en normale scans.
Veel deskundige ogen in plaats van één
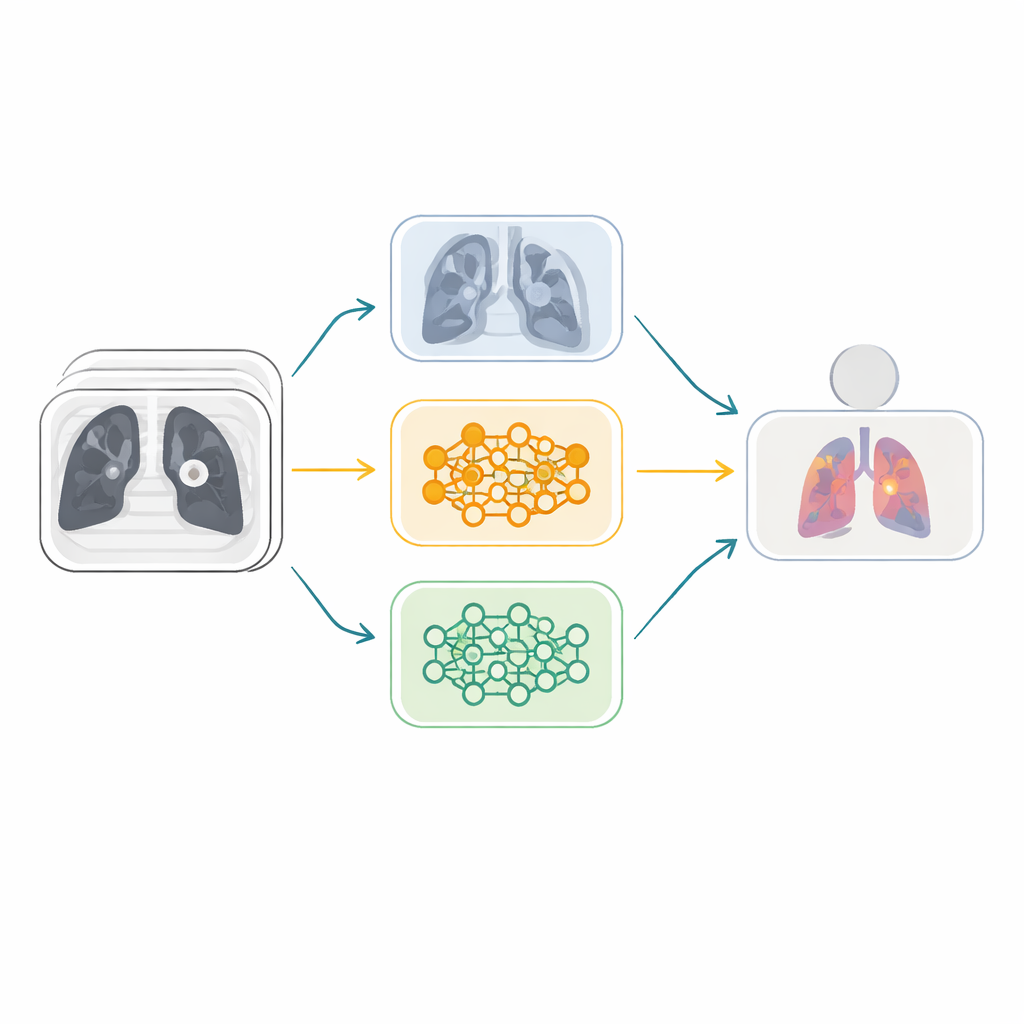
In plaats van te vertrouwen op één neuraal netwerk bouwen de onderzoekers een ensemble — een team van verschillende AI-modellen die gezamenlijk stemmen. Ze starten vanuit zes krachtige beeldherkenningsarchitecturen die oorspronkelijk op miljoenen alledaagse foto’s zijn getraind en passen deze aan voor long-CT-scans. Deze modellen worden vervolgens gekoppeld in drie “fusie”-takken, waarbij elke tak twee netwerken met elkaar combineert die elkaar aanvullen. Binnen elke tak leert een speciaal aandachtmechanisme, bekend als Squeeze-and-Excitation, welke interne feature-kanalen de meest bruikbare visuele aanwijzingen dragen — zoals subtiele texturen of knobbels — en versterkt die terwijl minder informatieve patronen worden verzwakt. Dit helpt het systeem te focussen op medisch relevante details in plaats van ruis.
De natuur als zoeker om het team af te stemmen
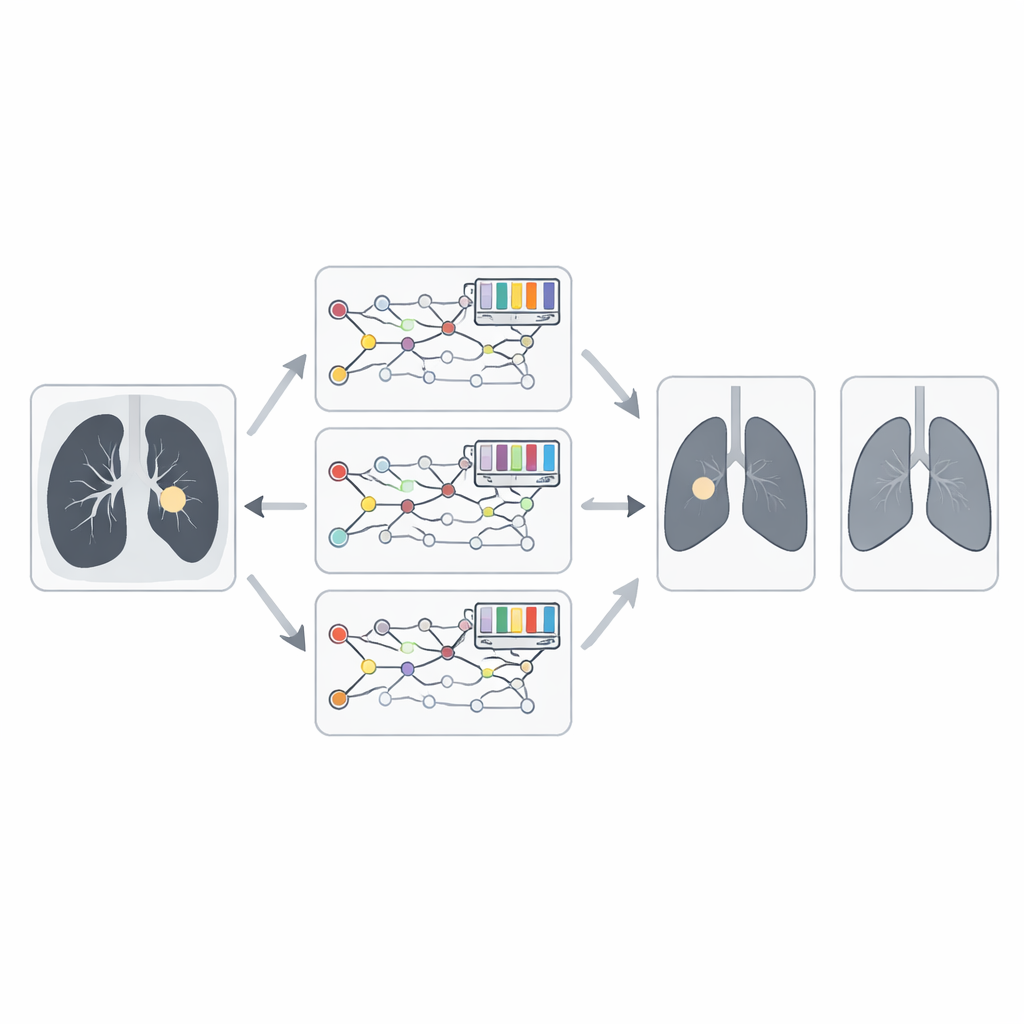
Gewoon de meningen van drie sterke takken gemiddeld samenvoegen laat nog ruimte voor verbetering. Het kernidee in dit werk is om een natuur-geïnspireerde optimizer te laten bepalen hoeveel gewicht elke tak krijgt. Het team introduceert een verbeterde versie van het Animated Oat Optimization-algoritme, uitgebreid met genetische bewerkingen zoals crossover en mutatie. Simpel gezegd beschouwt dit algoritme kandidaat-gewichtscombinaties als een populatie en laat ze herhaaldelijk “evolueren”, waarbij combinaties die tot nauwkeurigere kankerpredicties leiden behouden blijven en de rest wordt herschikt. Na veel iteraties ontdekt het een effectieve balans waarin de meest betrouwbare fusiemodellen zwaarder bijdragen aan de uiteindelijke diagnose.
Balanceren van zeldzame gevallen en de black box openen
Reële medische data bevatten vaak veel meer kwaadaardige dan goedaardige of normale voorbeelden, wat een AI-systeem kan bevoordelen om te snel kanker vast te stellen. Om dit tegen te werken gebruiken de auteurs een techniek genaamd SMOTE om aanvullende synthetische voorbeelden te genereren voor ondervertegenwoordigde klassen, waarmee de trainingsverdeling wordt uitgebalanceerd. Ze voegen ook een verklaringslaag toe met Grad-CAM, die heatmaps produceert die de beeldregio’s tonen die de beslissing het sterkst beïnvloedden. Bij kwaadaardige gevallen vallen de gemarkeerde gebieden doorgaans samen met onregelmatige, gespeticuleerde noduli; bij goedaardige of normale scans verschuift de focus naar gladdere weefsels. Dit helpt radiologen te verifiëren dat het model naar de juiste structuren kijkt in plaats van naar irrelevante artefacten.
Hoe goed het systeem presteert op data uit de praktijk
Getest op de IQ-OTH/NCCD longkanker-dataset behaalt het voorgestelde ensemble een indrukwekkende nauwkeurigheid van ongeveer 99,4 procent, met vergelijkbaar hoge precisie, recall en F1-score. Het overtreft consequent elk individueel netwerk, eenvoudigere fusiemethoden en een reeks andere optimalisatiemethoden. Cruciaal is dat de auteurs het model ook valideren op een aparte, veelgebruikte CT-verzameling bekend als LIDC-IDRI, waar het bijna 98 procent nauwkeurigheid behoudt. Deze externe test suggereert dat het systeem generaliseert buiten de beelden waarop het oorspronkelijk is getraind, een belangrijke vereiste voor elk hulpmiddel dat clinici in verschillende ziekenhuizen en scannerinstellingen moet bijstaan.
Wat dit betekent voor patiënten en clinici
Voor leken is de belangrijkste conclusie dat het combineren van meerdere AI-“experts”, het zorgvuldig afstemmen van hun samenwerking en het transparanter maken van hun redeneerlijnen de vroege opsporing van longkanker uit CT-scans aanzienlijk kan verbeteren. Het in dit artikel beschreven raamwerk zet ruwe beelden om in een zeer nauwkeurige, relatief interpreteerbare second opinion voor radiologen. Indien verder gevalideerd in klinische proeven en aangepast aan dagelijkse ziekenhuisworkflows, zouden dergelijke systemen kunnen helpen gevaarlijke tumoren eerder op te sporen, onnodige vervolgonderzoeken verminderen en uiteindelijk de overleving en kwaliteit van leven verbeteren voor mensen met een verhoogd risico op longkanker.
Bronvermelding: Al Duhayyim, M., Aldawsari, M.A., Ismail, A. et al. Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection. Sci Rep 16, 8159 (2026). https://doi.org/10.1038/s41598-026-37187-6
Trefwoorden: longkanker detectie, CT-scan analyse, deep learning ensemble, medische beeld-AI, uitlegbare diagnostiek