Clear Sky Science · nl
Integratieve machine learning en moleculaire docking onthullen dat narirutin ABCC1/ABCG2 richt voor hermodellering van het immuunmicro‑milieu bij colorectale kanker
Vruchtverbinding met grote kankerdromen
Colorectale kanker behoort tot de dodelijkste vormen van kanker wereldwijd, en veel patiënten krijgen nog steeds zware behandelingen te verduren en lopen tegen medicijnresistentie aan. Deze studie onderzoekt narirutin, een natuurlijke stof die in citrusvruchten voorkomt, om te bepalen of het lichaam kolon‑tumoren op een zachtere manier kan helpen bestrijden — door te veranderen hoe kankercellen omgaan met geneesmiddelen en hoe immuuncellen zich rondom de tumor gedragen.
Van citrusvrucht naar kankertarget
De onderzoekers begonnen met een eenvoudige vraag: als narirutin een medicijn zou zijn, aan welke onderdelen van onze cellen zou het zich hechten? Met grote openbare kankerdatabanken en computer‑voorspellingsinstrumenten scanden ze duizenden genen uit colorectale tumoren en gezond weefsel. Vervolgens overlappen ze deze kanker‑gekoppelde genen met diegenen waarop narirutin waarschijnlijk effect heeft. Van meer dan 3.000 afwijkende genen in colorectale kanker werd voorspeld dat narirutin betekenisvolle interacties heeft met slechts negen, en in het bijzonder met vijf ‘hub’‑genen die op sleutelposities binnen tumorcellen zitten.
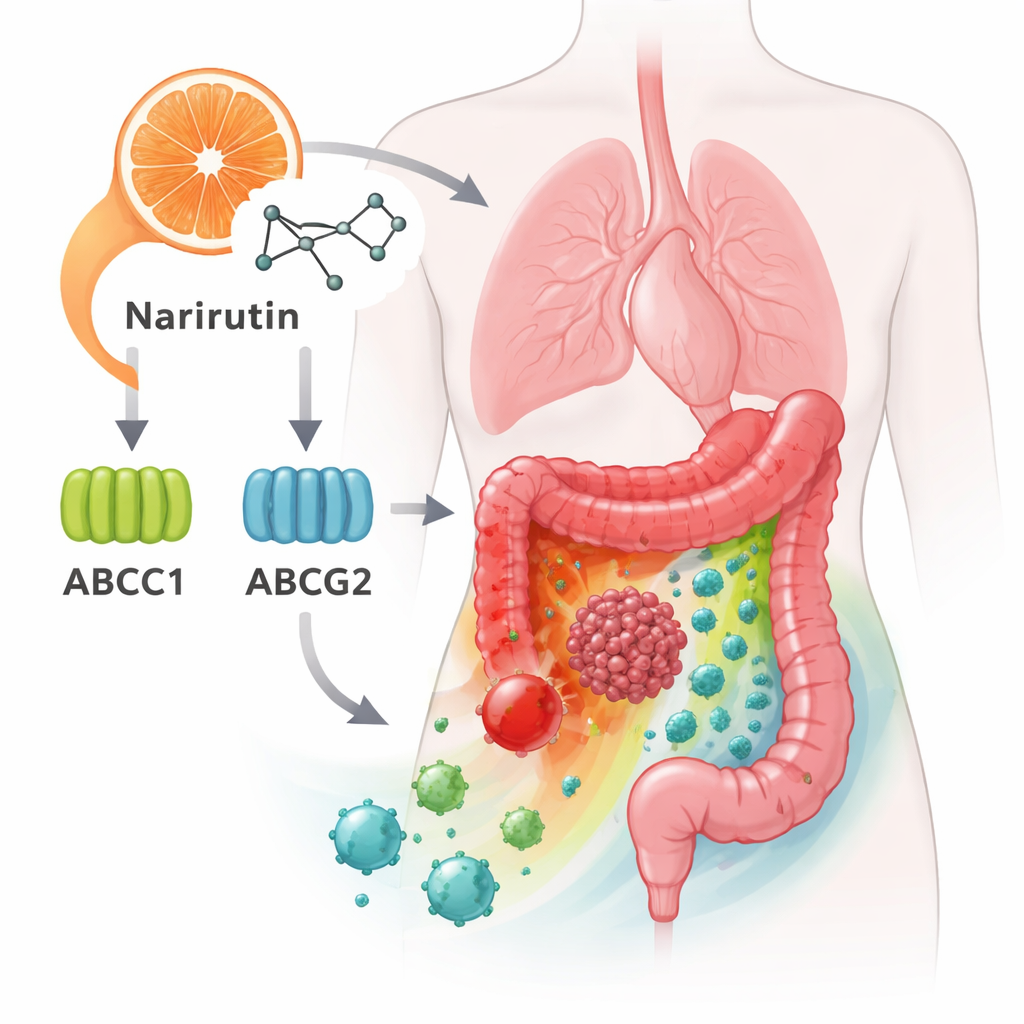
Belangrijke poortwachters op het oppervlak van kankercellen
Onder deze hub‑genen staken er twee bovenuit: ABCC1 en ABCG2. Zij coderen voor pompachtige eiwitten die in het buitenmembraan van cellen zitten en geneesmiddelen naar buiten pompen — een van de redenen dat sommige kankers resistent worden tegen chemotherapie. De nieuwe analyse suggereert dat narirutin aan deze pompen kan binden en mogelijk hun werking beïnvloedt. Andere hub‑genen, waaronder CA12, EPHX2 en PTGS1, zijn betrokken bij de regulatie van zuurgraad, vetstofwisseling en ontstekingssignalen. Samen bepalen deze genen mede of een tumor zich ongecontroleerd ontwikkelt, hoe hij op medicijnen reageert en hoe hij interacteert met het omringende normale weefsel.
Gesimuleerde binding en uitkomsten in de echte wereld
Om te toetsen of narirutin daadwerkelijk aan deze doelwit‑eiwitten zou kunnen binden, gebruikte het team moleculaire docking — hoogresolutie computermodellen die voorspellen hoe een klein molecuul past in een groter eiwit. Deze simulaties toonden aan dat narirutin goed in de bindingsgroeven van de doelwit‑eiwitten past en stabiele contacten vormt, wat de fysieke plausibiliteit van binding ondersteunt. Bij bestudering van patiëntengegevens bleek dat de hub‑genen duidelijk tumorweefsel onderscheiden van normaal weefsel en gekoppeld zijn aan overleving. Zo gingen hogere niveaus van ABCC1 en PTGS1 bijvoorbeeld vaak samen met slechtere uitkomsten, wat suggereert dat het onderdrukken van deze genen — mogelijk met verbindingen als narirutin — gunstig kan zijn.
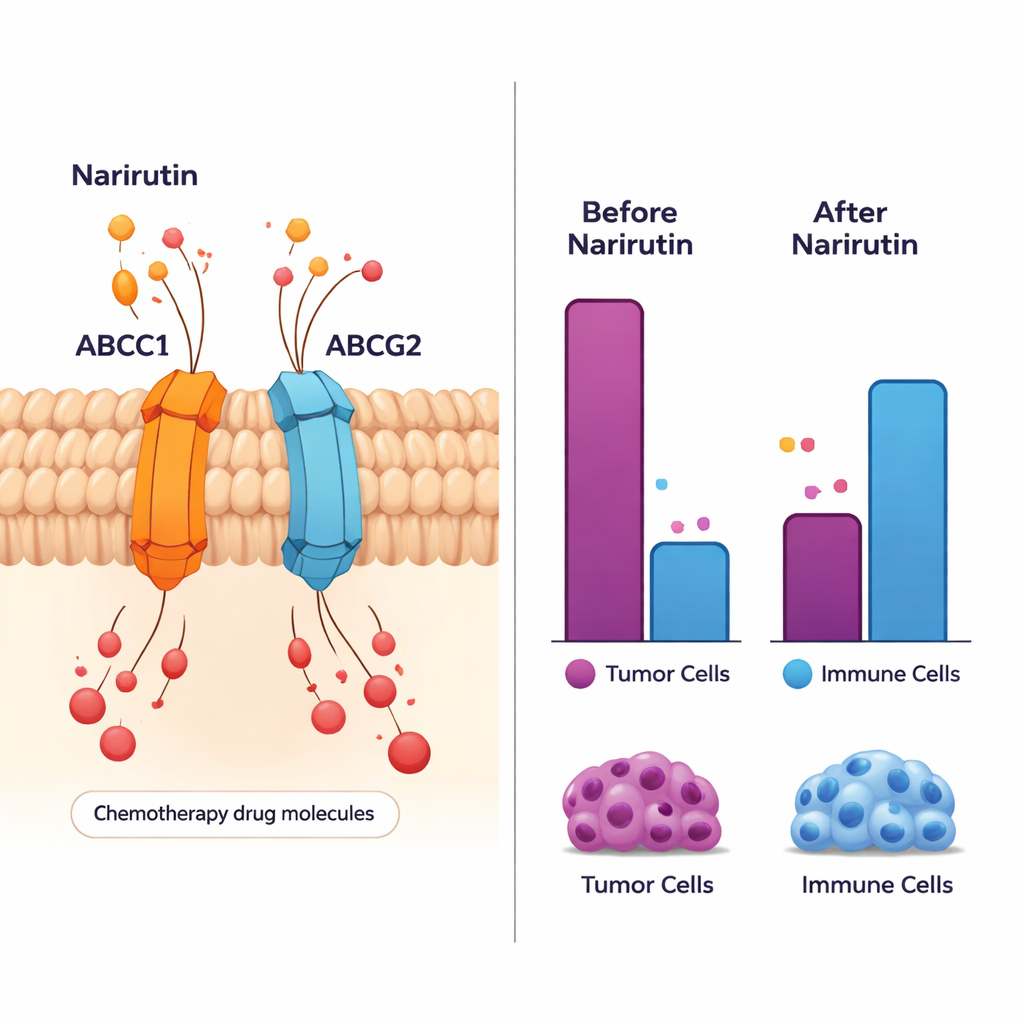
Het immuunbuurtje van de tumor hervormen
Kanker groeit niet geïsoleerd; het leeft binnen een druk ‘buurtje’ van immuuncellen, bloedvaten en steunweefsel. De studie onderzocht 28 verschillende typen immuuncellen rond colorectale tumoren en vond brede verschuivingen vergeleken met gezond weefsel. Bepaalde nuttige immuuncellen, zoals geactiveerde B‑cellen en specifieke T‑cellen, waren in tumoren in grotere aantallen aanwezig of gedroegen zich anders. De belangrijkste doelwitten van narirutin, met name ABCC1, ABCG2 en PTGS1, vertoonden sterke verbanden met deze immuunveranderingen. Dit suggereert dat narirutin door in te grijpen op deze genen niet alleen direct op kankercellen kan werken, maar ook de lokale immuunrespons kan bijsturen — mogelijk waardoor het milieu minder gunstig wordt voor tumorgroei.
Belofte, maar er is nog werk te doen
In begrijpelijke termen stelt dit onderzoek voor dat een natuurlijke flavonoïde uit citrus de pompen waarmee kankercellen chemotherapie ontwijken zou kunnen ‘verstoren’ en het immuuncircuit rond colorectale tumoren zou kunnen helpen resetten. Het werk is gebaseerd op krachtige computeranalyses en grote genetische datasets, en niet op laboratorium‑ of klinische proeven, dus het is een vroege maar belangrijke stap. Als toekomstige experimenten in cellen, dieren en patiënten deze voorspellingen bevestigen, zouden narirutin — of medicijnen geïnspireerd door dit molecuul — op termijn deel kunnen uitmaken van combinatietherapieën die standaardbehandelingen voor colorectale kanker effectiever maken en minder vatbaar voor resistentie.
Bronvermelding: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
Trefwoorden: colorectale kanker, narirutin, geneesmiddelenresistentie, tumormicro‑milieu, immuunmodulatie