Clear Sky Science · nl
Multimodale beeldvormingsevaluatie van de hypoxische beenmergomgeving en type H vasculaire schade bij diabetes
Waarom botgezondheid belangrijk is bij diabetes
Mensen denken vaak bij type 1 diabetes aan bloedsuiker en insuline, maar de ziekte verandert ook stilletjes het skelet. Veel patiënten ontwikkelen zwakkere botten en lopen een hoger risico op fracturen, zelfs wanneer hun botdichtheidstests vrijwel normaal lijken. Deze studie onderzoekt wat er diep in het beenmerg gebeurt bij konijnen met een diabetesmodel, waarbij geavanceerde medische beeldvorming wordt gebruikt om kleine bloedvaten en zuurstofniveaus in actie te volgen. Inzicht in deze verborgen schade kan wijzen op eerder stellen van de diagnose en op nieuwe behandelingen die de botsterkte bij mensen met diabetes beschermen.
De verborgen bloedwegen van het bot
Binnen lange botten zoals het scheenbeen ligt een dicht netwerk van bloedvaten dat niet alleen het bot voedt, maar ook de groei en reparatie ervan stuurt. Onder deze vaten bevindt zich een speciale subtype die “type H” vaten wordt genoemd, gegroepeerd nabij de uiteinden van botten waar groeischijven en actieve botremodellering plaatsvinden. Deze vaten vervoeren meer zuurstof dan andere en zijn nauw verbonden met de vorming van nieuw bot. Bij type 1 diabetes veroorzaakt langdurige hoge bloedsuiker echter reactieve bijproducten en oxidatieve stress die dit fijn afgestelde systeem kunnen verstikken. De onderzoekers wilden in levende dieren visualiseren hoe deze veranderingen zich in verschillende regio’s van het bot ontvouwen.
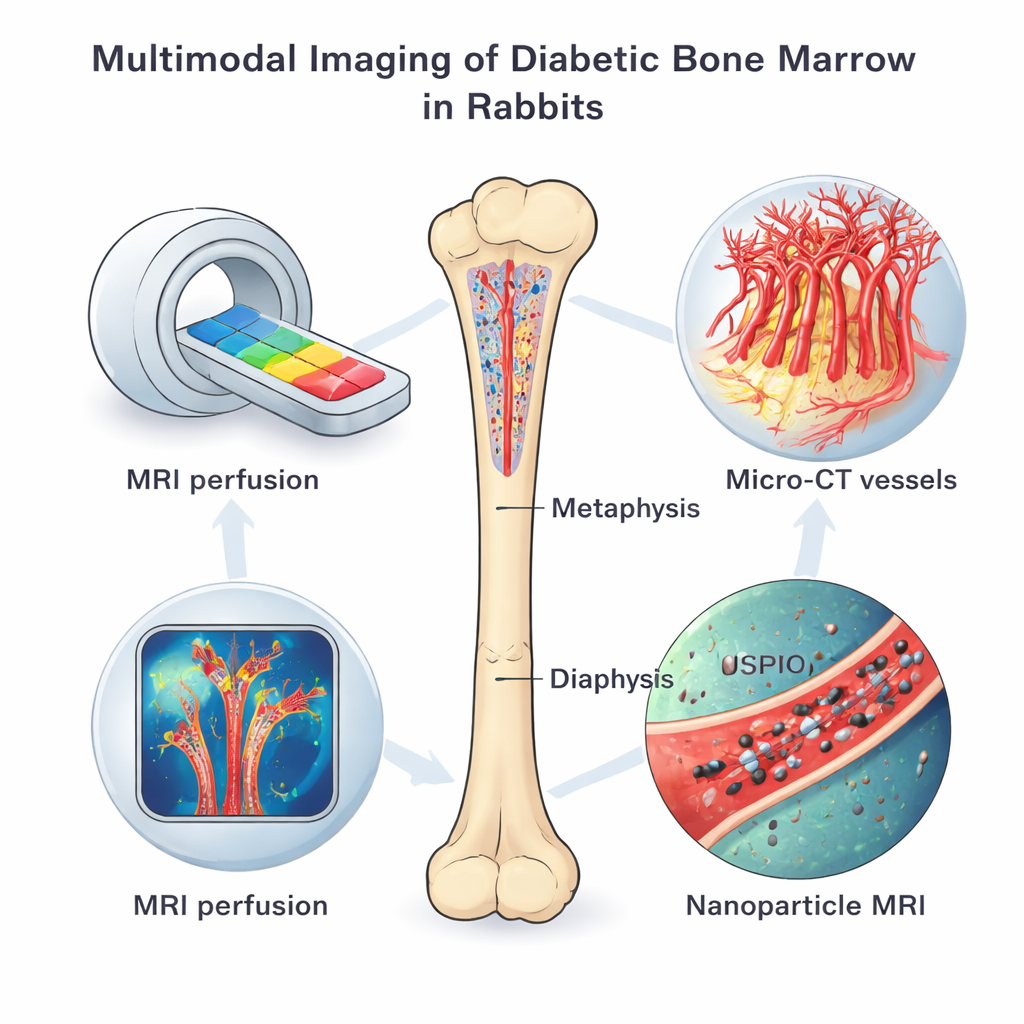
Levend bot scannen vanuit meerdere hoeken
Het team gebruikte een reeks beeldvormingstools bij konijnen met chemisch geïnduceerde type 1 diabetes en bij gezonde controles, allemaal onderzocht vier maanden nadat de diabetes was vastgesteld. Dynamische contrastversterkte MRI volgde hoe snel een kleurstof het beenmerg in en uit bewoog, wat onthulde hoe goed kleine vaten het weefsel perfundeerden en hoe lek ze waren. Een andere MRI-techniek, versterkt met speciale ijzerhoudende nanodeeltjes, toonde hoe actief de endotheelcellen de deeltjes opnamen, een teken van veranderde stofwisseling en vatgedrag. Nadat de dieren waren geofferd, brachten high-resolution micro-CT-scans het driedimensionale netwerk van microvaten in kaart, terwijl fluorescentiekleuring, genetische tests en elektronenmicroscopie vademtypes, zuurstofsensorsystemen en cellulaire schade in detail onderzochten.
Waar diabetes het hardst toeslaat in het bot
Over alle beeldvormingstechnieken heen lieten diabetische konijnen beenmergvaten zien die permeabeler en abnormaler waren dan die van gezonde dieren. Contrastvloeistof bewoog sneller en verbleef langer, en ijzer-nanodeeltjes werden intenser opgenomen, vooral nabij de metafyse—de uiteinden van het bot die rijk zijn aan type H vaten. Micro-CT toonde dat diabetische botten veel minder kleine vaten en een lagere totale vatvolumes hadden, tot het punt dat het gebruikelijke voordeel van de metafyse ten opzichte van de schachtregio verdween. Flowcytometrie en fluorescentie-labeling bevestigden dat het aandeel type H vaten zelf scherp daalde bij diabetes, terwijl nieuwe uitgroeiende vaten langs de groeischijf schaars werden. Kortom, de vasculaire niche die normaal sterke botvorming ondersteunt werd selectief uitgedund en beschadigd.
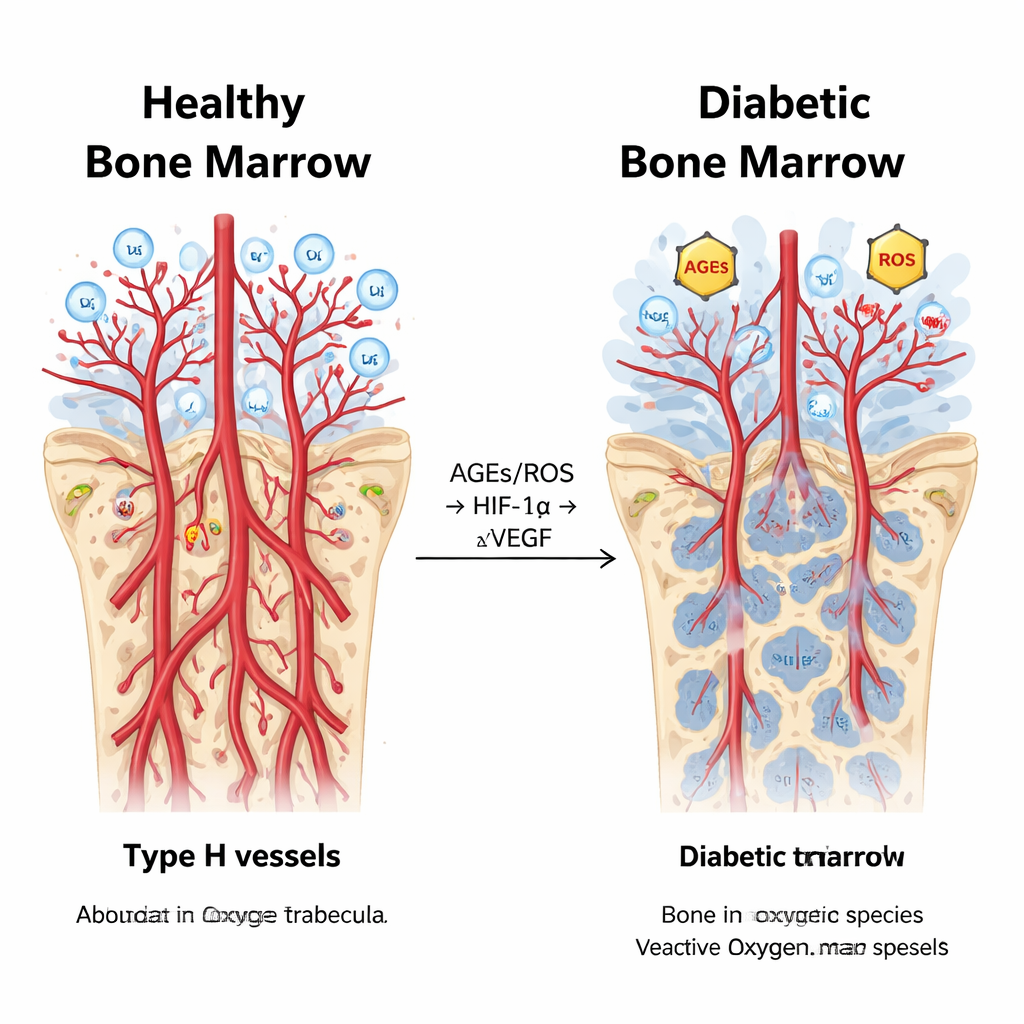
Een verwarde chemische cascade in diabetisch merg
Dieper gravend maten de wetenschappers moleculen die betrokken zijn bij hypoxie—het tekort aan voldoende zuurstof—en bij de oxidatieve stress die wordt veroorzaakt door hoge bloedsuiker. Diabetische konijnen hadden hogere niveaus van geavanceerde glycatieresiduen (AGEs) en reactieve zuurstofsoorten (ROS), samen met sterkere activiteit van het zuurstof-sensorische eiwit HIF-1α en zijn receptorpartner AGER, met name in de metafyse. Verrassend genoeg, hoewel HIF-1α gewoonlijk vaatgroei stimuleert, was het centrale groeisignaal VEGF juist onderdrukt in het diabetische beenmerg, en daalde de vatuitgroei. Statistische analyses verbonden deze draden: markers van oxidatieve stress en abnormale perfusie stegen en daalden synchroon met HIF-1α, terwijl VEGF en maatstaven voor vaatdichtheid in tegenovergestelde richting bewogen. Dit patroon suggereert dat bij chronische diabetes het normale "zuurstofalarm"-systeem wordt gekaapt, waardoor ontsteking en lekkage worden aangedreven in plaats van gezonde nieuwe vaat- en botvorming.
Wat dit betekent voor mensen met diabetes
Simpel gezegd toont de studie dat diabetes botten niet uniform verdunt; het creëert plaatselijke "hotspots" van vasculaire schade en lage zuurstof, vooral daar waar het bot normaal het sterkst en meest regeneratief zou moeten zijn. Door meerdere beeldvormingstechnieken te combineren konden de onderzoekers zowel de functionele lekkage als het structurele verlies van type H vaten zien en deze veranderingen koppelen aan een specifiek chemisch traject met AGEs, ROS, HIF-1α en VEGF. Voor patiënten suggereert dit werk dat toekomstige scans mogelijk vroege botaantasting kunnen detecteren voordat fracturen optreden, en dat therapieën gericht op het herstellen van gezonde zuurstofsignalering en het beschermen van type H vaten een nieuwe invalshoek kunnen vormen bij het voorkomen van diabetische botziekte.
Bronvermelding: Lei, H., Wang, K., Li, L. et al. Multimodal imaging evaluation of hypoxic bone marrow microenvironment and type H vascular injury in diabetes. Sci Rep 16, 7206 (2026). https://doi.org/10.1038/s41598-026-37164-z
Trefwoorden: type 1 diabetes, beenmerg, microvasculaire schade, hypoxie, botbreukgevoeligheid