Clear Sky Science · nl
Genoomwijde screens identificeren kernregelaars van prionproteïne-expressie op celoppervlakken
Waarom dit belangrijk is voor de gezondheid van de hersenen
Prionziekten, zoals Creutzfeldt–Jakob bij mensen en de ziekte van “gekke koeien” bij runderen, zijn zeldzaam maar altijd dodelijk. Een centrale boosdoener is een normaal herseneiwit, het prionproteïne, dat verkeerd kan vouwen en zo schade van cel naar cel kan verspreiden. Hoe meer van dit eiwit op het oppervlak van zenuwcellen zit, hoe makkelijker de ziekte zich kan ontwikkelen. Deze studie had tot doel om, over het hele genoom, in kaart te brengen welke genen bepalen hoeveel prionproteïne zichtbaar is aan de buitenzijde van neuronachtige cellen. Die kaart kan onderzoekers helpen nieuwe manieren te ontwerpen om dit eiwit te verlagen en mogelijk meerdere neurodegeneratieve ziekten te vertragen.
De bedieningsknoppen van de cel vinden
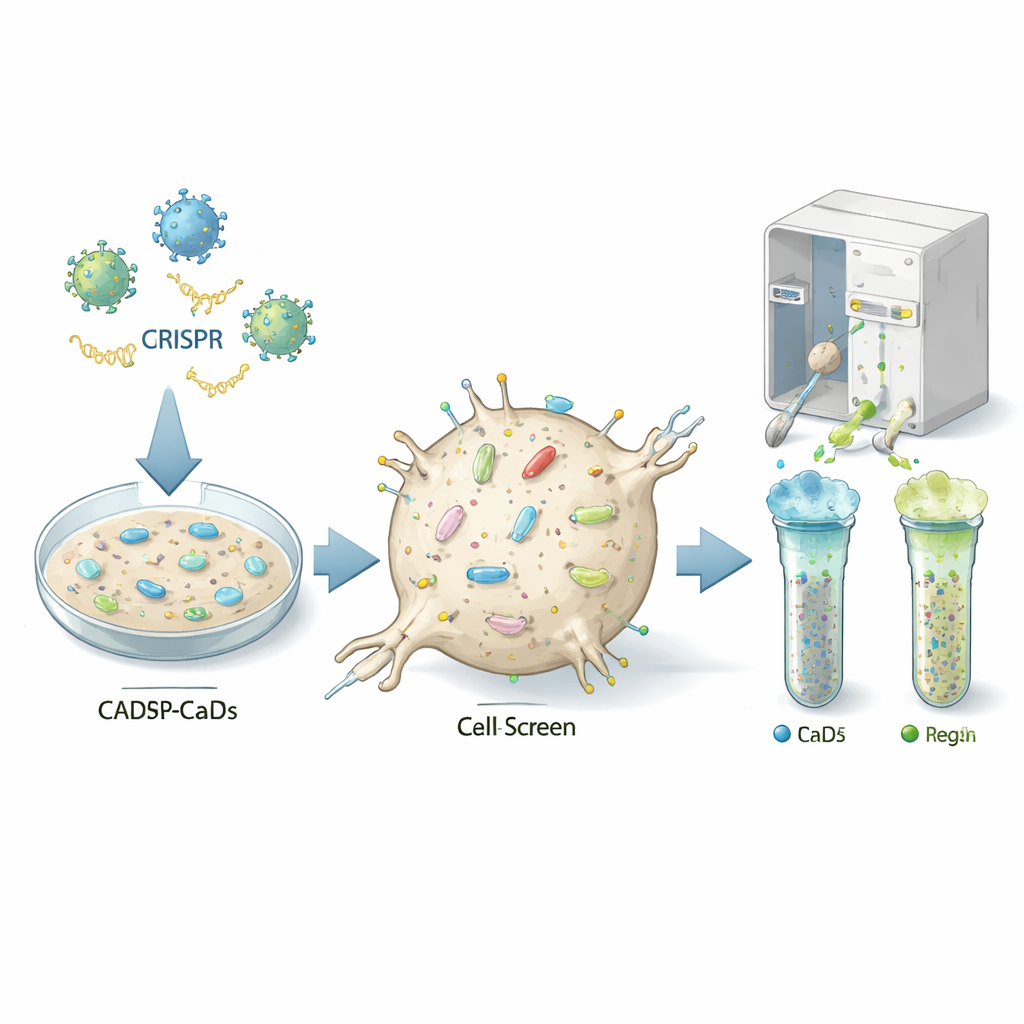
De auteurs gebruikten een krachtige genbewerkingstechniek, CRISPR, om bijna elk gen één voor één uit te schakelen in een muisachtige, neuronachtige cellijn die vatbaar is voor prioninfectie (CAD5-cellen). Iedere cel kreeg een andere genetische “klap”, zodat de resulterende populatie miljoenen varianten bevatte, elk zonder een specifiek gen. Het team kleurde de cellen vervolgens met fluorescente antilichamen die het normale prionproteïne op het celoppervlak herkennen en gebruikte een cel-sorteermachine om cellen met abnormaal lage of hoge niveaus van dit eiwit te scheiden. Door te sequencen welke gids-RNA’s verrijkt waren in de lage of hoge groepen, konden ze afleiden welke uitgeschakelde genen normaal gesproken als aan- of uit-schakelaars voor prionproteïne aan het celoppervlak werken.
Twee celtoestanden, overlappende antwoorden
Zenuwcellen zien er tijdens hun levensloop niet allemaal hetzelfde uit en gedragen zich ook anders, dus vroegen de onderzoekers zich af of dezelfde genen prionproteïne in verschillende celtoestanden reguleren. CAD5-cellen kunnen in een snelgroeiende, minder gespecialiseerde toestand worden gehouden of, door serum uit het kweekmedium te verwijderen, worden gestimuleerd om een meer volwassen, neuronachtige vorm aan te nemen. Het team voerde dezelfde genoomwijde CRISPR-screen in beide condities uit. In de ongedifferentieerde (minder volwassen) cellen valideerden ze 46 genen die, wanneer aanwezig, het oppervlakprion verhoogden, en 21 die het verlaagden. In de gedifferentieerde (meer neuronachtige) cellen bevestigden ze 41 positieve en 13 negatieve regulatoren. Drieëntwintig genen — voornamelijk die welke helpen een lipide-“anker” aan het eiwit te bevestigen — waren in beide celtoestanden gedeeld, wat wijst op een kernregulerend systeem dat onafhankelijk van volwassenheid werkt.
Belangrijke assemblagelijnen die het meest tellen
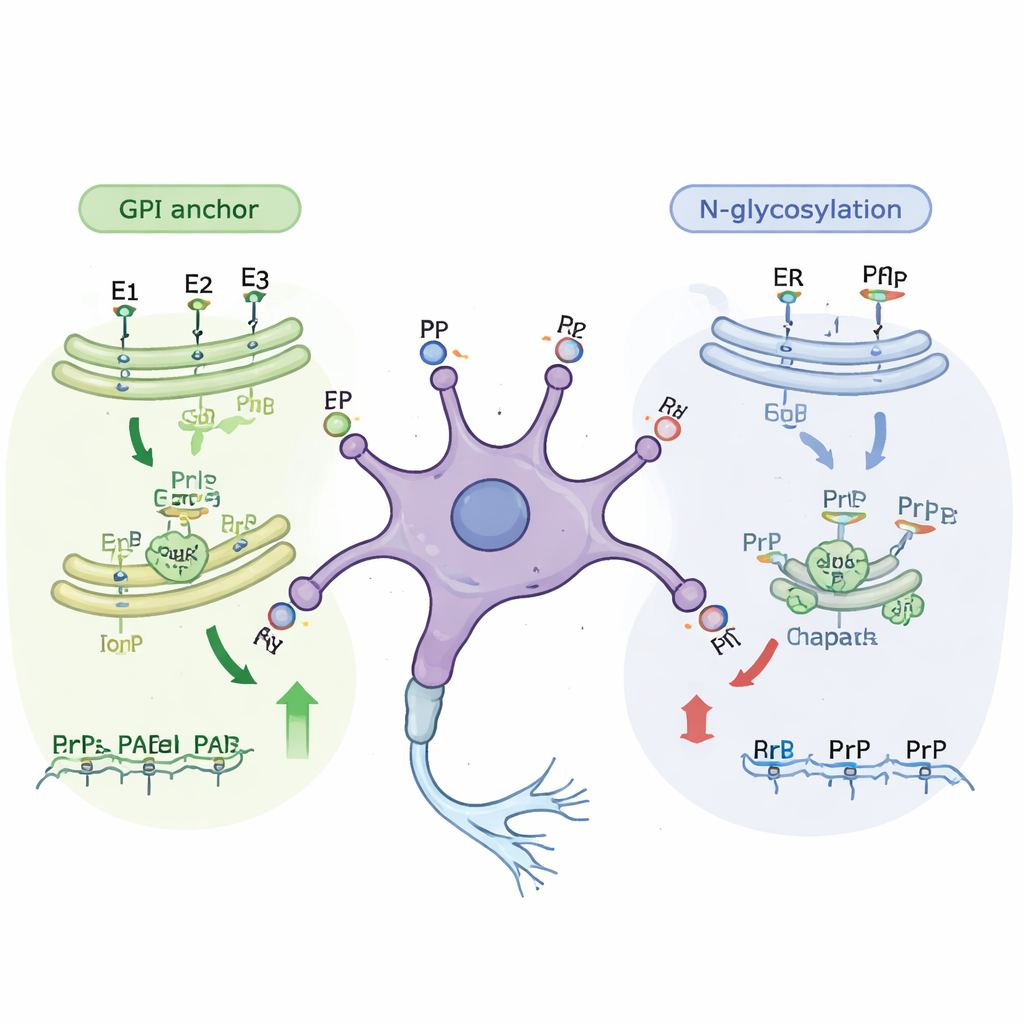
Verdere analyse toonde aan dat veel van de nieuw geïdentificeerde genen behoren tot bekende cellulaire “assemblagelijnen” die eiwitten onderweg naar het celoppervlak bewerken. Een belangrijk pad bouwt het GPI-anker, een klein vetrijk structuurtje dat het prionproteïne aan de buitenzijde van het celmembraan vastzet. Het verstoren van vrijwel elke stap in dit pad verminderde hoeveel prionproteïne het oppervlak bereikte, zowel in onrijpe als in rijpe cellen. Een tweede route betreft N-glycosylering, waarbij complexe suikerketens aan eiwitten worden toegevoegd terwijl ze door de interne membranen van de cel gaan. Genen in deze suikertoevoegende route bleken vooral belangrijk in de minder volwassen cellen. Toen de onderzoekers cellen behandelden met kleine moleculen die specifieke glycosyleringsstappen blokkeren, daalden de hoeveelheden oppervlakprion met ongeveer een derde zonder dat de cellen stierven, wat de genetische bevindingen bevestigt.
Hulp-eiwitten en stressreacties
De screens benadrukten ook moleculaire chaperonnes — eiwitten die andere eiwitten helpen correct op te vouwen — als belangrijke prionregulatoren. In het bijzonder kwam Hspa5 (ook BiP genoemd), een centrale chaperonne in de eiwitvouwcompartimenten van de cel, naar voren als positieve regulator in de meer neuronachtige cellen. Toen de onderzoekers Hspa5 met een geneesmiddel inhibitiseerden, daalden de oppervlakprionniveaus in beide celtoestanden, wederom zonder duidelijke schade aan de cellen. Andere hits omvatten genen betrokken bij het verplaatsen van eiwitten door de cel, het regelen van genexpressie, en meerdere eiwitten die gelinkt zijn aan synapsfunctie en andere hersenziekten zoals Alzheimer en ALS. Samen tonen deze resultaten dat de hoeveelheid prionproteïne aan het celoppervlak wordt gevormd door een netwerk van paden die eiwitproductie, modificatie, transport en kwaliteitscontrole overspannen.
Wat dit betekent voor toekomstige behandelingen
Dit werk levert de eerste uitgebreide catalogus van genen die bepalen hoeveel prionproteïne op het oppervlak van neuronachtige cellen verschijnt die vatbaar zijn voor prioninfectie. Sommige van deze genen, in het bijzonder die in de GPI-anker- en N-glycosyleringspaden en het Hspa5-chaperonnesysteem, vormen veelbelovende startpunten voor medicijnontdekking: het temperen van hun activiteit zou de hoeveelheid prionproteïne die kan verkeerdvouwen kunnen verminderen, en eerdere studies tonen dat zelfs gedeeltelijke verlagingen ziekte bij dieren aanzienlijk kunnen vertragen. Tegelijkertijd benadrukken de duidelijke verschillen tussen onrijpe en rijpe cellen dat de toestand van de hersencel ertoe doet bij het kiezen van targets. Hoewel meer onderzoek nodig is om te testen hoe het manipuleren van deze genen daadwerkelijke prioninfectie en andere neurodegeneratieve aandoeningen in levende hersenen beïnvloedt, biedt deze studie een routekaart van cellulaire hendels die onderzoekers kunnen verkennen om deze verwoestende ziekten te vertragen of te voorkomen.
Bronvermelding: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Trefwoorden: prionproteïne, CRISPR-screen, neurodegeneratie, eiwitglycosylering, GPI-anker