Clear Sky Science · nl
Drukversterkte dubbele vaste-oppervlakte ultrasnelle koeling verbetert herstel na ontdooiing in hepatocyten en precies gesneden leverplakken
Waarom het invriezen van leverweefsel ertoe doet
Cellen en weefsels buiten het lichaam levend houden is een van de stille werkpaarden van de moderne geneeskunde. Bevroren levercellen helpen onderzoekers nieuwe medicijnen te testen, ziekte te modelleren en kunnen op termijn falende organen repareren. Maar het invriezen van levend materiaal is ingewikkeld: als ijs kristalliseert binnen of tussen cellen, scheurt het tere structuren uiteen. Deze studie onderzoekt een nieuwe manier om levercellen en dunne leverplakken zó snel en onder zulke gecontroleerde omstandigheden te koelen dat schadelijke ijskristallen nauwelijks de tijd krijgen om zich te vormen.
Het probleem met ijs en chemische beschermers
Conventionele cryopreservatie steunt op twee onvolmaakte middelen: kou en chemicaliën. Tijdens het afkoelen neigt water naar ijsvorming, wat membranen kan doorboren en weefsels kan ontregelen. Om dit tegen te gaan voegen wetenschappers cryoprotectieve middelen toe, zoals dimethylsulfoxide (DMSO), die helpen dat water in een glasachtige toestand stolt in plaats van in kristallijn ijs. Bij de hoge concentraties die gewoonlijk gebruikt worden, kunnen deze middelen echter zelf toxisch zijn voor cellen of schadelijke zwelling en krimp veroorzaken wanneer ze in en uit het weefsel bewegen. Het doel van de auteurs was het gebruik van DMSO te verminderen terwijl schadelijk ijs vermeden blijft, zodat het bewaren van levercellen en -weefsel veiliger en praktischer wordt.
Een nieuwe manier om tegelijk te persen en te koelen
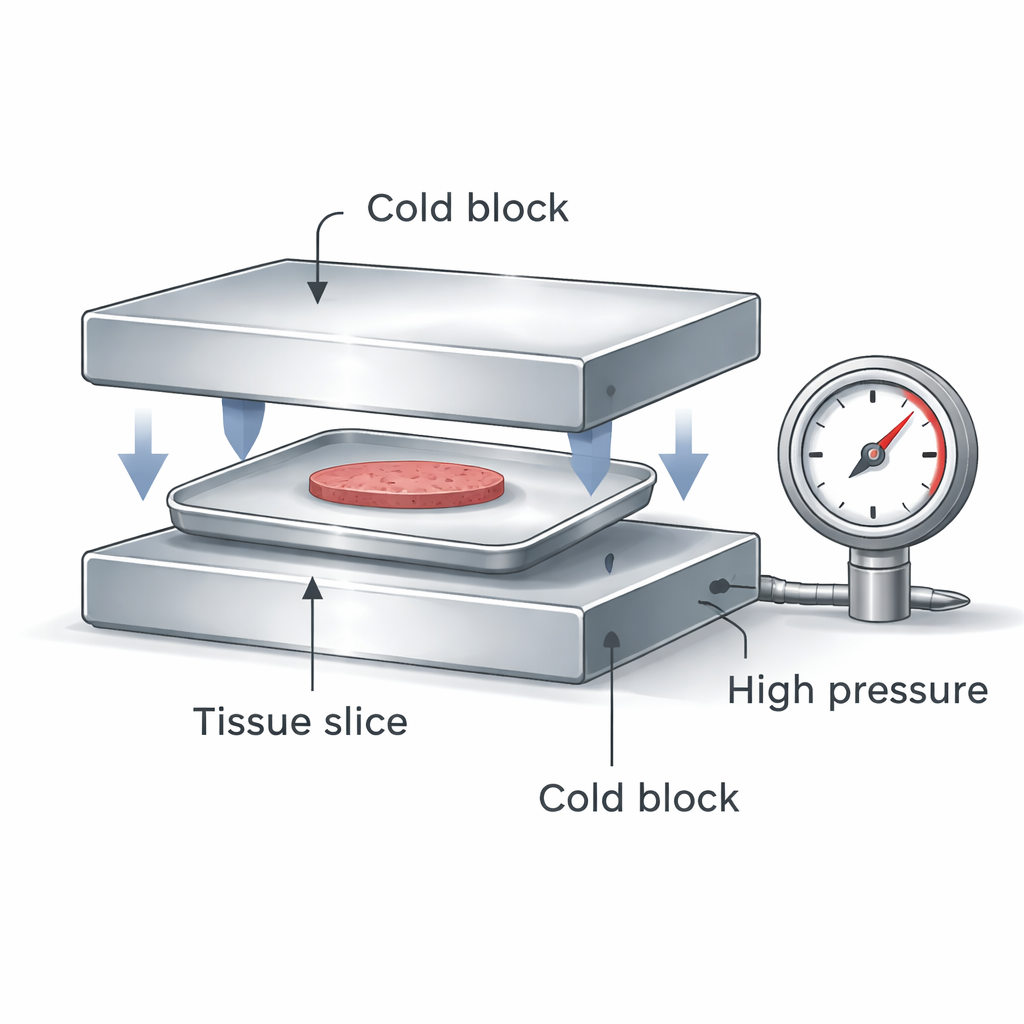
Het team ontwierp een compact apparaat dat een verzegelde, platte aluminium houder met levercellen of precies gesneden leverplakken tussen twee extreem koude metalen blokken klemt. Wanneer de blokken samen drukken, doen ze tegelijk twee belangrijke dingen: ze creëren hoge druk in de verzegelde houder en onttrekken warmte aan het monster zowel van boven als van onderen. Hoge druk verandert het gedrag van water zodat ijs bij lagere temperaturen vormt en de oplossing gemakkelijker glasachtig wordt. Dubbelzijdig contact levert een veel snellere en gelijkmatiger koelsnelheid dan simpelweg een plastic buis in vloeibare stikstof dompelen, en de verzegelde houder houdt het monster geïsoleerd van verontreiniging.
Het vinden van de optimale balans tussen veiligheid en overleving
Om te beoordelen of deze aanpak zacht genoeg was voor levend materiaal, controleerden de onderzoekers eerst of de aluminium houder zelf de uit lever afkomstige HepG2-cellen niet schaadde tijdens de korte hanteringstijden. De celloverleving bleef nagenoeg ongewijzigd. Vervolgens brachten ze deze cellen vóór het invriezen bloot aan verschillende DMSO-concentraties en bevestigden een bekende afweging: meer DMSO onderdrukt ijsvorming beter maar wordt duidelijk toxisch bij 30%, terwijl 20% overwegend nog draaglijk blijft. Voor muisleverplakken testten ze hoeveel druk het weefsel zonder bevriezing kon verdragen. Korte stoten tot 150 megapascal hadden weinig effect op de levensvatbaarheid, maar 200 megapascal veroorzaakten ongeveer 30% daling, wat een bovengrens voor veilige werking aangeeft.
Beter bewaarde leverplakken na ontdooiing
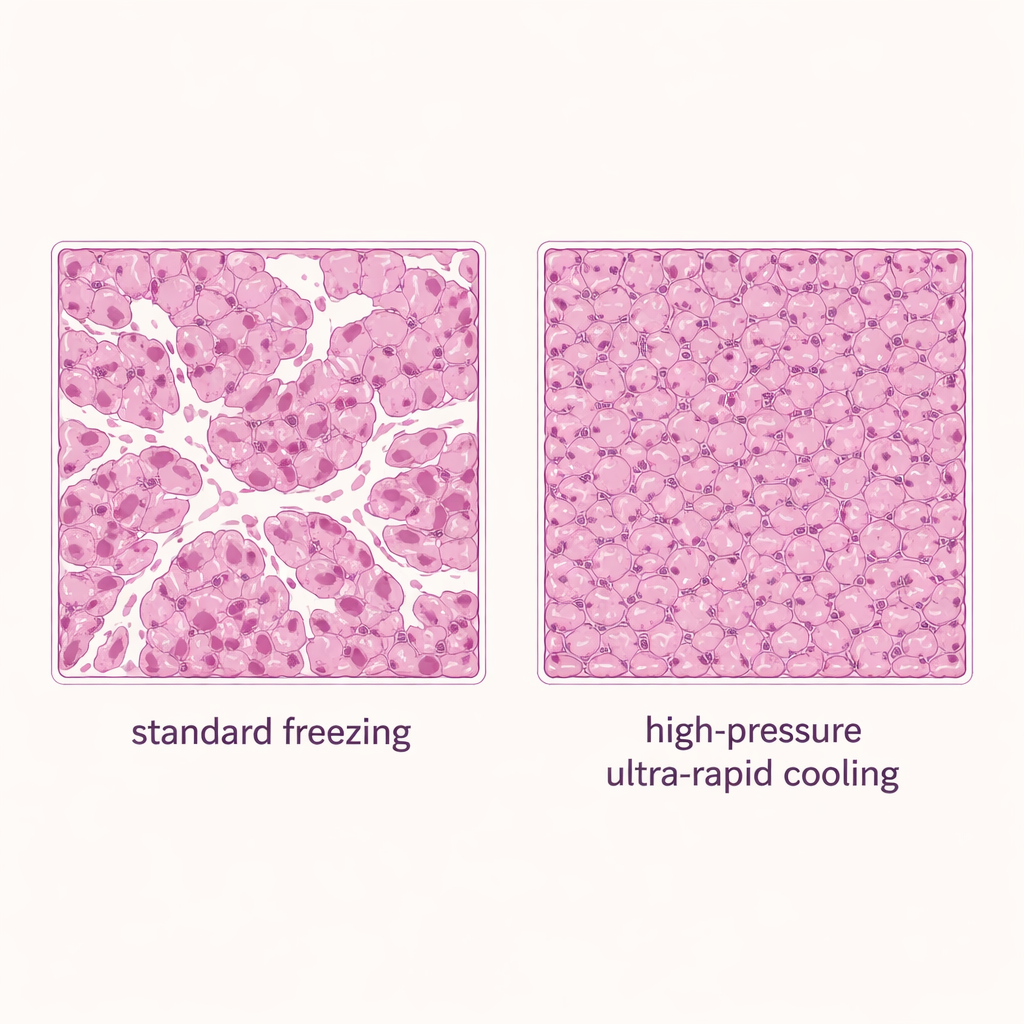
Met veilige bereiken vastgesteld vergeleken de auteurs drie invriesmethoden voor leverplakken: standaard onderdompeling van de verzegelde houder in vloeibare stikstof (een convectie- of vloeistofgebaseerde benadering), vaste-oppervlaktekoeling zonder extra druk, en vaste-oppervlaktekoeling met hoge druk bij 150 megapascal. Alle groepen gebruikten 20% DMSO. De drukondersteunde methode leverde de beste resultaten: ongeveer 80% van de oorspronkelijke levensvatbaarheid van het weefsel bleef behouden, beter dan zowel standaardvriezing als uitsluitend vaste-oppervlaktekoeling. Microscopie van gekleurde weefselplakken ondersteunde deze bevindingen. Monsters die conventioneel door onderdompeling waren bevroren toonden veel open witte ruimtes—typische tekenen van ijsbeschadiging—terwijl drukversterkte vaste-oppervlaktekoeling dichter, meer intact weefsel met veel minder lege ruimten produceerde.
Wat dit betekent voor toekomstige weefselsbanken
Samenvattend laat de studie zien dat het samendrukken van een verzegelde, in aluminium verpakte leverplak tussen twee ultra-koude blokken onder zorgvuldig gecontroleerde hoge druk de overleving na ontdooiing sterk kan verbeteren. Door snellere, gelijkmatigere koeling te combineren met drukgeïnduceerde veranderingen in waterverschijnselen, beperkt de methode de groei van schadelijk ijs terwijl toch een matige, klinisch vertrouwde DMSO-concentratie wordt gebruikt. Voor de niet-specialist is de conclusie dat slim ingenieurswerk—hoe we weefsel verpakken en koelen—even belangrijk kan zijn als de chemicaliën die we toevoegen. Deze dubbelzijdige, hoge-drukbenadering kan een opstap vormen naar veiliger, betrouwbaarder bewaren van leverweefsel en mogelijk later ook andere organen voor onderzoek en therapie.
Bronvermelding: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Trefwoorden: cryopreservatie, leverweefsel, vitrificatie, hoge druk koeling, ijsvrije vriezing