Clear Sky Science · nl
DANEELpath open source digitale analysetools voor histopathologisch onderzoek in neuroblastoommodellen
Waarom kleine tumoren in gel ertoe doen
Kanker is niet slechts een massa losgeslagen cellen; het is een hele buurt waarin cellen met elkaar en met het omringende skelet communiceren. Bij kinderoncologieën zoals neuroblastoom kan deze ondersteunende omgeving tumoren helpen groeien en weerstand bieden tegen behandeling. Deze studie introduceert DANEELpath, een gratis, open-source set digitale hulpmiddelen die microscoopbeelden van in het lab gekweekte mini‑tumoren omzet in rijke, kwantitatieve kaarten. Daarmee helpt het wetenschappers te begrijpen hoe kankercellen zich organiseren, hoe ze reageren op experimentele geneesmiddelen en hoe die inzichten kunnen bijdragen aan betere therapieën voor kinderen.
Kleine tumorwerelden in het lab bouwen
Om de complexe omgeving van een echte tumor na te bootsen, kweken onderzoekers neuroblastoomcellen in zachte 3D‑hydrogels gemaakt van gelatine en zijde. In deze omgeving vormen cellen van nature ronde clusters, vergelijkbaar met mini‑tumoren. Een belangrijke speler is vitronectine, een plakkerig eiwit in de extracellulaire matrix dat cellen helpt hechten en kan bijdragen aan agressiever ziektegedrag. Het team bereidde hydrogels met en zonder extra vitronectine en stelde sommige gels bloot aan cilengitide, een experimenteel middel dat receptoren gerelateerd aan vitronectine blokkeert. Na weken van groei werden de gels in plakjes gesneden, gekleurd en gescand als hoge‑resolutie whole‑slide beelden, waarmee voor elke mini‑tumorwereld een digitale versie ontstond.
Complexe beelden omzetten in meetbare patronen
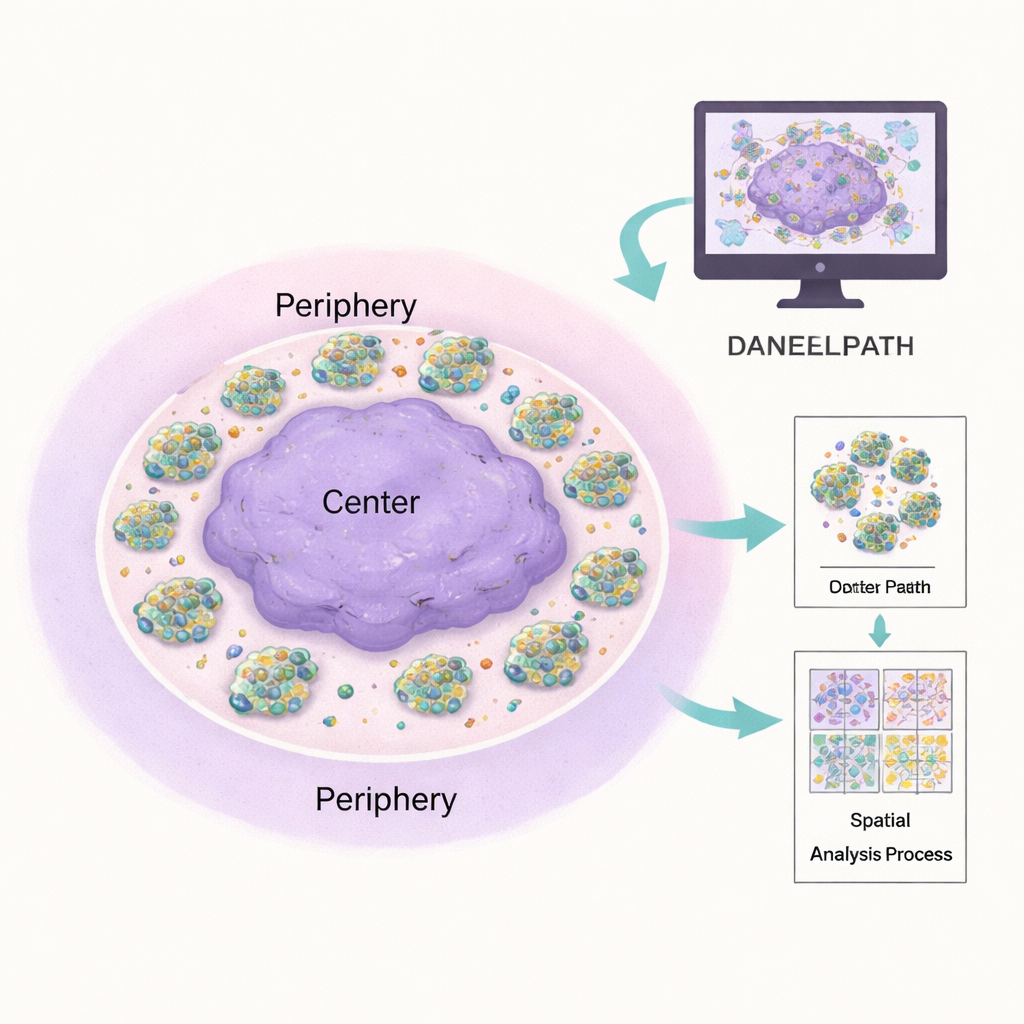
Traditionele pathologie vertrouwt op ervaren ogen aan de microscoop, wat krachtig is maar moeilijk te standaardiseren en op te schalen. DANEELpath sluit aan op het populaire open‑source platform QuPath en automatiseert veel van dit werk. Met deep‑learningmodellen genaamd U‑Nets kan de toolkit nauwkeurig elke celcluster afbakenen in gangbare kleuringen, zelfs wanneer clusters variëren van enkele cellen tot honderden. Vervolgens past het wiskundige methoden toe om elke onregelmatig gevormde hydrogel te verdelen in een evenwichtige „kern” en „periferie” ring, zodat vergelijkingen tussen binnen‑ en buitengebieden eerlijk zijn ongeacht de vorm van de gel. Dit stelde de auteurs in staat te bevestigen dat neuroblastoomclusters vaak dichter zijn naar de rand van de hydrogel toe en dat dit patroon verandert afhankelijk van vitronectinegehalte en geneesmiddelbehandeling.
Celafstand en buren van clusters meten
Naast het tellen van clusters onderzoekt DANEELpath hoe cellen en clusters ruimtelijk geordend zijn. Binnen elk cluster vindt een ander hulpmiddel individuele celkernen en meet de afstand tot de dichtstbijzijnde buur, waarmee wordt samengevat hoe dicht opeengepakt de cellen zijn. Tussen clusters biedt de toolkit drie manieren om „buren” te definiëren, waaronder een methode gebaseerd op Voronoi‑diagrammen die invloedzones rond elke cluster tekent. Door deze maten onder verschillende condities te vergelijken, toonden de onderzoekers aan dat cilengitide verandert hoeveel naburige clusters een grote cluster heeft en hoe die buren zijn verdeeld, maar op manieren die afhangen van of er vitronectine aan de gel was toegevoegd. Dit benadrukt hoe de omringende matrix en mechanische geneesmiddelen samen de tumororganisatie vormen.
De halo rond tumorclusters zien
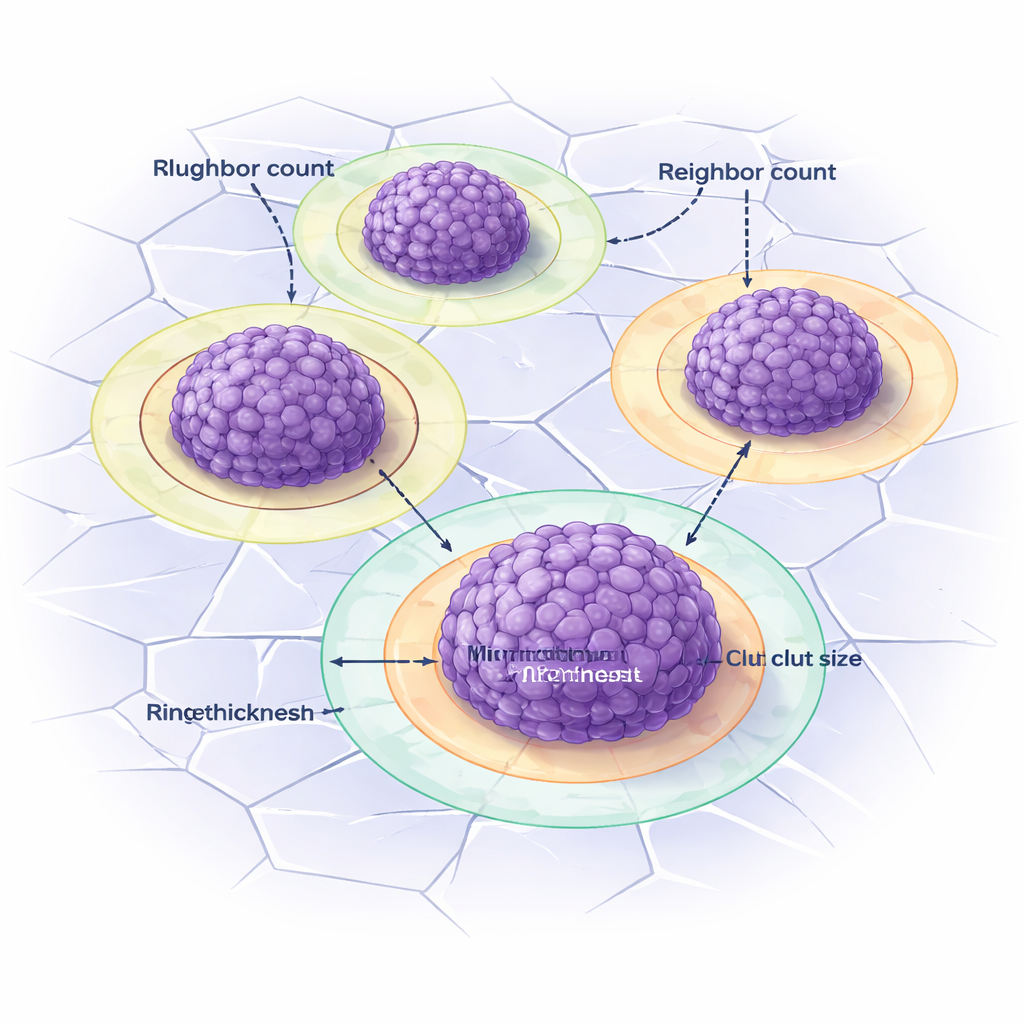
Vitronectine vormt in deze modellen vaak opvallende ringen rond clusters: een heldere „corona” wanneer alleen door de cellen geproduceerde vitronectine aanwezig is, en een bleke halo wanneer extra vitronectine in de gel is ingebouwd. Het visueel scheiden van deze ringen van de clusterkern is lastig. DANEELpath pakt dit aan door eerst Voronoi‑gebaseerde invloedgebieden rond elke cluster te tekenen en deze vervolgens naar buiten uit te breiden net genoeg om de ring vast te leggen zonder buren te overlappen. Eenvoudige beeldcontrastregels worden gebruikt om corona’s en halo’s te detecteren, en de toolkit meet automatisch hun dikte. Vergelijkbare strategieën werden ook toegepast op echte patiëntmonsters, bijvoorbeeld om immuuncellen aan de rand van tumorregio’s in kaart te brengen of zones rond bloedvaten te definiëren om te bestuderen hoe vitronectine en andere markers in menselijk neuroblastoom gerangschikt zijn.
Wat dit betekent voor toekomstig kankeronderzoek
In wezen verandert dit werk statische pathologiebeelden in gedetailleerde, reproduceerbare metingen van hoe kankercellen en hun omgeving geordend zijn. Voor niet‑specialisten betekent dat dat onderzoekers nu makkelijker kunnen testen hoe nieuwe geneesmiddelen, scaffolding‑materialen of genetische veranderingen niet alleen beïnvloeden of tumoren groeien, maar hoe ze ruimtelijk groeien. Omdat DANEELpath open‑source is, via een grafische interface werkt en op gewone computers draait, verlaagt het de drempel voor laboratoria wereldwijd om geavanceerde beeldanalyse te adopteren. In de loop van de tijd kunnen zulke hulpmiddelen helpen patronen in 3D‑modellen en patiëntweefsel te koppelen aan klinische uitkomsten, en zo gerichtere en effectievere behandelingen voor kinderen met hoog‑risico neuroblastoom te ondersteunen.
Bronvermelding: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Trefwoorden: neuroblastoom, digitale pathologie, 3D-hydrogels, extracellulaire matrix, deep learning