Clear Sky Science · nl
Iteratief multiblockkader voor detectie van neurologische aandoeningen op basis van EEG met hoge frequentie
Waarom hersengolven belangrijk zijn voor vroege diagnose
De ziekte van Alzheimer en de ziekte van Parkinson beschadigen het brein vaak jaren voordat symptomen duidelijk worden, maar artsen missen nog steeds snelle en betrouwbare middelen om ze vroegtijdig op te sporen. Deze studie presenteert een nieuwe manier om hersengolven te lezen, vastgelegd met elektro-encefalografie (EEG), met focus op de snelste ritmes van het brein. Door deze lawaaierige signalen zorgvuldig te reinigen en ze in een verklaarbaar kunstmatig-intelligentiesysteem te voeden, laten de auteurs zien dat het mogelijk is neurologische problemen te detecteren met een nauwkeurigheid die wedijvert met, en soms beter is dan, veel bestaande benaderingen.
Luisteren naar de snelste hersenritmes
EEG registreert kleine spanningsveranderingen vanaf de hoofdhuid wanneer netwerken van neuronen vuren. Traditioneel besteedden artsen en onderzoekers de meeste aandacht aan langzamere ritmes, zoals alfa- en theta-golven. Maar toenemend bewijs suggereert dat hoogfrequente “gamma”-activiteit, boven ongeveer 30 hertz, vroege tekenen van ziekte kan onthullen, van subtiele geheugenproblemen tot bewegingsstoornissen. Helaas gaan deze snelle signalen gemakkelijk verloren onder spiertrekkingen, oogknipperen en elektrische ruis. Standaardinstrumenten, zoals de bekende Fourier- en golflettransformaties, werken het beste wanneer signalen stabiel zijn in de tijd, wat niet het geval is bij EEG uit de dagelijkse praktijk. Daardoor is veel van de klinisch nuttige detail in hoogfrequente activiteit moeilijk te extraheren en gemakkelijk verkeerd te interpreteren.
Ruisige hersensignalen opschonen
Om dit aan te pakken, ontwerpen de auteurs een meerstaps “pipeline” die EEG-analyse meer behandelt als een zorgvuldig geconstrueerde productielijn dan als één magisch algoritme. Eerst gebruiken ze een benadering genaamd de Hilbert–Huang-transformatie gecombineerd met een aangepaste empirische modedecompositie. Simpel gezegd splitst deze methode automatisch een rommelig signaal in eenvoudigere bouwstenen die beter de werkelijke fluctuaties van het brein volgen. Componenten die zich als ruis gedragen—gebaseerd op hoe weinig energie en complexiteit ze bevatten—worden vervolgens weggefilterd, terwijl snelle oscillaties in het gamma-bereik behouden blijven. Deze tweefasige filtering verbetert de signaal-ruisverhouding aanzienlijk, waardoor een rommige ruwe trace verandert in een schonere weergave van hoogfrequente hersenactiviteit die waarschijnlijker echte neurale gebeurtenissen weerspiegelt dan toevallige artefacten. 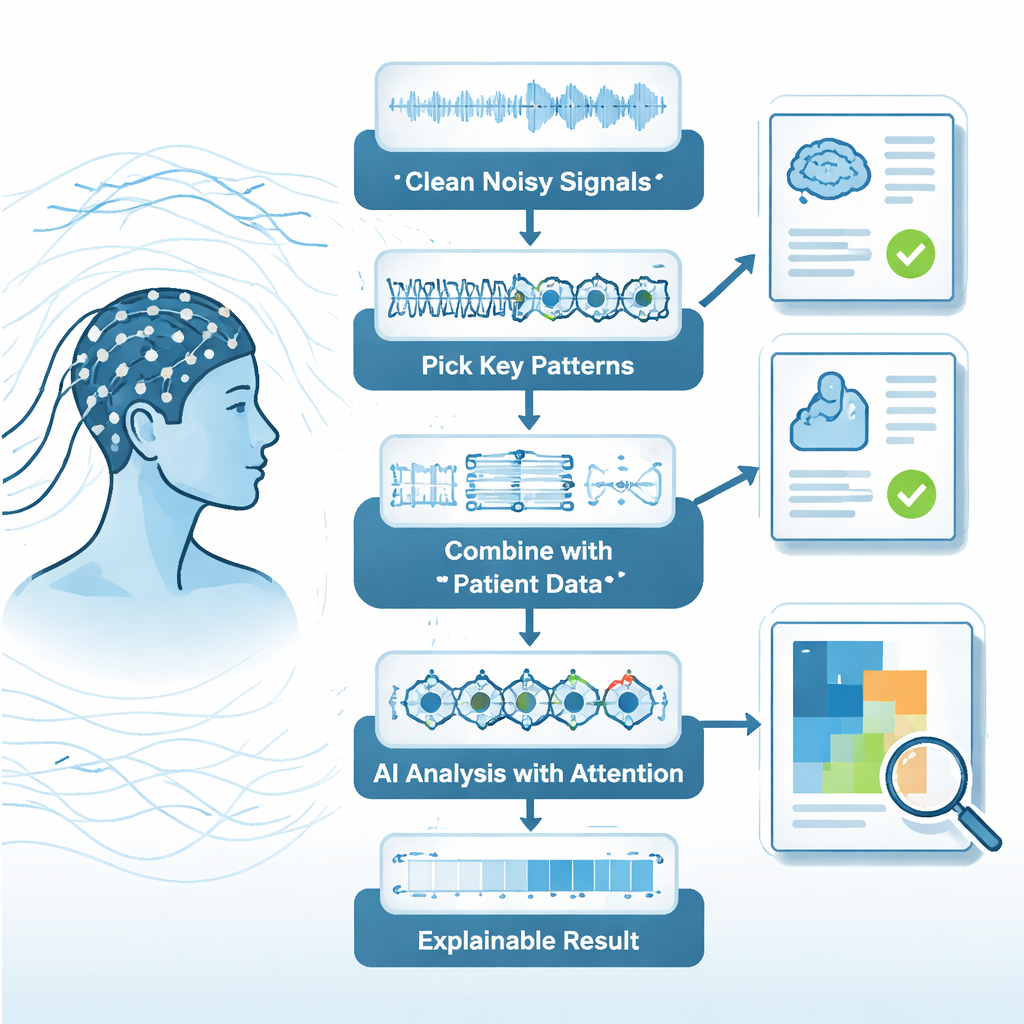
De meest sprekende patronen vinden
Zodra de signalen zijn gereinigd, richt het kader zich op de meest informatieve kenmerken. Een wavelet-pakkettransformatie verdeelt elke EEG-component in meerdere frequentiebanden, en een maatstaf genaamd Shannon-entropie beoordeelt hoe complex en informatief elke band is. Bandjes met lage scores—die meer redundant zijn dan verhelderend—worden verworpen, waardoor de feature-set met ongeveer 60% krimpt terwijl ongeveer 95% van de klinisch relevante informatie behouden blijft. Cruciaal is dat het systeem niet alleen op EEG vertrouwt. Klinische gegevens zoals leeftijd, geslacht en ziektegeschiedenis worden wiskundig uitgelijnd met de EEG-kenmerken met behulp van een techniek genaamd canonische correlatieanalyse. Deze fusie creëert een gedeelde ruimte waarin subtiele verbanden tussen hersenactiviteit en klinische context voor een computer makkelijker detecteerbaar worden.
Hoe de AI leert van hersengolven
De samengevoegde gegevens worden vervolgens geanalyseerd door een deep-learningmodel dat specifiek is gebouwd voor tijdsvariërende hersensignalen. De architectuur combineert convolutionele lagen, die lokaal patronen over kanalen en frequenties scannen, met recurrente lagen die bijhouden hoe die patronen seconde voor seconde evolueren. Een “attention”-mechanisme kent hogere gewicht toe aan tijdsegmenten die het meest diagnostisch lijken—vergelijkbaar met een clinicus die zich focust op een verdachte uitbarsting van activiteit in een opname. Om te voorkomen dat het systeem een black box is, bevat het verklaarbaarheidstools zoals Grad-CAM en geïntegreerde gradiënten. Deze leveren visuele kaarten en scores die aangeven welke frequenties, tijdvensters en klinische variabelen de grootste invloed hadden op elke voorspelling. In tests op twee grote openbare EEG-databases bereikte het kader ongeveer 94% nauwkeurigheid, met sensitiviteiten en specificiteiten boven 92%, en presteerde het beter dan meerdere sterke vergelijkingsmethoden. 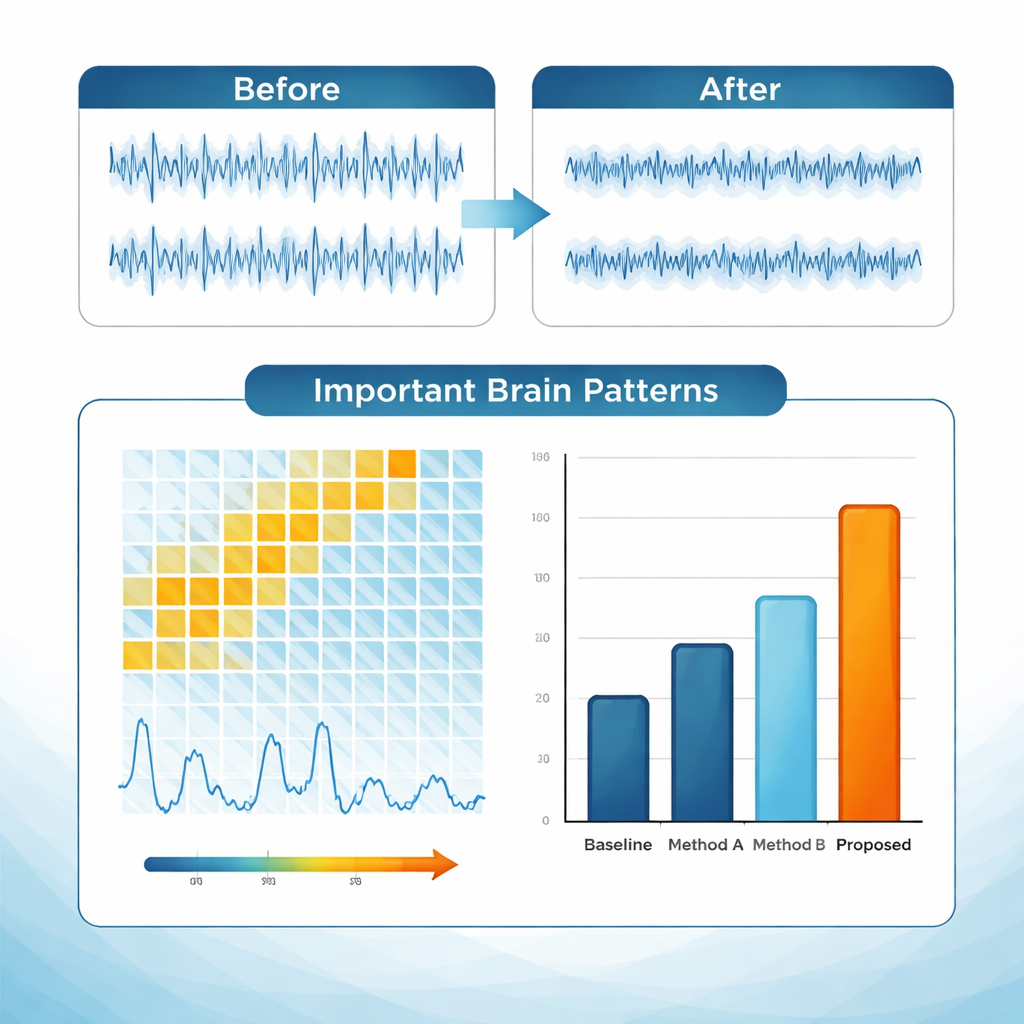
Wat dit voor patiënten kan betekenen
Voor de niet-specialist is de kernboodschap dat dit werk aantoont hoe een zorgvuldig gefaseerd, verklaarbaar AI-systeem ingewikkelde, lawaaierige EEG-opnames kan omzetten in heldere, klinisch relevante inzichten. Door beter gebruik te maken van snelle hersenritmes en deze te integreren met routinematige patiëntinformatie, signaleert het kader vroege tekenen van aandoeningen zoals Alzheimer en Parkinson en laat het artsen ook zien waarom het tot zijn conclusies kwam. Hoewel verder testen op alledaagse klinische en draagbare EEG-gegevens nodig is, wijst deze aanpak in de richting van toekomstige bed- of zelfs thuistoepassingen die neurologische problemen eerder kunnen signaleren, behandelbeslissingen kunnen ondersteunen en uiteindelijk de levenskwaliteit kunnen verbeteren voor miljoenen die risico lopen op neurodegeneratieve ziekten.
Bronvermelding: Agrawal, R., Dhule, C., Shukla, G. et al. Iterative multiblock framework for high frequency EEG based neurological disorder detection. Sci Rep 16, 5995 (2026). https://doi.org/10.1038/s41598-026-37126-5
Trefwoorden: EEG, neurologische aandoeningen, Ziekte van Alzheimer, Ziekte van Parkinson, hersenritmes