Clear Sky Science · nl
Senescentie-geassocieerde LncRNA's TRMP en TRMP-S bevorderen maagkanker door IGFL4 te activeren
Waarom dit onderzoek ertoe doet
Maagkanker behoort wereldwijd nog steeds tot de meest dodelijke kankersoorten, grotendeels omdat het vaak laat wordt ontdekt en moeilijk te behandelen kan zijn. Deze studie onthult hoe twee weinig bekende genetische moleculen, genaamd TRMP en TRMP-S, maagtumoren helpen groeien en zich verspreiden. Door de reeks gebeurtenissen te beschrijven die ze in kankercellen en in het immuune milieu van de tumor veroorzaken, wijst het werk op nieuwe manieren waarop artsen mogelijk patiënten eerder kunnen diagnosticeren en effectievere, gerichte behandelingen kunnen ontwikkelen.
Verborgen boodschappen in ons DNA
De meeste mensen denken bij genen aan blauwdrukken voor eiwitten, maar ons DNA maakt ook lange niet-coderende RNA’s (lncRNA’s) die geen eiwitten produceren en toch sterk beïnvloeden hoe cellen functioneren. TRMP en zijn kortere splice-variant TRMP-S zijn twee van zulke lncRNA’s. Ze waren eerder in verband gebracht met veroudering en celdelingscontrole in long- en dikkedarmcellen, maar hun rol bij maagkanker was onbekend. Omdat lncRNA’s zowel als diagnostische markers als therapeutische doelen kunnen dienen, onderzocht het team of TRMP en TRMP-S maagcellen naar kanker duwen en hoe ze mogelijk samenwerken met andere moleculen om dat te doen.
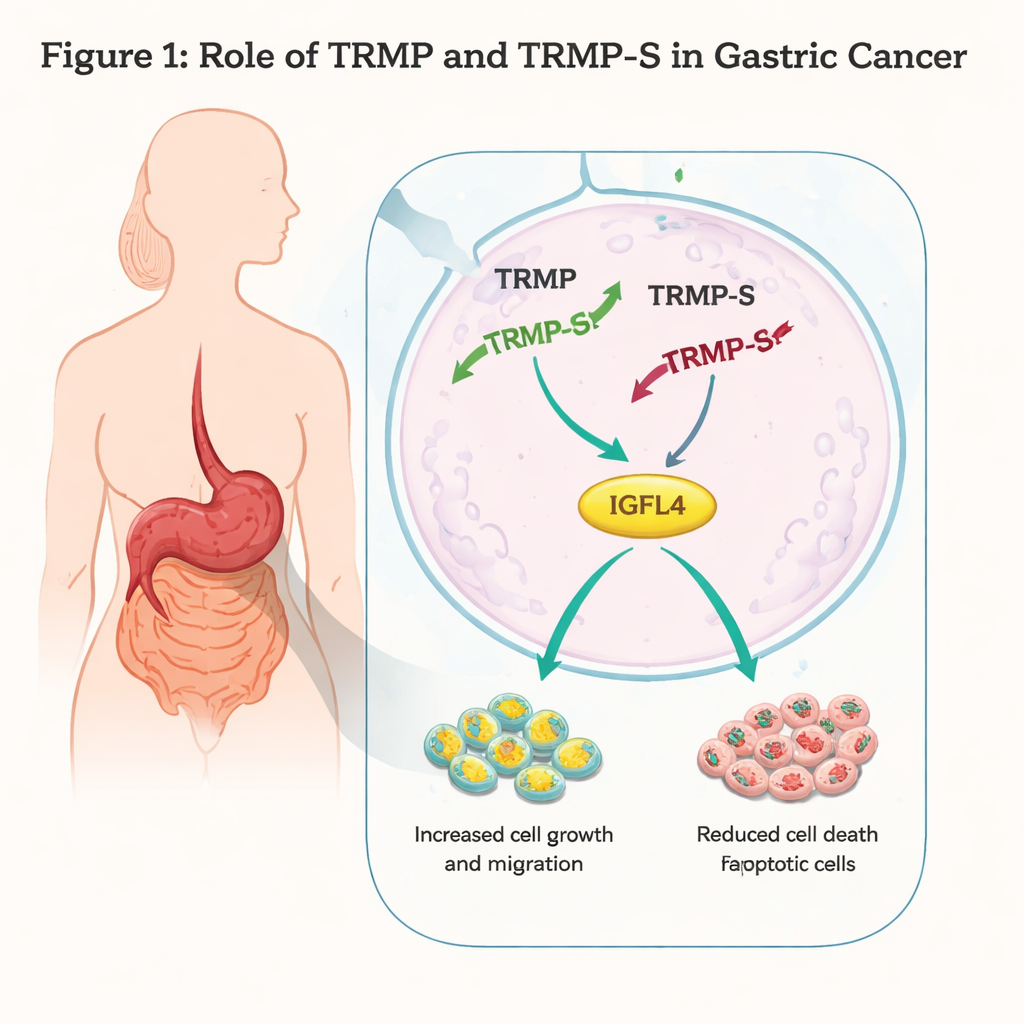
Een kankerversneller uitzetten
De onderzoekers werkten met twee humane maagkankercellijnen, AGS en MKN45, en gebruikten genetische middelen om de niveaus van TRMP-S en TRMP te verlagen. Wanneer ze TRMP-S uitschakelden, groeiden kankercellen trager, vormden ze minder kolonies en konden ze minder goed migreren door kunstmatige barrières of wonden in een schaaltje sluiten. Flowcytometrie en proteïneanalyses lieten zien dat meer cellen geprogrammeerde celdood (apoptose) ondergingen en dat de celcyclus werd geblokkeerd in de G1-fase, een belangrijke ‘controlepost’ voordat cellen hun DNA kopiëren. De niveaus van p73, een lid van de p53-tumorsuppressorfamilie, stegen bij verlies van TRMP-S, wat consistent is met sterkere celdelingscontrole en meer celdood. Deze resultaten samen duiden erop dat TRMP-S normaal gesproken fungeert als het gaspedaal voor maagkankercellen.
Een belangrijke partner: het IGFL4-signaal
Om te begrijpen hoe TRMP en TRMP-S hun effecten uitoefenen, doorzochten de onderzoekers grote patiëntendatasets van The Cancer Genome Atlas en een Koreaanse maagkankercohort. Ze zochten naar genen die zowel abnormaal hoog waren in tumoren als positief gekoppeld aan TRMP-niveaus, en bouwden vervolgens een zes-genen “risicomodel” dat de overleving van patiënten voorspelde—hogere scores waren gekoppeld aan slechtere uitkomsten. Onder deze genen stak er één uit: IGFL4, een lid van een familie die gerelateerd is aan insuline-achtige groeifactoren, waarvan bekend is dat ze groei en overleving in veel kankers stimuleren. In maagkankercellen verlaagde het onderdrukken van TRMP-S sterk de RNA- en eiwitniveaus van IGFL4, terwijl een RNA-immunoprecipitatie-assay toonde dat zowel TRMP als TRMP-S fysiek binden aan IGFL4-eiwit. Directe verlaging van TRMP had hetzelfde dempende effect op IGFL4, wat suggereert dat deze lncRNA’s helpen bij het stabiliseren of ondersteunen van de productie van dit groeibevorderende signaal.
Verspreiding vertragen en het immuune landschap herschikken
Toen de onderzoekers kleine interfererende RNA’s gebruikten om IGFL4 zelf te stilleggen, vertraagden maagkankercellen hun groei, migreerden ze minder en toonden ze een verminderde capaciteit om door membranen heen te dringen en wonden te sluiten. Analyse van patiëntentumorgegevens toonde aan dat IGFL4-niveaus significant hoger waren in maagtumoren dan in normaal maagweefsel, en verhoogd waren in veel andere kankertypen. Belangrijk is dat tumoren met hoge IGFL4-expressie onderscheidende patronen van immuuncel-infiltratie lieten zien: meer ongedifferentieerde macrofagen (M0) en minder plasmacellen, monocyten, eosinofielen en neutrofielen. Computationele immuunscores suggereerden dat tumoren met hoge IGFL4 mogelijk beter reageren op moderne immuuntherapieën die immuunremmers blokkeren, wat aangeeft dat IGFL4 kan helpen bij het identificeren van patiënten die goede kandidaten zijn voor deze behandelingen.
Een klein RNA dat tegenwerkt
De studie bracht ook een tegenwicht aan dit kankerversterkende pad aan het licht. Door microRNA- en genexpressie in patiëntgegevens te correleren, identificeerden de auteurs miR-129-5p als een klein RNA dat negatief gekoppeld is aan zowel TRMP als IGFL4. In maagkankercellen verminderde toevoeging van miR-129-5p de IGFL4-niveaus en vertraagde de groei, terwijl blokkering van miR-129-5p IGFL4 verhoogde en de proliferatie versnelde. Een andere kandidaat-microRNA, miR-4739, had geen meetbaar effect op IGFL4 en werd uitgesloten. Deze resultaten ondersteunen een regulatoir keten waarin TRMP en TRMP-S, miR-129-5p en IGFL4 een netwerk vormen dat fijnregelt hoe agressief maagkankercellen groeien en hoe ze met hun omgeving interageren.
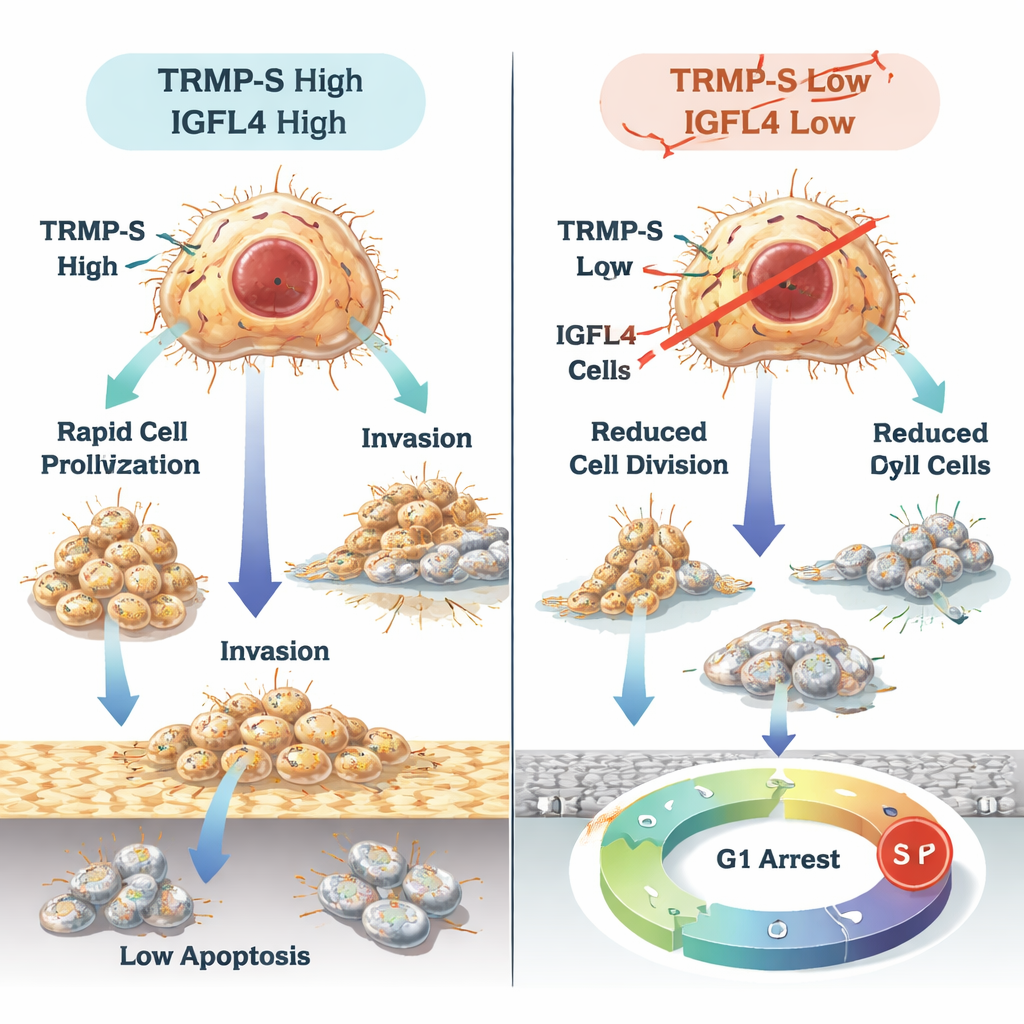
Wat dit voor patiënten zou kunnen betekenen
In eenvoudige bewoordingen toont dit werk aan dat TRMP en TRMP-S als regisseurs achter de schermen fungeren die IGFL4 inschakelen en maagkankercellen helpen groeien, zich verspreiden en natuurlijke remmechanismen ontwijken. Tegelijkertijd fungeert het kleine RNA miR-129-5p als rem op IGFL4, en helpt IGFL4 zelf bepalen hoe immuuncellen zich rond tumoren verzamelen en hoe goed therapieën die het immuunsysteem activeren kunnen werken. Hoewel meer onderzoek en klinische testen nodig zijn, vormen TRMP, TRMP-S, IGFL4 en miR-129-5p samen een veelbelovende set markers voor prognose en potentiële nieuwe doelwitten voor middelen die gericht zijn op het vertragen of stoppen van maagkanker.
Bronvermelding: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Trefwoorden: maagkanker, lange niet-coderende RNA, TRMP, IGFL4, tumormicro-omgeving