Clear Sky Science · nl
Identificatie van RBX1 als regulator van LIPT1-transcriptie en de rol ervan bij koper-geïnduceerde celdood in GBM-cellen
Waarom koper en hersentumoren ertoe doen
Glioblastoma multiforme is een van de dodelijkste vormen van hersenkanker; de meeste patiënten overleven ondanks agressieve chirurgie, bestraling en chemotherapie kort na de diagnose. Deze studie onderzoekt een onverwachte bondgenoot tegen deze tumoren: het metaal koper. De onderzoekers bestuderen een recent herkende vorm van celdood die door koper wordt getriggerd en identificeren een moleculaire route die artsen mogelijk kunnen benutten om tumoren te verzwakken en potentiëel het immuunsysteem te helpen bij de aanval op kankercellen.
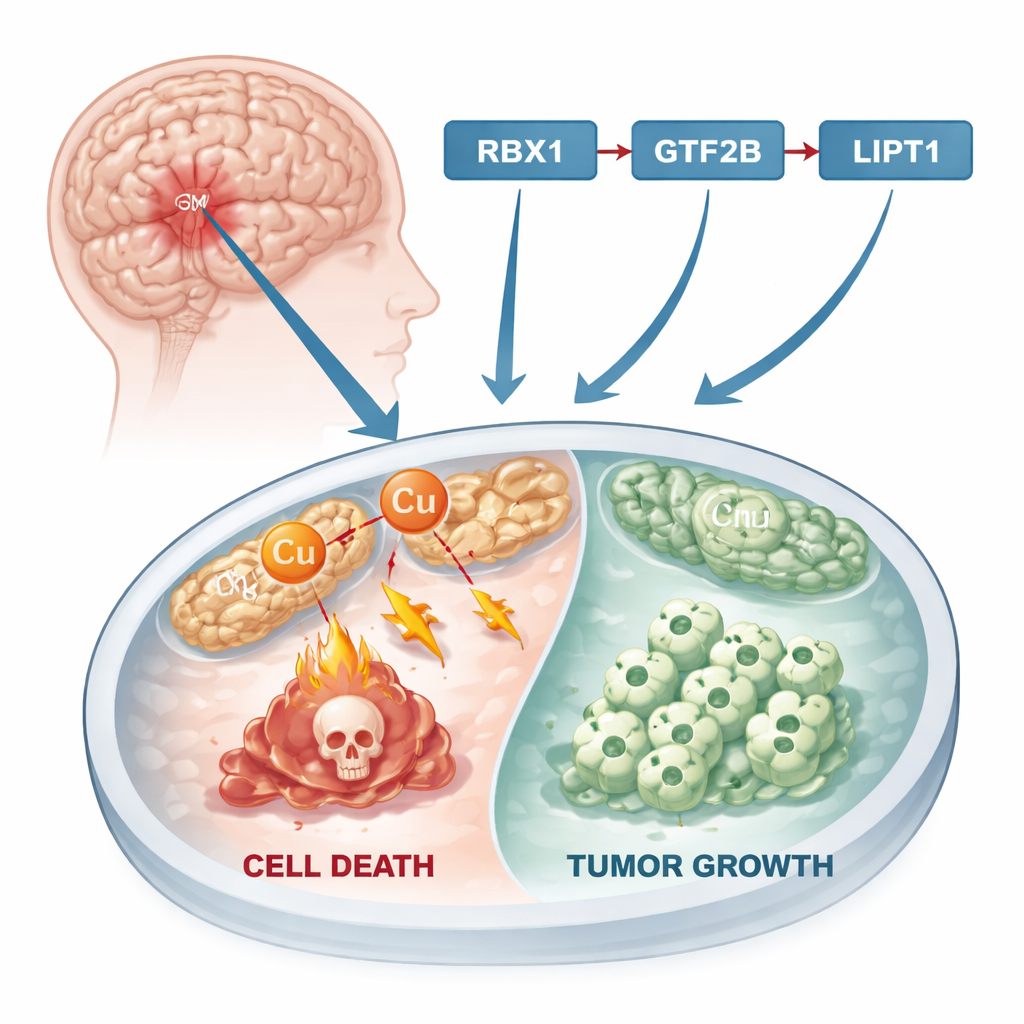
Een nieuwe manier waarop cellen kunnen sterven
Decennialang richtte kankeronderzoek zich op bekende vormen van celdood zoals apoptose, waarbij beschadigde cellen zichzelf rustig uitschakelen. Recent ontdekten wetenschappers een andere route die koper-geïnduceerde celdood wordt genoemd, of “cuproptose.” In dit proces hoopt zich te veel koper op in de energiecentrales van de cel, de mitochondriën. Daar verstoort het belangrijke eiwitten, waardoor toxische klonten ontstaan die uiteindelijk de cel doden. Omdat veel tumoren een veranderd metaalmetabolisme en hogere koperconcentraties hebben dan normaal weefsel, biedt cuproptose een potentiële kwetsbaarheid: als onderzoekers kankercellen in de richting van deze koper-gedreven ondergang kunnen duwen, zouden ze de groei van de tumor kunnen vertragen of stoppen.
Focus op een sleutelgen in glioblastoom
De auteurs begonnen met het onderzoeken van een groep genen die al bekendstaan als betrokken bij cuproptose en vroegen hoe deze zich gedragen in glioblastoommonsters vergeleken met normaal hersenweefsel. Eén gen sprong er met name uit: LIPT1. Het was actiever in glioblastoomweefsel en in verschillende glioblastoomcelijn dan in normale hersencellen. Belangrijk is dat patiënten wiens tumoren hogere LIPT1-activiteit hadden, geneigd waren langer vrij te blijven van terugkeer van de kanker na behandeling. Hoge LIPT1-niveaus waren ook gelinkt aan een grotere aanwezigheid van CD8-T-cellen, de voorhoede van het immuunsysteem tegen kanker, wat suggereert dat dit gen kan helpen de tumoromgeving vatbaarder te maken voor immuunaanvallen.
Wat er gebeurt als de koper-doodschakelaar wordt gedimd
Om te testen of LIPT1 daadwerkelijk invloed heeft op koper-gedreven celdood, stelden de onderzoekers glioblastoomcellen bloot aan een koperdragende geneesmiddelcombinatie die betrouwbaar cuproptose opwekt. Vervolgens gebruikten ze genetische middelen om LIPT1-niveaus te verlagen. Wanneer LIPT1 werd geremd, werden tumorcellen resistenter tegen koper-geïnduceerde doding, overleefden ze beter en toonden ze sterkere migratie- en invasiecapaciteiten — gedragingen die samenhangen met agressievere kanker. In gemengde kweek van tumorcellen en menselijke CD8-T-cellen verminderde de verlaging van LIPT1 ook de afgifte van immuunsignaalmoleculen en werd het voor T-cellen moeilijker de kankercellen te vernietigen. Samen wijzen deze experimenten erop dat LIPT1 de gevoeligheid voor koper-geïnduceerde celdood vergroot en anti-tumor immuunactiviteit ondersteunt.
De commandoketen volgen tot aan RBX1
De volgende uitdaging was te begrijpen waarom LIPT1 in glioblastoom omhoog is. Door verschillende grote gen- en proteïne-databases te combineren, identificeerden de onderzoekers een transcriptiefactor — een soort hoofdschakelaar voor genactiviteit — genaamd GTF2B die nabij het LIPT1-gen bindt en waarschijnlijk de expressie ervan versterkt. Vervolgens vroegen ze wat GTF2B zelf reguleert. Een tweede eiwit, RBX1, kwam naar voren als sterke kandidaat. RBX1 maakt deel uit van het cellulaire label- en verwijderingssysteem dat andere eiwitten markeert voor afbraak. In glioblastoomcellen waren de RBX1-niveaus lager dan in normale hersencellen, terwijl GTF2B en LIPT1 hoger waren. Laboratoriumassays toonden aan dat RBX1 kleine ‘vernietig mij’-labels aan GTF2B kan bevestigen, wat leidt tot diens afbraak; wanneer RBX1 toenam, daalden GTF2B-niveaus en LIPT1-activiteit, en het blokkeren van het afbraaksysteem van de cel keerde dit effect om.
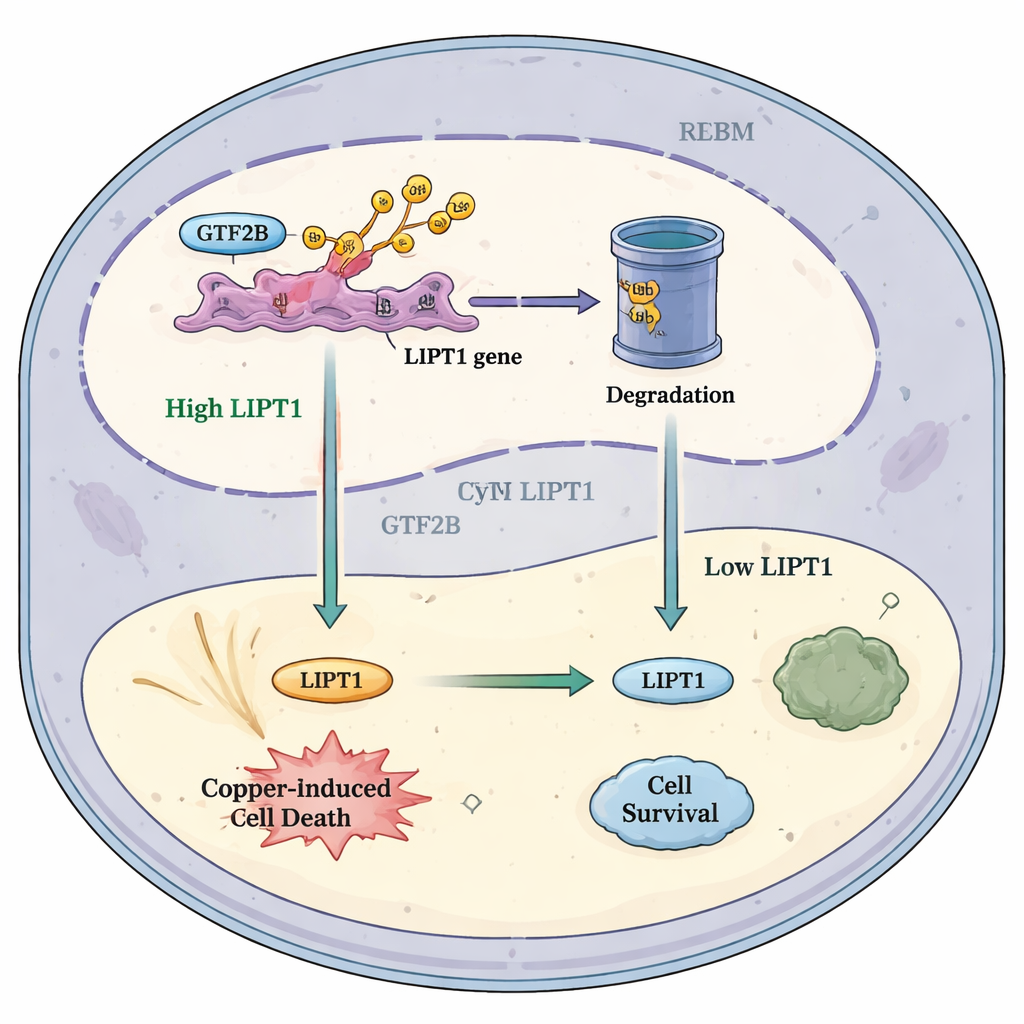
Hoe deze route toekomstige behandelingen zou kunnen helpen
Samenvattend stellen de auteurs een eenvoudig model voor: onder gezonde omstandigheden houdt RBX1 GTF2B in toom en beperkt hoe sterk het het LIPT1-gen activeert. In glioblastoom betekent verminderde RBX1 minder afbraak van GTF2B. Extra GTF2B verhoogt vervolgens LIPT1, waardoor tumorcellen gevoeliger worden voor koper-geïnduceerde celdood en er meer kankerbestrijdende immuuncellen worden aangetrokken. Dit model suggereert dat het zorgvuldig afstemmen van de RBX1–GTF2B–LIPT1-route, mogelijk in combinatie met koper-gerichte geneesmiddelen en immunotherapieën, de balans in hersentumoren naar zelfvernietiging zou kunnen kantelen. Hoewel er nog veel werk nodig is voordat dit idee patiënten bereikt, benadrukt de studie een veelbelovende kruising tussen metaalbiologie, genregulatie en kankerimmunologie die nieuwe therapeutische wegen zou kunnen openen voor een van de hardnekkigste vormen van kanker.
Bronvermelding: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Trefwoorden: glioblastoom, koper-geïnduceerde celdood, LIPT1, tumorimmunologie, RBX1-route