Clear Sky Science · nl
Integratie van machine learning en fysica-gebaseerde modellering voor predictief ontwerp van gemcitabine-beladen nanocomposieten
Slimmere kankertherapieën door ontwerp
Kankergeneesmiddelen zoals gemcitabine kunnen levens redden, maar gedragen zich vaak meer als botte instrumenten dan als precisie-instrumenten: ze worden snel afgebroken, missen hun doel en veroorzaken ernstige bijwerkingen. Deze studie onderzoekt hoe computers onderzoekers kunnen helpen nieuwe, kleine medicijndragers eerst digitaal te testen in plaats van alleen in het laboratorium, om gemcitabine-behandelingen effectiever, langduriger en mogelijk veiliger voor patiënten te maken.
Waarom kleine dragers ertoe doen
Traditionele chemotherapie overspoelt het lichaam met medicijnmoleculen die overal circuleren, niet alleen in tumoren. Nanocomposieten — ontworpen deeltjes duizenden keren kleiner dan een zandkorrel — bieden een manier om gemcitabine te verpakken zodat het in de bloedbaan wordt beschermd en gerichter bij kankercellen terechtkomt. Twee grootheden bepalen grotendeels of een ontwerp bruikbaar is. De laad-efficiëntie geeft aan hoeveel geneesmiddel er in elk deeltje terechtkomt, terwijl de encapsulatie-efficiëntie meet welk deel van het begingeneesmiddel succesvol wordt ingesloten in plaats van verspild. Hoge waarden voor beide betekenen minder injecties, minder draagermateriaal en een grotere kans om de tumor hard te treffen zonder de rest van het lichaam te overbelasten.
Van proef-en-fout naar datagestuurd ontwerp
Het met de hand ontwerpen van deze nanodragers is als het proberen af te stemmen van een radio met honderden knoppen—deeltjesgrootte, oppervlakte-lading, materialen, coatings en bereidingsmethoden werken allemaal complex samen. Tot nu toe varieerden onderzoekers meestal één of twee instellingen tegelijk en maten het resultaat, een langzaam en duur proces dat slechts een klein deel van het totale plaatje blootlegt. In dit werk verzamelden de auteurs 59 zorgvuldig gecontroleerde recepturen voor gemcitabine-nanodragers uit de wetenschappelijke literatuur en verrijkten die met extra, fysica-gebaseerde voorbeelden die op de computer werden gegenereerd. Deze gecombineerde dataset stelde hen in staat meerdere machine learning-benaderingen te testen—computerprogramma’s die patronen uit gegevens leren—om laad- en encapsulatie-efficiënties te voorspellen op basis van de ontwerpkiezen alleen.
De algoritmen laten sturen door fysica
De meeste machine learning-systemen zijn krachtige curve-fitters: ze kunnen patronen herkennen maar weten niet wanneer een antwoord de natuurwetten zou schenden. Om onrealistische voorspellingen te vermijden bouwden de onderzoekers een hybride methode die data mengt met basisfysische regels over hoe geneesmiddelmoleculen bewegen, binden en in evenwicht blijven in een gesloten systeem. In hun kader wordt elke voorspelling die bijvoorbeeld zou impliceren dat er meer geneesmiddel ontstaat dan oorspronkelijk is toegevoegd, of die negeert hoe moleculen door een materiaal diffunderen, tijdens training zacht bestraft. Deze "physics-informed" aanpak stuurt het model richting antwoorden die chemisch en fysisch logisch zijn, vooral in delen van de ontwerpruimte waar echte metingen schaars zijn.
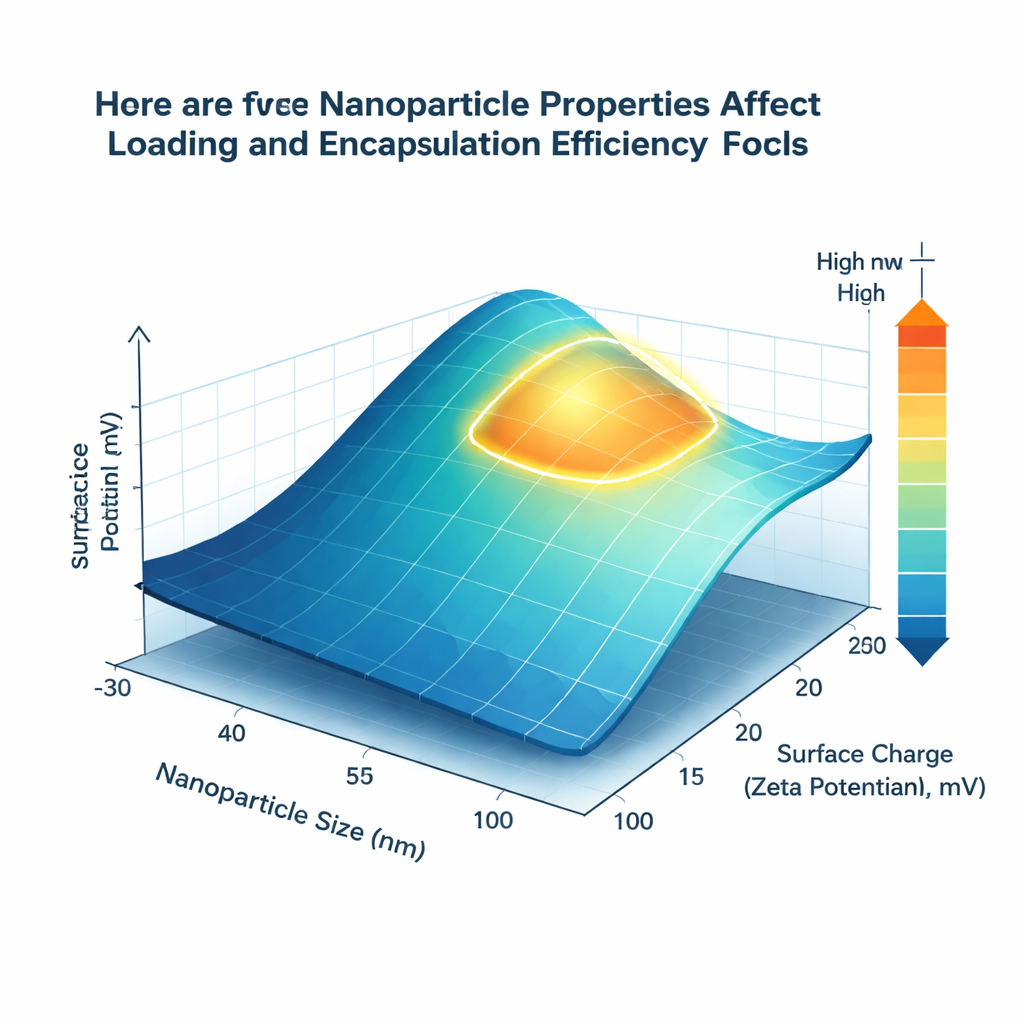
Wat de modellen ontdekten
Van de geteste technieken leverde een geavanceerd ensemble-algoritme genaamd XGBoost de meest accurate voorspellingen, die de gerapporteerde experimentele resultaten voor beide belangrijke efficiënties nauw volgden. Maar naast nauwkeurigheid wilde het team begrijpelijke ontwerprichtlijnen. Met een methode genaamd SHAP, die rangschikt hoe sterk elke factor de voorspelling omhoog of omlaag duwt, ontdekten ze dat deeltjesgrootte en oppervlakte-lading consequent bepalend zijn voor de prestatie. Nanodragers met een diameter van ongeveer 80 tot 150 nanometer boden de beste balans tussen oppervlakte en intern volume, wat zowel laden als encapsulatie bevorderde. Een licht positieve oppervlakte-lading, in het bereik van +15 tot +25 millivolt, hing samen met betere insluiting van gemcitabine, waarschijnlijk omdat positief geladen drageroppervlakken gunstig interageren met de negatief geladen groepen van het middel.
Een digitaal kaartje voor toekomstige kankerbehandelingen
Het eindresultaat is geen afgewerkt medicijn maar een krachtig planningsinstrument. De studie levert een soort "ontwerpkaart" die onderzoekers wijst naar nanodragerrecepten die waarschijnlijk goed in staat zijn gemcitabine vast te houden en te beschermen, terwijl miljoenen weinig veelbelovende combinaties worden vermeden. De auteurs benadrukken dat hun voorspellingen nog moeten worden bevestigd in nieuwe laboratorium- en dierstudies, en dat hun dataset—hoewel zorgvuldig samengesteld—relatief klein van omvang is. Toch toont dit fysica-bewuste machine learning-kader hoe computers kunnen helpen de zoektocht naar betere dragers voor kankergeneesmiddelen te verkleinen, waardoor kosten dalen en de reis van idee naar preciezere, patiëntvriendelijkere therapieën wordt versneld.
Bronvermelding: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Trefwoorden: nanomedicijn, gemcitabine, geneesmiddelafgifte, machine learning, nanodeeltjes