Clear Sky Science · nl
MCT1 als cruciale regulator van insulinesignaalering, energiebalans en podocytfunctie
Waarom de brandstofkeuze van niercellen ertoe doet
Onze nieren filteren elke dag ongemerkt honderden liters bloed, en een groot deel van dat werk berust op kleine cellen die podocyten worden genoemd en die zich om de nierschijfjes heen vouwen. Deze cellen moeten zich voortdurend herschikken om eiwitten in het bloed te houden en afvalstoffen in de urine. Deze studie onderzoekt hoe podocyten aan hun energie komen, wat er gebeurt als een van hun belangrijkste "brandstofdeuren" wordt geblokkeerd, en waarom dat relevant kan zijn voor veelvoorkomende aandoeningen zoals diabetes en nierziekte. 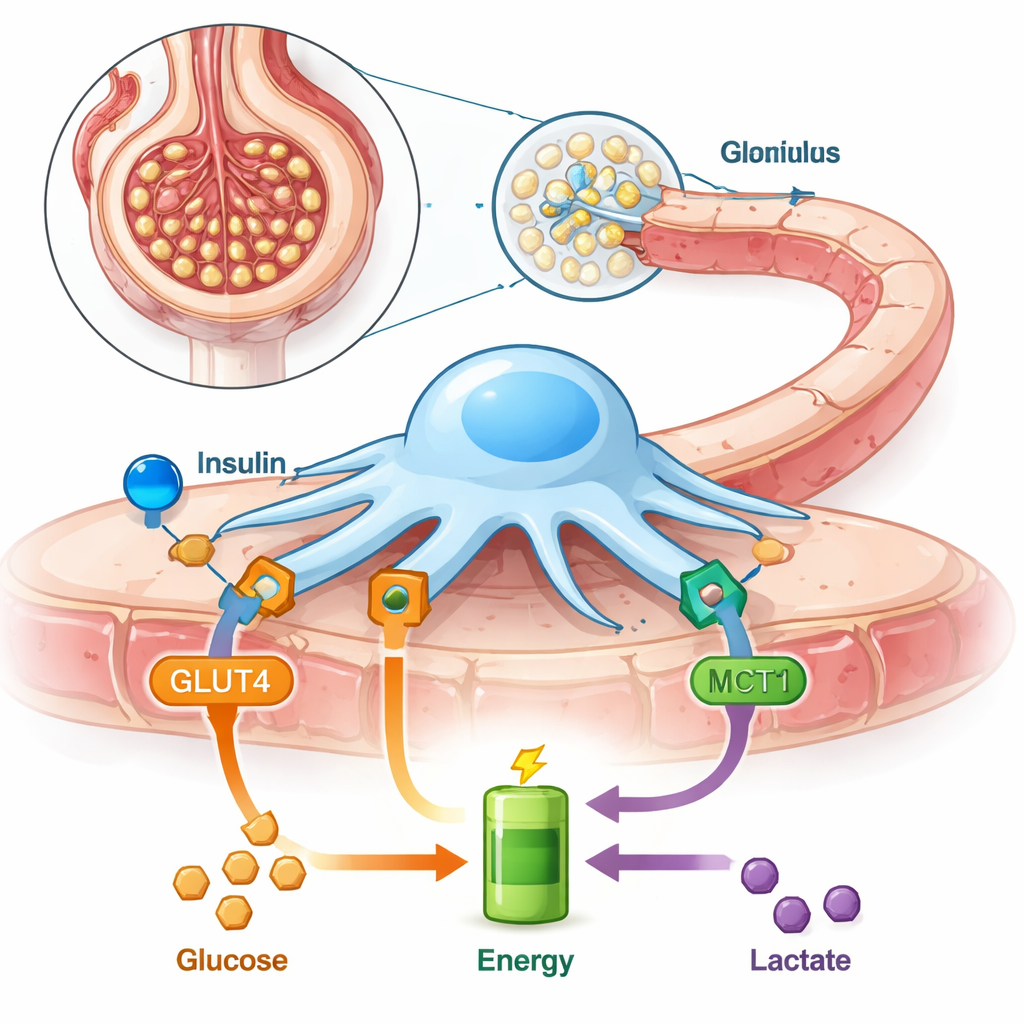
Poortwachters bij het filter
Podocyten bevinden zich aan de buitenkant van elk nierfilter en sturen fijne, voetachtige uitlopers uit die in elkaar grijpen om een laatste barrière te vormen voordat urine wordt geproduceerd. Omdat ze voortdurend hun vorm aanpassen, verbruiken ze veel energie. In tegenstelling tot veel andere cellen vertrouwen podocyten sterk op het afbreken van suiker zonder zuurstof (een route genaamd glycolyse) en reageren ze bijzonder sterk op insuline, dat hen aanzet om meer suiker uit het bloed te halen via een transporter genaamd GLUT4. De auteurs hadden eerder laten zien dat podocyten ook op lactaat kunnen draaien, een klein molecuul dat vaak als "afval" wordt afgedaan, wat erop wijst dat deze cellen flexibeler zijn dan ooit werd gedacht.
De lactaatdeur: MCT1
Lactaat verplaatst zich in en uit cellen via speciale transporteiwitten. Een van de belangrijkste is monocarboxylaattransporter 1 (MCT1), die lactaat in cellen kan brengen zodat het als brandstof kan worden verbrand. In deze studie gebruikten onderzoekers met ratpodocyten gekweekt in schaaltjes een chemische remmer om MCT1 te blokkeren. Ze onderzochten vervolgens hoe dit de werking van insuline op glucose-opname beïnvloedde, hoeveel energie de cellen konden produceren, hoe hun interne steigerwerk eruitzag en hoe "lekt" het filter werd voor een groot bloedeiwit genaamd albumine. Ze testten ook gehele geïsoleerde nierfilters (glomeruli) van ratten om te zien hoe lactaat en het blokkeren van MCT1 de eiwitlekkage in een meer intact systeem veranderden.
Als de brandstofdeur sluit
Het blokkeren van MCT1 had verschillende opvallende effecten. Ten eerste verminderde het de hoeveelheid glucose die podocyten opnamen, zowel in rusttoestand als na insuline-stimulatie, en verzwakte het een belangrijke schakel in het insulinepad (een eiwit genaamd Akt) zonder de insulinereceptor zelf te verstoren. Tegelijkertijd werd de normale herschikking van de GLUT4-transporter naar het celoppervlak afgezwakt. Metingen van de cellulaire stofwisseling lieten zien dat de totale energieproductie daalde wanneer MCT1 werd geblokkeerd, en dat de cellen verschoven van glycolyse naar meer zuurstofafhankelijke verbranding in de mitochondriën. Zelfs wanneer insuline of lactaat werd toegevoegd, werd dit energietekort niet volledig gecorrigeerd, wat suggereert dat MCT1 centraal staat in hoe podocyten hun energiemix reguleren. 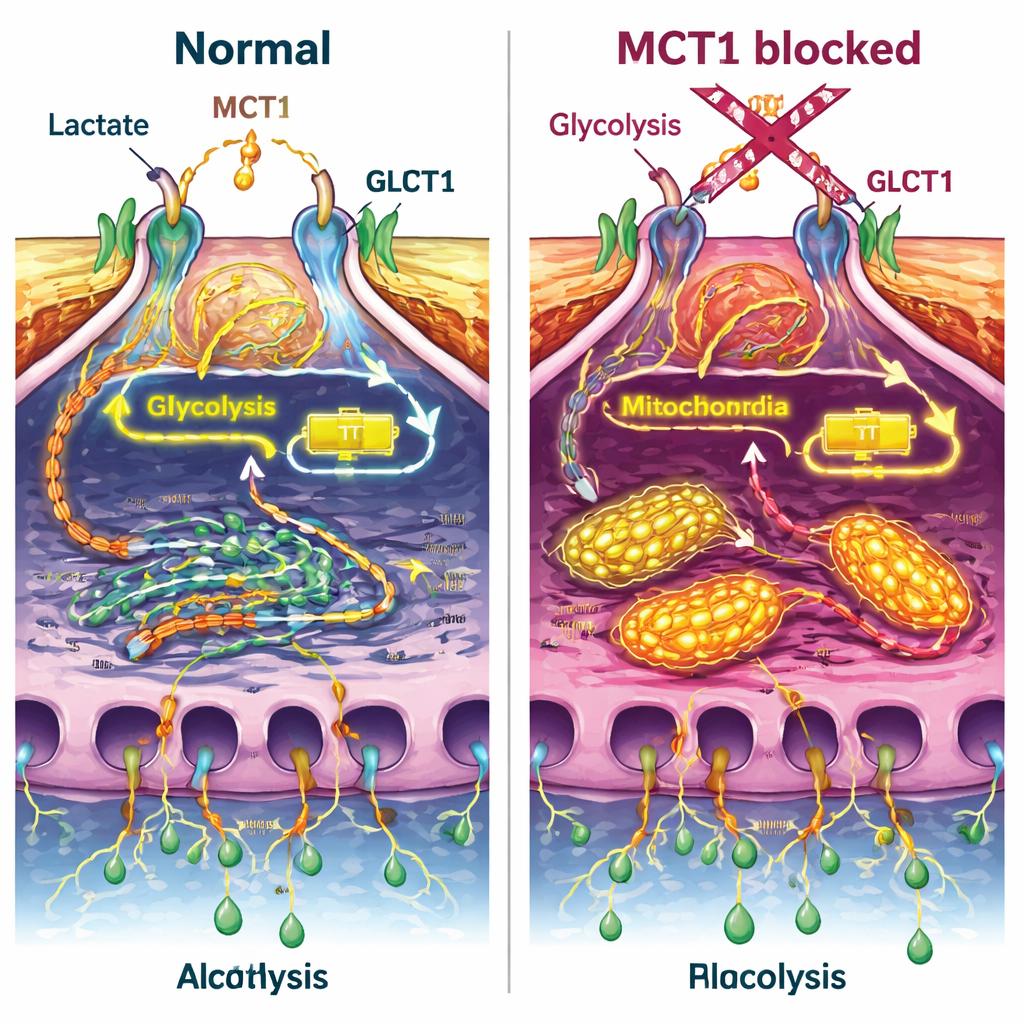
Lekkende filters en gestreste steigers
Energieveranderingen stonden sterk in verband met fysieke schade. Wanneer MCT1 werd geblokkeerd, lieten podocytlagen in kweek meer albumine door, vergelijkbaar met het effect van alleen insuline. Ook lactaat zelf maakte de barrière lekkender, en het combineren van lactaat of insuline met MCT1-blokkade hield de permeabiliteit hoog. Binnenin de cellen raakten de actinevezels die hun vorm bepalen meer gebundeld en gedesorganiseerd, een patroon dat geassocieerd is met verlies van de fijne voetprocessen die het filter vormen. Een ander belangrijk eiwit, nephrin, dat helpt het filter bij elkaar te houden en ook de werking van insuline ondersteunt, was verminderd of verkeerd gelokaliseerd wanneer MCT1 werd geremd. In geïsoleerde gehele filters uit ratnieren verhoogde toevoeging van lactaat snel de albuminelekkage, en MCT1-blokkade gaf een vergelijkbare toename, wat het idee ondersteunt dat verstoorde lactaathuishouding direct de filterfunctie verzwakt.
Implicaties voor diabetes en niergezondheid
De auteurs stellen dat een correcte doorstroming van lactaat via MCT1 essentieel is voor podocyten om hun voorkeursenergieprogramma te draaien, op insuline te reageren en een strakke filtratiebarrière te behouden. Wanneer deze lactaat-"deur" verstoord is — door blokkering van MCT1 of door chronisch hoge bloedglucose die de lactaatbalans verandert — verliezen podocyten hun metabole flexibiliteit, verbranden ze minder glucose, vertrouwen ze te veel op mitochondriale verbranding en worden ze structureel instabiel en lek. Voor mensen suggereert dit werk dat subtiele veranderingen in hoe niercellen met lactaat omgaan kunnen bijdragen aan insulineresistentie en vroege nierschade, lang voordat de algemene nierfunctie duidelijk afwijkend is. Inzicht in en uiteindelijk het richten op dit lactaattransportsysteem zou nieuwe mogelijkheden kunnen openen om de nierfilters te beschermen bij diabetes en andere metabole ziekten.
Bronvermelding: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Trefwoorden: nierpodocyten, lactaatmetabolisme, insulineresistentie, glomerulaire filtratiebarrière, MCT1-transporter