Clear Sky Science · nl
Geautomatiseerde kwantificatie van tumor-infiltrerende lymfocyten met machine learning onthult prognostische en immunogenomische kenmerken bij longkanker
Waarom het tellen van piepkleine immuuncellen in longtumoren ertoe doet
Longkanker behoort nog steeds tot de dodelijkste vormen van kanker, maar niet alle tumoren gedragen zich hetzelfde. Sommige worden sterk bewaakt door immuuncellen die het tumorweefsel binnendringen, terwijl andere vrijwel onaangetast blijven. Deze tumor-infiltrerende lymfocyten, of TILs, kunnen aanwijzingen geven over het verloop van de ziekte en of een patiënt mogelijk baat heeft bij moderne immunotherapieën. Het probleem is dat TILs momenteel meestal met het blote oog onder de microscoop worden geteld, wat traag en subjectief is. Deze studie stelt een actuele vraag: kunnen we machine learning gebruiken om deze cellen automatisch op routine-pathologievlekken te meten, en wat zegt dat over de biologie van longkanker en het patiëntenoverleven?
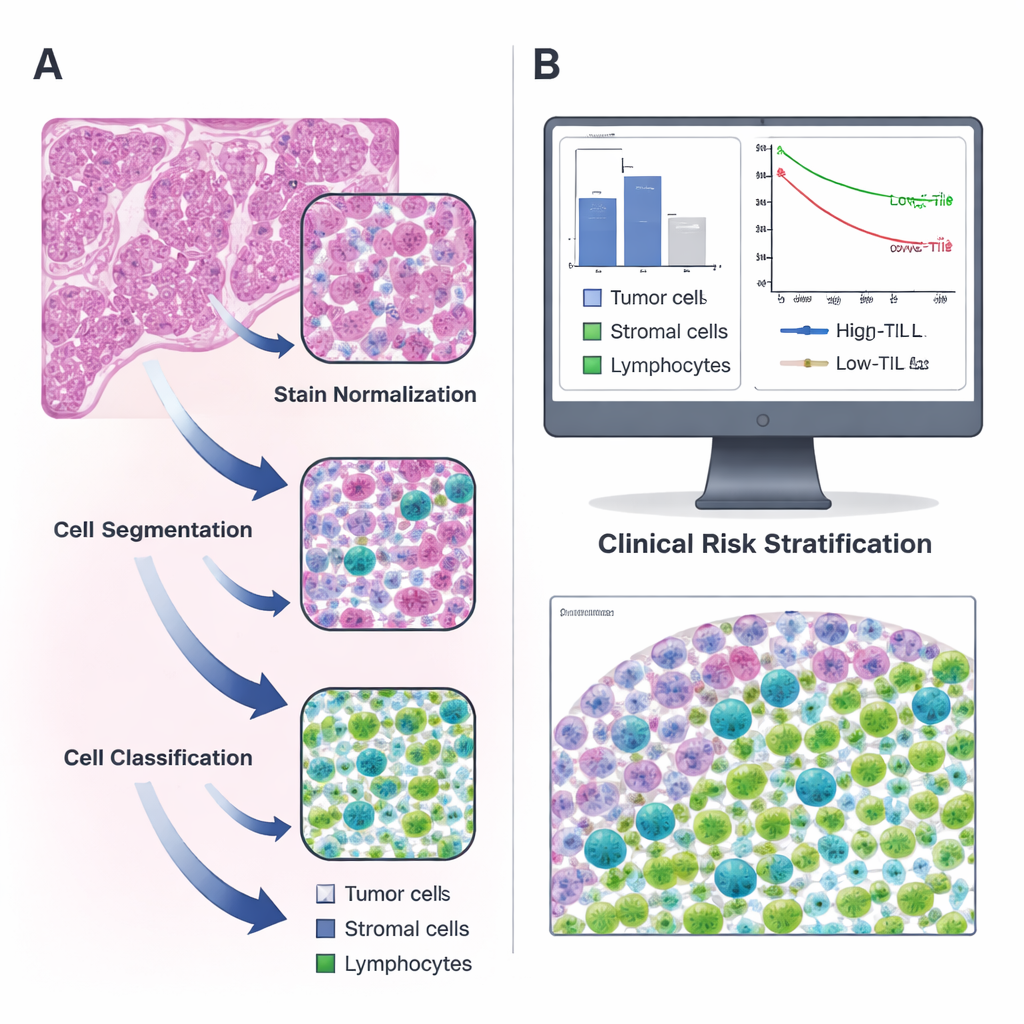
Gewone vlekkjes omzetten in digitale kaarten
De onderzoekers concentreerden zich op longadenocarcinoom, een veelvoorkomend type longkanker, en gebruikten publieke gegevens van The Cancer Genome Atlas naast een onafhankelijke patiëntenserie uit hun eigen ziekenhuis. Voor elke patiënt analyseerden ze standaard hematoxyline‑ en eosine (H&E)‑gekleurde weefselvlekken, die roze‑paarse beelden die elke patholoog goed kent. Met de open‑source software QuPath bouwden ze een stapsgewijze pijplijn: eerst corrigeerden ze kleurverschillen tussen vlekken; vervolgens gebruikten ze een watershed‑algoritme om overlappende celkernen van elkaar te scheiden; tenslotte labelde een getrainde computercalssificator elke gedetecteerde cel als tumor, steunend weefsel (stroma) of lymfocyt. Twee ervaren pathologen controleerden en corrigeerden herhaaldelijk het werk van de machine totdat deze betrouwbaar de verschillende celtypen zelfstandig herkende.
Immuuncellen koppelen aan patiëntenuitkomst
Zodra het systeem cellen met vertrouwen kon identificeren, berekenden de onderzoekers hoeveel lymfocyten er per vierkante millimeter tumormateriaal aanwezig waren voor meer dan 300 patiënten. Ze vonden dat TIL‑niveaus sterk varieerden en gemiddeld slechts een klein deel van alle cellen uitmaakten. Met een statistische methode om de meest informatieve drempel te vinden, kozen ze 135 TILs per vierkante millimeter als scheidslijn tussen tumoren met “hoog” en “laag” TIL‑gehalte. Patiënten met tumoren boven deze grens leefden langer dan zij met schaarse immuuninfiltratie, en dit patroon hield stand in zowel de originele als de verificatiegroep. Met andere woorden: een eenvoudige waarde, geproduceerd door een geautomatiseerd hulpmiddel, ving betekenisvolle verschillen in overleving op en bevestigde eerdere, arbeidsintensievere studies die handmatig tellen gebruikten.
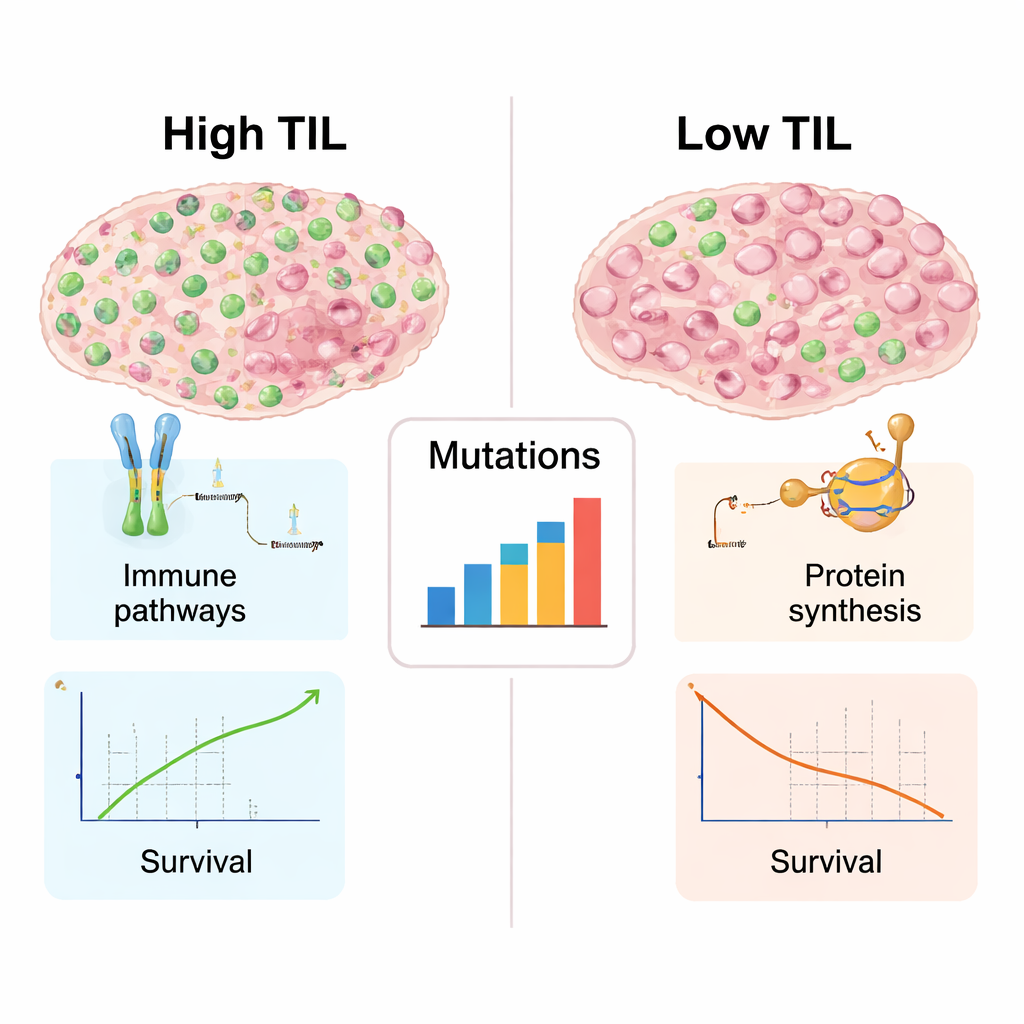
Hoe immuunrijke tumoren er ‘onder de motorkap’ uitzien
Aangezien genetische en moleculaire gegevens beschikbaar waren voor veel van deze tumoren, konden de auteurs onderzoeken wat hoge‑TIL‑ en lage‑TIL‑kankers verder onderscheidde naast eenvoudige celtellingen. Tumoren die vol zaten met lymfocyten vertoonden sterkere handtekeningen van immuunactiviteit: genen betrokken bij het herkennen van abnormale eiwitten, het presenteren daarvan aan T‑cellen en het coördineren van een immuunaanval waren meer actief. Deze tumoren droegen ook een bredere mix van DNA‑mutaties, die nieuwe doelwitten voor het immuunsysteem kunnen creëren. Daarentegen vertoonden lage‑TIL‑tumoren een voorkeur voor genen die gekoppeld zijn aan de opbouw van ribosomen en eiwitsynthese, een teken van intensieve groeimechanismen maar relatief weinig immuunbetrokkenheid. Deze scheiding weerspiegelt het inmiddels bekende contrast tussen “hete” tumoren, rijk aan immuuncellen en waarschijnlijker reagerend op immunotherapie, en “koude” tumoren, die het immuunsysteem grotendeels negeren.
Een computer leren de immuunstatus te voorspellen
Het team ging een stap verder en vroeg of een compacte set beeldkenmerken kon voorspellen of een tumor in de hoge‑ of lage‑TIL‑categorie zou vallen zonder elke lymfocyt expliciet te tellen. Ze vatten subtiele textuurpatronen in de vlekken samen — hoe pixelintensiteiten veranderen binnen kleine buurtjes — in zogenaamde Haralick‑kenmerken, en combineerden deze met het klinische stadium van de tumor in een random forest‑model. In kruisvalidatie scheidde deze classifier hoge‑ van lage‑TIL‑tumoren met hoge nauwkeurigheid, en hij behield redelijke prestaties in een onafhankelijke ziekenhuiscohort. Belangrijk is dat de hele aanpak op standaardcomputers draait met vrij beschikbare software, wat suggereert dat veel pathologielabs het in principe kunnen overnemen zonder gespecialiseerde hardware.
Wat dit betekent voor toekomstige zorg bij longkanker
Voor niet‑specialisten is de kernboodschap dat een computer kan leren routinevlekken van longkanker te lezen op een manier die weergeeft hoe sterk het immuunsysteem de tumor is aangegaan. Hoge niveaus van infiltrerende lymfocyten duiden op een actievere immuunreactie, een rijker mutatielandschap en betere overleving. Hoewel meer onderzoek nodig is — vooral bij patiënten die daadwerkelijk immuuntherapie kregen — zou deze geautomatiseerde methode artsen uiteindelijk kunnen helpen tumoren snel en consequent in immuun “heet” of “koud” in te delen. Dat kan weer beslissingen sturen over wie het meeste baat heeft bij immuunbehandelingen en nieuwe strategieën stimuleren om koude tumoren heet te maken.
Bronvermelding: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Trefwoorden: longadenocarcinoom, tumor-infiltrerende lymfocyten, machine learning, digitale pathologie, kankerimmunotherapie