Clear Sky Science · nl
Geautomatiseerde diagnose van Plus-vorm en vroege stadia van ROP met deep learning-modellen
Waarom kleine oogjes en slimme computers ertoe doen
Ieder jaar lopen duizenden te vroeg geboren baby’s het risico hun gezichtsvermogen te verliezen omdat de bloedvaten achter in hun ogen zich niet normaal ontwikkelen—een aandoening die retinopathie van prematuriteit (ROP) wordt genoemd. Het vroegtijdig opsporen van dit probleem kan het gezichtsvermogen redden, maar vereist frequente oogonderzoeken door hoogopgeleide specialisten—deskundigen die in veel delen van de wereld schaars zijn. Deze studie onderzoekt hoe moderne kunstmatige intelligentie (AI) artsen kan helpen vroegtijdige waarschuwingssignalen in retinafoto’s te herkennen, en zo mogelijk screening op expertniveau kan brengen naar ziekenhuizen en klinieken zonder gespecialiseerde oogzorg.
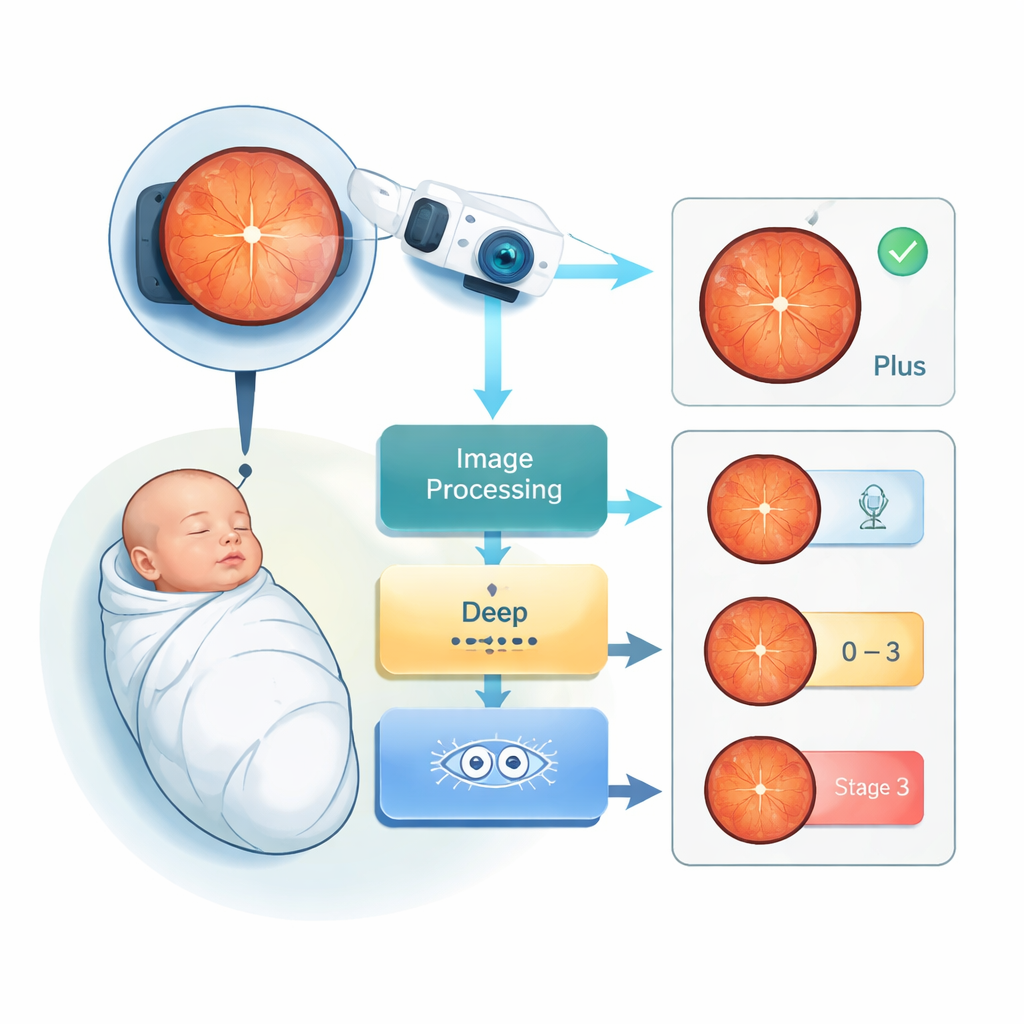
Het probleem: kwetsbaar zicht bij de allerkleinsten
ROP ontstaat wanneer vroeggeboorte de normale groei van bloedvaten in het netvlies, de lichtgevoelige laag achter in het oog, onderbreekt. Baby’s die zeer vroeg geboren zijn of een zeer laag geboortegewicht hebben, lopen het grootste risico. In milde gevallen herstelt het oog vanzelf. In ernstige gevallen kunnen abnormale vaten aan het netvlies trekken en permanente blindheid veroorzaken. Wereldwijd leidt ROP naar schatting tot ongeveer 50.000 blinde mensen, vooral in regio’s waar de neonatale zorg de overleving heeft verbeterd, maar screeningsprogramma’s en specialisten voor ogen niet gelijke tred hielden. De huidige screening is arbeidsintensief, kostbaar en subjectief: twee experts kunnen het soms oneens zijn over hoe ernstig de aandoening van een baby werkelijk is.
Waar artsen op letten: gedraaide vaten en vroege stadia
Oogartsen beoordelen ROP aan de hand van twee hoofdkenmerken in retinabeelden. Ten eerste de algemene fase van de ziekte, van Fase 0 (geen zichtbare veranderingen) tot de vroege probleemstadia (1–3). Ten tweede de zogenaamde “Plus disease”, een waarschuwingssignaal waarbij bloedvaten op het netvlies ongewoon verwijd en gedraaid zijn. Plus disease duidt op een hoger risico op ernstige schade en leidt vaak tot behandeling zoals lasertherapie of injecties. Het beoordelen van deze kenmerken met het blote oog is uitdagend, vooral wanneer beelden wazig zijn of wanneer zuigelingen week na week opnieuw onderzocht moeten worden. Een systeem dat automatisch Plus disease kan signaleren en het ROP-stadium uit beelden kan inschatten, zou een krachtig hulpmiddel voor clinici zijn.
Hoe de AI ziet: vaatlijnen traceren in oogfoto’s
De onderzoekers bouwden een tweestaps-AI-pijplijn met meer dan 6.000 retinafoto’s van 188 zuigelingen. Eerst trainden ze een neuraal netwerk om een nauwkeurige “vaatkaart” van elk netvlies te tekenen, waarbij elk zichtbaar bloedvat, zelfs de fijnste vertakkingen, werd gemarkeerd. Van meerdere concurrerende beeldverwerkingsmodellen bleek een variant genaamd U-Net++ het beste in het vastleggen van gedetailleerde vaatpatronen, vooral in ruisige of laagcontrastbeelden. Om de duidelijkheid te verbeteren, versterkte het team elke foto met contrastversterkende filters en ruisreductie voordat segmentatie plaatsvond. Voor de detectie van Plus disease voedden ze vervolgens alleen de vaatkaarten—niet de volledige kleurenfoto’s—naar een tweede neuraal netwerk, omdat Plus disease bijna uitsluitend wordt gedefinieerd door vaathouding en kromming.
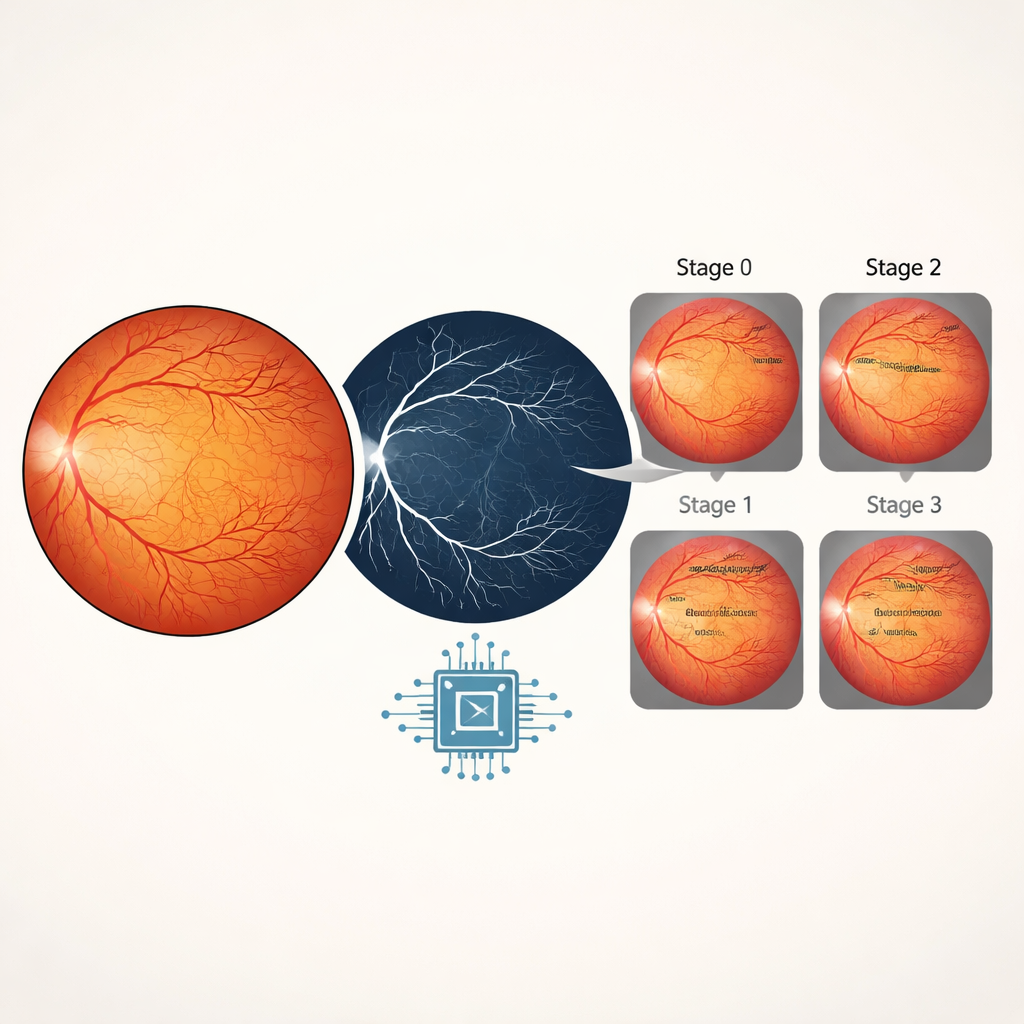
Het netwerk leren de ernst van de ziekte te beoordelen
Voor het bepalen van het ROP-stadium had de AI meer nodig dan alleen de vorm van bloedvaten. Het systeem combineerde daarom de originele kleurretinabeelden met de bijbehorende vaatkaarten, waardoor het model zowel het algemene overzicht van het netvlies als een verscherpt beeld van de vaten kreeg. Het team testte meerdere bekende deep learning-backbones en ontdekte dat een model genaamd EfficientNetB4 de beste balans bood tussen nauwkeurigheid en efficiëntie. Op achtergehouden validatiebeelden behaalde de Plus-detectie een nauwkeurigheid van 99,6 procent, terwijl de stadieclassificatie 98 procent nauwkeurigheid bereikte voor Stadia 0 tot en met 3. Aanvullende controles, inclusief precision–recall-curves en ROC-curves, toonden aan dat het model een hoge sensitiviteit (zelden ziekte missen) en hoge specificiteit (zelden valse alarmen geven) behield, ondanks het feit dat Plus disease veel zeldzamer was dan normale beelden.
In de “zwarte doos” kijken
Aangezien clinici elk hulpmiddel dat behandelingsbeslissingen beïnvloedt moeten vertrouwen, onderzochten de auteurs hoe hun AI tot beslissingen kwam. Met visualisatiemethoden zoals t-SNE toonden ze aan dat beelden uit verschillende klassen (bijvoorbeeld Plus versus Normaal of Fase 1 versus Fase 3) goed gescheiden clusters vormden in de interne featurespace van het model. Met heatmap-technieken zoals Grad-CAM benadrukten ze welke delen van elk netvlies de voorspelling het sterkst beïnvloedden. Voor Plus disease concentreerde het model zich op gebieden waar vaten abnormaal breed of gedraaid waren, wat overeenkomt met waar experts op letten. Voor het stadieoordeel besteedde het model ook aandacht aan andere regio’s zoals de oogzenuwschijf en macula, wat suggereert dat de redenatie nauw aansluit bij gevestigde medische criteria en niet op toevallige beeldartefacten berustte.
Wat dit betekent voor baby’s en klinieken
Simpel gezegd laat dit werk zien dat een zorgvuldig ontworpen AI-systeem retinafoto’s van te vroeg geboren zuigelingen met bijna-expertniveau kan lezen, zowel om gevaarlijke vaatveranderingen te detecteren als om in te schatten hoe ver de ziekte gevorderd is. De studie werd uitgevoerd in één medisch centrum en omvatte alleen vroege tot matige stadia, dus grotere multicenterproeven en gegevens van meer gevorderde gevallen zijn nog nodig. De resultaten wijzen er echter op dat, met verdere validatie en zorgvuldige integratie in telemedicine-platforms, zulke hulpmiddelen overbelaste zorgsystemen kunnen helpen veel meer zuigelingen consistenter en goedkoper te screenen. Dat kan vroegere behandeling betekenen en een grotere kans om het gezichtsvermogen te behouden voor enkele van de meest kwetsbare patiënten in de neonatale zorg.
Bronvermelding: Vahidmoghadam, M., Ghorbani, P., Ahmadi, M.J. et al. Automated diagnosis of plus form and early stages of ROP using deep learning models. Sci Rep 16, 7234 (2026). https://doi.org/10.1038/s41598-026-37064-2
Trefwoorden: retinopathie van prematuriteit, kunstmatige intelligentie, deep learning, medische beeldvorming, neonatale oogaandoening