Clear Sky Science · nl
Onderzoek naar het moleculaire mechanisme waarbij celastrol CTNNB1/STAT3 target om uveale melanoom te remmen op basis van netwerkfarmacologie en multi-omics-analyse
Oude geneeskunst ontmoet oogkanker
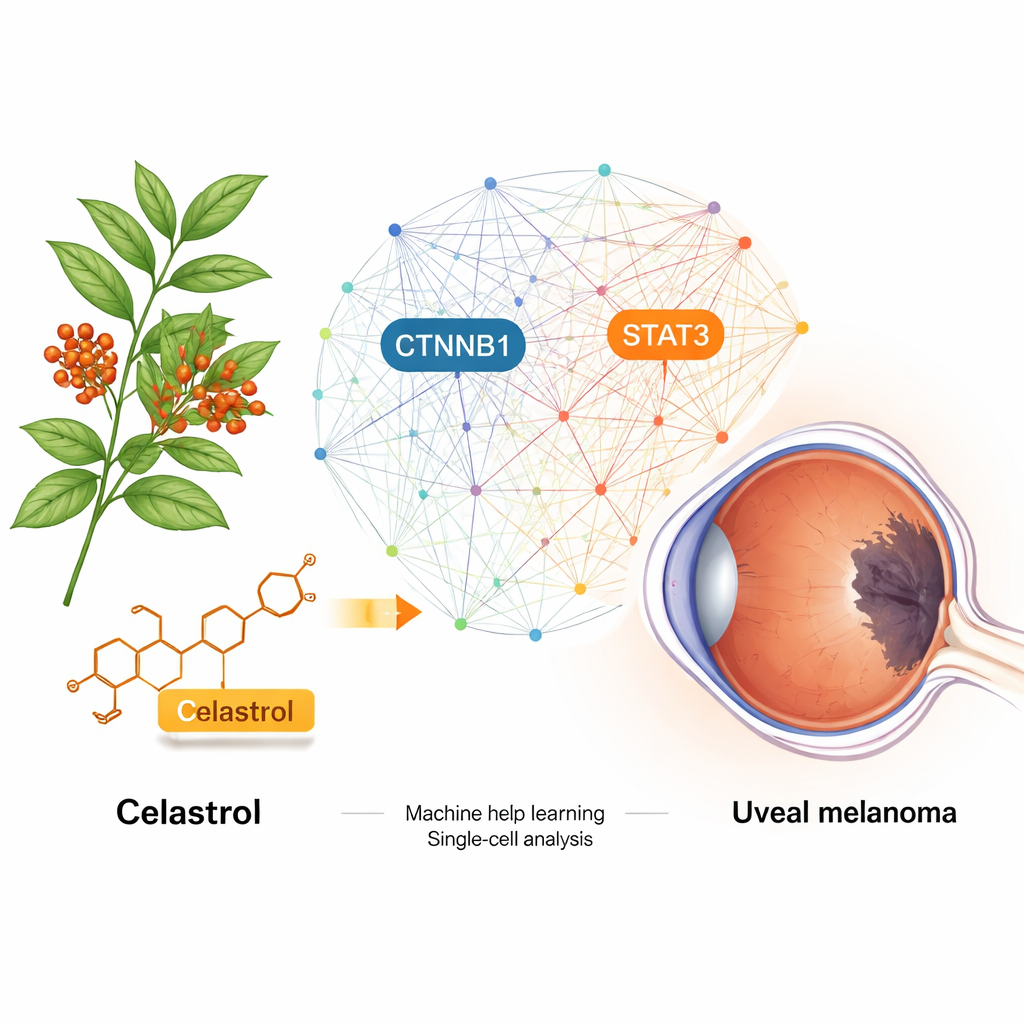
Uveaal melanoom is een zeldzame maar dodelijke kanker die zich binnenin het oog ontwikkelt. Zodra deze uitzaait, veranderen de huidige behandelingen weinig aan de uitkomst. Deze studie onderzoekt of celastrol — een molecule gewonnen uit een traditioneel Chinees geneeskrachtig plant — mogelijk herbestemd kan worden om deze kanker te bestrijden. Door big-data-biologie, computersimulaties en laboratoriumexperimenten te combineren, onthullen de onderzoekers hoe celastrol belangrijke moleculaire schakelaars kan uitschakelen die uveale melanoom helpen groeien en zich verspreiden.
Wat deze oogovertuiging zo gevaarlijk maakt
Uveaal melanoom is de meest voorkomende primaire oogkanker bij volwassenen, en ongeveer de helft van de patiënten ontwikkelt uiteindelijk metastasen, meestal in de lever. In dat stadium wordt overleving vaak in maanden gemeten. Standaardbehandelingen zoals chirurgie, bestraling en lokale therapieën kunnen de primaire oogtumor onder controle houden, maar systemisch toegediende geneesmiddelen hebben beperkte successen geboekt en kunnen ernstige bijwerkingen veroorzaken. Wetenschappers zoeken daarom naar medicijnen die zowel tumorgroei kunnen remmen als beter worden verdragen — een gebied waarin natuurlijke producten zoals celastrol veel belangstelling trekken.
Een natuurlijke verbinding onder de microscoop
Celastrol is afkomstig van Tripterygium wilfordii, een plant die al lang gebruikt wordt in de traditionele Chinese geneeskunde. Eerder werk toonde aan dat het de groei van meerdere kankers kan vertragen, maar hoe het in uveaal melanoom zou werken, was onduidelijk. Het team begon met het doorzoeken van talrijke biomedische databases om te voorspellen aan welke menselijke eiwitten celastrol mogelijk kan binden en welke eiwitten sterk gerelateerd zijn aan uveaal melanoom. Bij vergelijking van deze lijsten vonden ze 46 overlappende kandidaten. Met computertools die laten zien hoe eiwitten met elkaar interageren, snoerden ze dit terug tot een handvol “hub”-moleculen die op de knooppunten van belangrijke groeioverlevingsroutes in tumorcellen liggen.
Inzoomen op twee meesterschakelaars
Om de meest cruciale spelers vast te stellen, combineerden de onderzoekers tumorgenexpressiegegevens van patiënten uit The Cancer Genome Atlas met drie verschillende machine-learningmethoden. Alle drie benaderingen kwamen uit op twee genen: CTNNB1, een kerncomponent van de Wnt-signaleringsweg die celgroei aanstuurt, en STAT3, een belangrijke regulator van ontsteking, overleving en immuunontwijking. Verdere analyses van bulk-tumormonsters en single-cell RNA-sequencing toonden aan dat deze genen sterk actief zijn in uveale melanoomcellen, met name in agressievere celsubgroepen, en gekoppeld zijn aan veranderingen in de omringende immuuncellen. Kortom, CTNNB1 en STAT3 leken op meesters schakelaars die de kanker helpen floreren terwijl ze het immuunsysteem op afstand houden.
Van computermodellen naar levende cellen
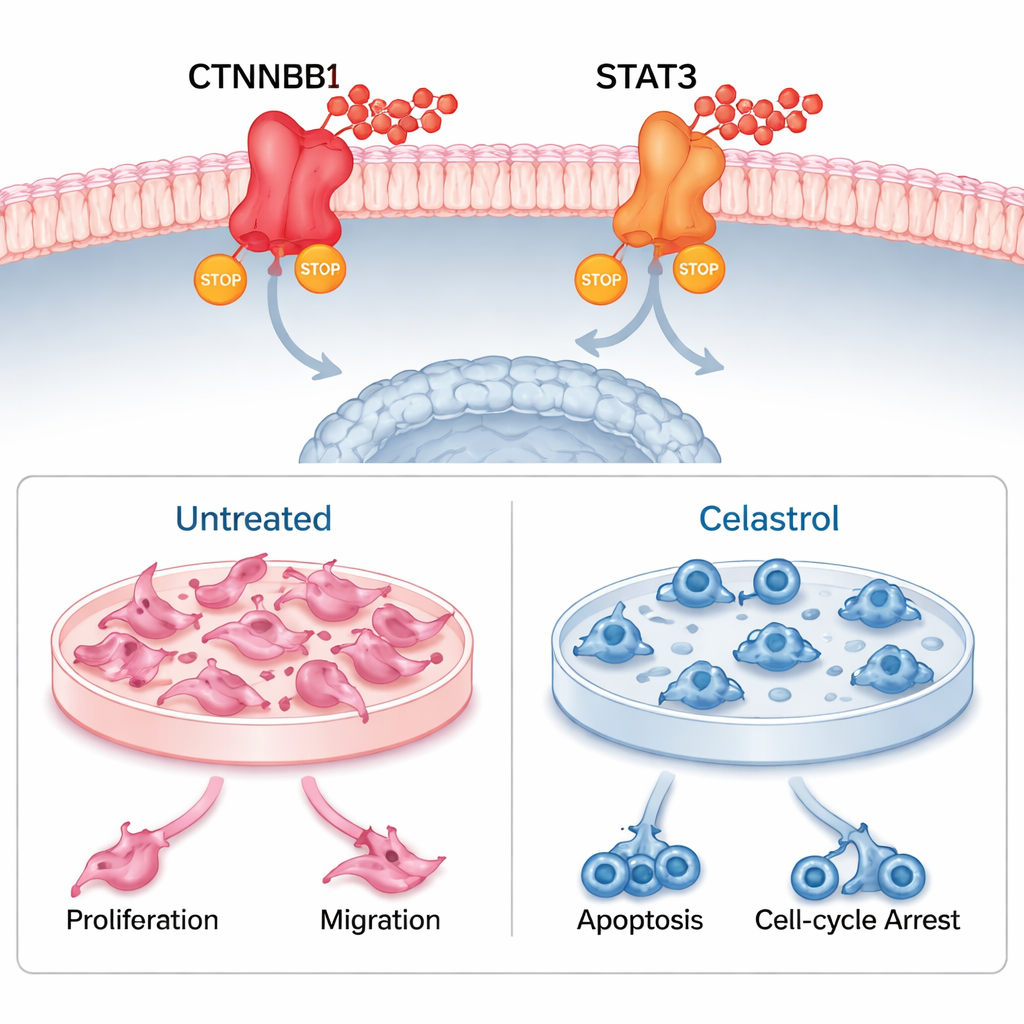
Het team gebruikte vervolgens moleculair docken en langdurige moleculaire dynamicasimulaties om te testen of celastrol zich fysiek aan CTNNB1 en STAT3 kan hechten. De virtuele experimenten suggereerden sterke en stabiele binding, ondersteund door meerdere waterstofbruggen en strakke verpakking rond het geneesmiddel. Vervolgens gingen ze het laboratorium in en behandelden menselijke uveale melanoomcellen en een gerelateerde muizenmelanoomcelijn met celastrol. In beide verminderde celastrol sterk de celoverleving en kolonievorming, vertraagde migratie in wondgenezingsassays en activeerde geprogrammeerde celdood. Het veroorzaakte ook dat cellen bleven hangen op specifieke punten in de celdelingcyclus, waardoor ze niet konden delen. Toen de onderzoekers genactiviteit en eiwitniveaus maten, vonden ze dat celastrol CTNNB1 en STAT3 duidelijk verlaagde, waarmee bevestigd werd dat het zijn voorspelde doelen in levende cellen raakt.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat suggereren de resultaten dat celastrol uveaal melanoom bestrijdt door tegelijkertijd CTNNB1 en STAT3 uit te schakelen. Deze dubbele werking remt niet alleen tumorgroei en -verspreiding, maar kan ook de immuunomgeving van de tumor zo hervormen dat deze een antikankerrespons bevordert. Hoewel dit werk is uitgevoerd in cellen en computermodellen — nog niet in patiënten of diermodellen — vormt het een sterke basis voor verder onderzoek. Voor niet-specialistische lezers is de kernboodschap dat een verbinding geworteld in de traditionele geneeskunde naar voren komt als een wetenschappelijk plausibele kandidaat voor een nieuwe klasse van oogkankertherapieën, eentje die zowel de tumor als het ecosysteem van omliggende cellen aanpakt.
Bronvermelding: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
Trefwoorden: uveaal melanoom, celastrol, oogkanker, kankersignalering, tumormicro-omgeving