Clear Sky Science · nl
Ontwikkeling en voorlopige evaluatie van realtime PCR-tests voor zes melkzuurbacteriën
Vriendelijke microben achter alledaags voedsel
Veel van de voedingsmiddelen in de supermarkt—van yoghurt en kaas tot augurken en gefermenteerde groenten—verlaten hun smaak en mogelijke gezondheidsvoordelen aan vriendelijke bacteriën die bekendstaan als probiotica. Maar om deze “goede beestjes” veilig en betrouwbaar te benutten, moeten producenten er absoluut zeker van zijn welke bacteriesoorten daadwerkelijk in hun producten aanwezig zijn. Deze studie beschrijft nieuwe laboratoriumtests die snel en nauwkeurig zes veelbelovende probiotische bacteriën kunnen identificeren die in voedsel worden gebruikt, waarmee een brug wordt geslagen tussen geavanceerde microbiologie en het dagelijkse voedingspatroon.
Waarom deze probiotische bacteriën ertoe doen
De zes bacteriën die centraal staan in dit werk behoren allemaal tot de bredere groep van melkzuurbacteriën, die al lang bij fermentatie worden gebruikt. Recent onderzoek suggereert dat ze meer kunnen dan alleen melk of kool verzuren. Sommige stammen van Ligilactobacillus agilis en Ligilactobacillus salivarius kunnen mogelijk schadelijke darmbacteriën tegengaan, ontstekingen dempen en de gezondheid van de darmbarrière ondersteunen. Limosilactobacillus fermentum is in dierstudies in verband gebracht met betere bloeddrukregulatie en antioxidantwerking. Lactobacillus johnsonii lijkt de darmmicrobiota op manieren te helpen balanceren die meerdere organen kunnen beschermen. Pediococcus pentosaceus en Weissella cibaria tonen potentie om cholesterol te verlagen, bederf tegen te gaan en zelfs de mondgezondheid te ondersteunen. Met zo’n scala aan mogelijke voordelen is de voedingsindustrie erop gebrand deze soorten breder toe te passen—maar alleen als ze met vertrouwen geïdentificeerd kunnen worden.
De uitdaging van sterk op elkaar lijkende microben uit elkaar houden
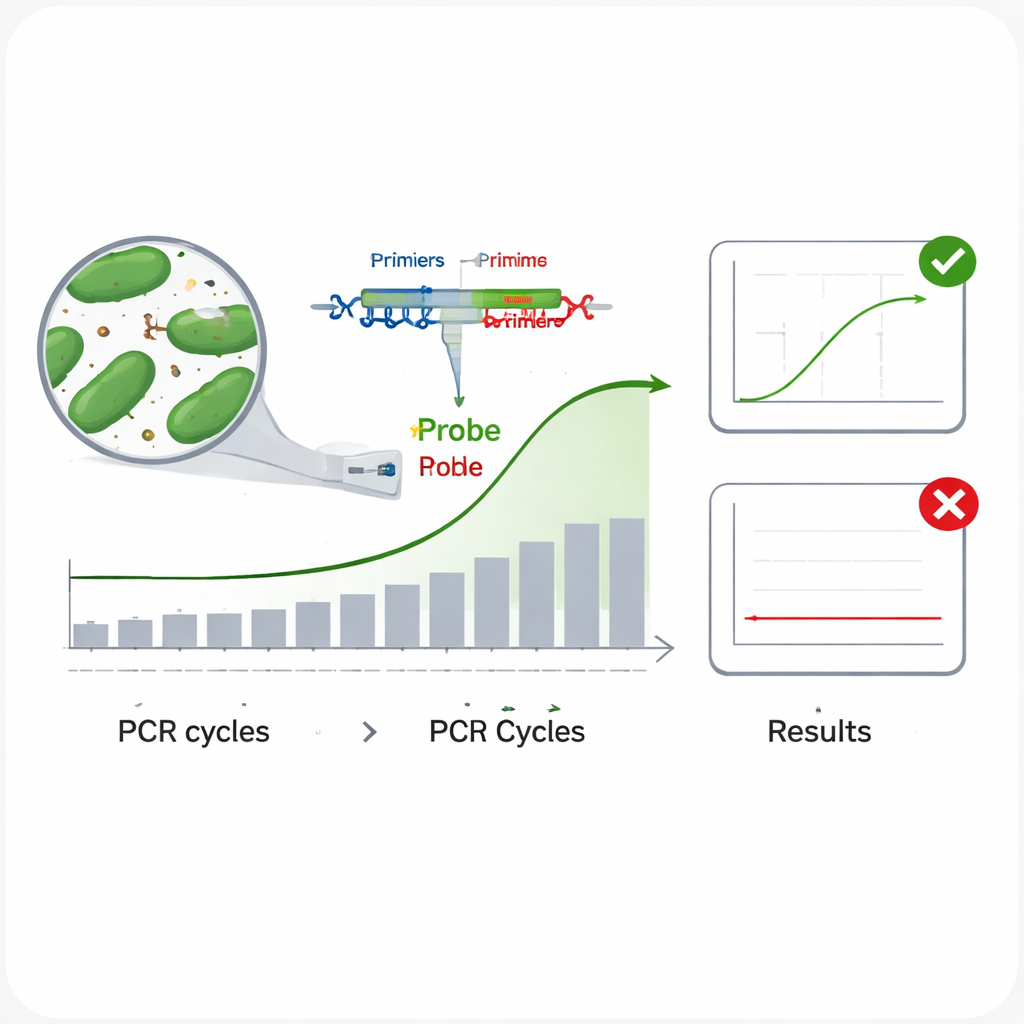
Traditionele methoden om bacteriën te identificeren—door ze te kweken in het lab en biochemische tests uit te voeren—zijn traag en arbeidsintensief. Moderne DNA-gebaseerde methoden, met name realtime PCR, zijn veel sneller. Bij realtime PCR richten korte DNA-stukken, primers en een fluorescente probe, zich op een unieke reeks in het genetische materiaal van een microbe; als de juiste microbe aanwezig is, detecteert het instrument een oplichtend signaal terwijl het DNA cyclus na cyclus wordt gekopieerd. Het probleem is dat nauwe verwanten vaak zeer vergelijkbaar DNA delen, waardoor algemeen gebruikte genetische regio’s zoals het 16S rRNA-gen soms niet in staat zijn één soort van een andere te onderscheiden. Dat kan leiden tot tests die het doel missen (valse negatieven) of reageren op de verkeerde soort (valse positieven), wat onaanvaardbaar is voor productetikettering en veiligheid.
Het ontwerpen van scherpere moleculaire "barcodes"
Om dit te overwinnen doorzochten de onderzoekers volledige genomen om korte DNA-regio’s te vinden die binnen elke doelsoort sterk geconserveerd zijn en duidelijk verschillen van andere bacteriën. Voor elk van de zes probiotica ontwierpen ze een bijpassende set primers en een probe met zorgvuldig afgestemde lengte, basensamenstelling, smelttemperatuur en minimale neiging tot zichzelf vouwen of aan elkaar plakken. Computercontroles met de BLAST-database en sequentie-alignments bevestigden dat de geselecteerde DNA-regio’s stabiel waren binnen de soort maar verschillend van niet-doelen. Het team werkte vervolgens een standaard reactiemix en verwarmingsprogramma uit zodat alle tests onder consistente en praktische voorwaarden op hetzelfde type realtime PCR-machine konden worden uitgevoerd.
De nieuwe tests in de praktijk toetsen
De wetenschappers evalueerden daarna hoe goed elke assay in de praktijk presteerde. Om inclusiviteit te testen—of een test veel verschillende stammen van dezelfde soort kan detecteren—voerden ze elke assay uit op meerdere DNA-monsters van de doelbacterie. In alle gevallen gaven alle geteste stammen een duidelijke amplificatiecurve, wat wijst op een laag risico om echte doelen te missen. Om specificiteit te controleren—of de assay niet reageert op niet-doelsoorten—stelden ze elke test bloot aan DNA van 13 andere darmbacteriën, waaronder verwante melkzuurbacteriën en veelvoorkomende darmmicroben zoals Escherichia coli. Geen van deze gaf een signaal, wat duidt op een zeer laag risico op valse alarmen. Het team onderzocht ook de amplificatie-efficiëntie door een reeks tienvoudige verdunningen van DNA uit te voeren en bevestigde dat alle zes assays hun doelwitten ongeveer met 95–100% efficiëntie kopieerden, dicht bij het ideale. Ten slotte maten ze de precisie door runs te herhalen op twee DNA-niveaus en constateerden dat kleine variaties tussen herhalingen en tussen afzonderlijke experimenten ruim binnen aanvaarde grenzen bleven.
Wat dit betekent voor toekomstige voedingsmiddelen
Kort gezegd hebben de auteurs zes fijnafgestelde DNA-"vingerafdruk"-tests ontwikkeld die sleutelprobiotische soorten snel, nauwkeurig en betrouwbaar van elkaar kunnen onderscheiden. Hoewel ze waarschuwen dat uitgebreidere tests op meer stammen, meer niet-doelsoorten en extra PCR-instrumenten nog nodig zijn voordat routinematige industriële toepassing mogelijk is, zijn de vroege resultaten bemoedigend. Voor consumenten helpen dergelijke vooruitgangen ervoor te zorgen dat voedingsmiddelen die adverteren specifieke probiotica te bevatten, daadwerkelijk de juiste microben bevatten, wat weer bijdraagt aan eerlijke etikettering, betere kwaliteitscontrole en betrouwbaarder onderzoek naar hoe deze kleine partners onze gezondheid beïnvloeden.
Bronvermelding: Li, SJ., Cui, B., Li, W. et al. Development and preliminary evaluation of real-time PCR assays for six lactic acid bacteria. Sci Rep 16, 6165 (2026). https://doi.org/10.1038/s41598-026-37047-3
Trefwoorden: probiotica, melkzuurbacteriën, realtime PCR, voedselmicrobiologie, microbiële identificatie