Clear Sky Science · nl
Een unified multimodaal transformer‑framework voor voorspelling van terugkeer van borstkanker en overlevingsanalyse
Waarom het voorspellen van terugkeer van kanker ertoe doet
Voor veel vrouwen brengt het afronden van de behandeling tegen borstkanker verlichting, maar ook een aanhoudende vraag: zal de ziekte terugkeren, en zo ja, wanneer en hoe ernstig? Huidige nazorgplannen zijn vaak gebaseerd op brede gemiddelden in plaats van op de unieke mix van factoren die elke patiënt kenmerken. Deze studie introduceert een nieuw systeem met kunstmatige intelligentie dat artsen een helderder, persoonlijker beeld wil geven van zowel het risico op terugkeer van borstkanker als de periode waarin patiënten waarschijnlijk kankervrij blijven.
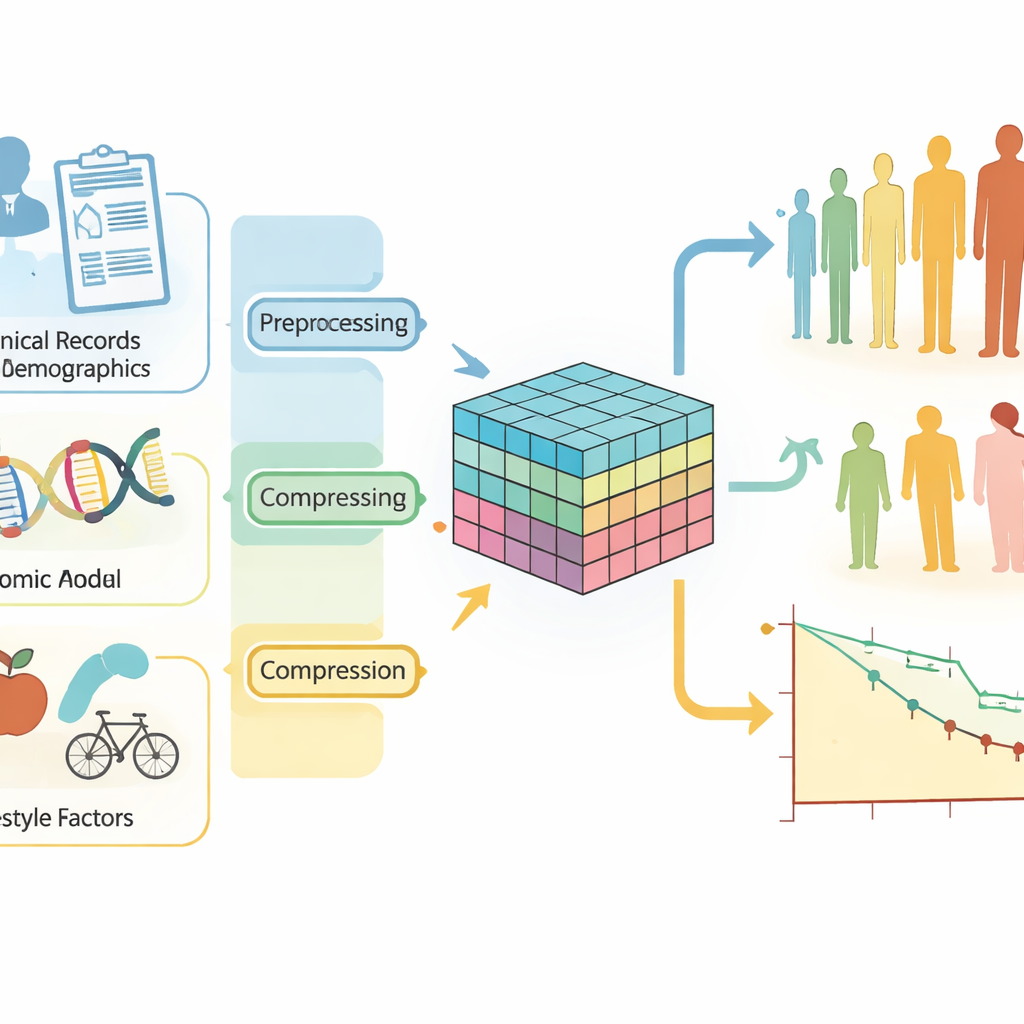
Verschillende soorten patiëntgegevens samenbrengen
Terugkeer van borstkanker is geen eenduidige uitkomst. Het kan zich openbaren als een nieuwe tumor in dezelfde borst, uitzaaiing naar naburige lymfeklieren of verre metastasen in organen zoals longen of botten. Elk patroon heeft andere implicaties voor behandeling en overleving. Tegelijk wordt het risico gevormd door veel onderling verweven invloeden: tumoreigenschappen, genexpressie, leeftijd, menopauzale status, lichaamsgewicht, roken en meer. Traditionele statistische hulpmiddelen hebben moeite met deze mix van klinische, genetische en leefstijlinformatie. Ze veronderstellen meestal eenvoudige, lineaire relaties en vertrouwen vaak op met de hand gemaakte risicoscores die de echte complexiteit van moderne kankerdata niet kunnen vatten.
Een verenigd slim model in plaats van losse instrumenten
De onderzoekers ontwierpen één diepgaand leerframework dat twee taken tegelijk aanpakt: het voorspelt welke van vier terugkeertypen een patiënt het meest waarschijnlijk zal krijgen, en het schat de timing van dat evenement met behulp van overlevingsanalyse. In plaats van aparte modellen te bouwen voor "komt het terug?" en "wanneer komt het terug?", leert het systeem beide antwoorden tegelijk. Onder de motorkap gebruikt het een transformer‑architectuur — dezelfde modelfamilie die veel geavanceerde taalhulpmiddelen aandrijft — om subtiele patronen en langafstandinteracties in de data te ontdekken. Deze geïntegreerde aanpak is bedoeld om te weerspiegelen hoe oncologen denken: vele aanwijzingen tegelijk afwegen in plaats van geïsoleerde berekeningen uit te voeren.
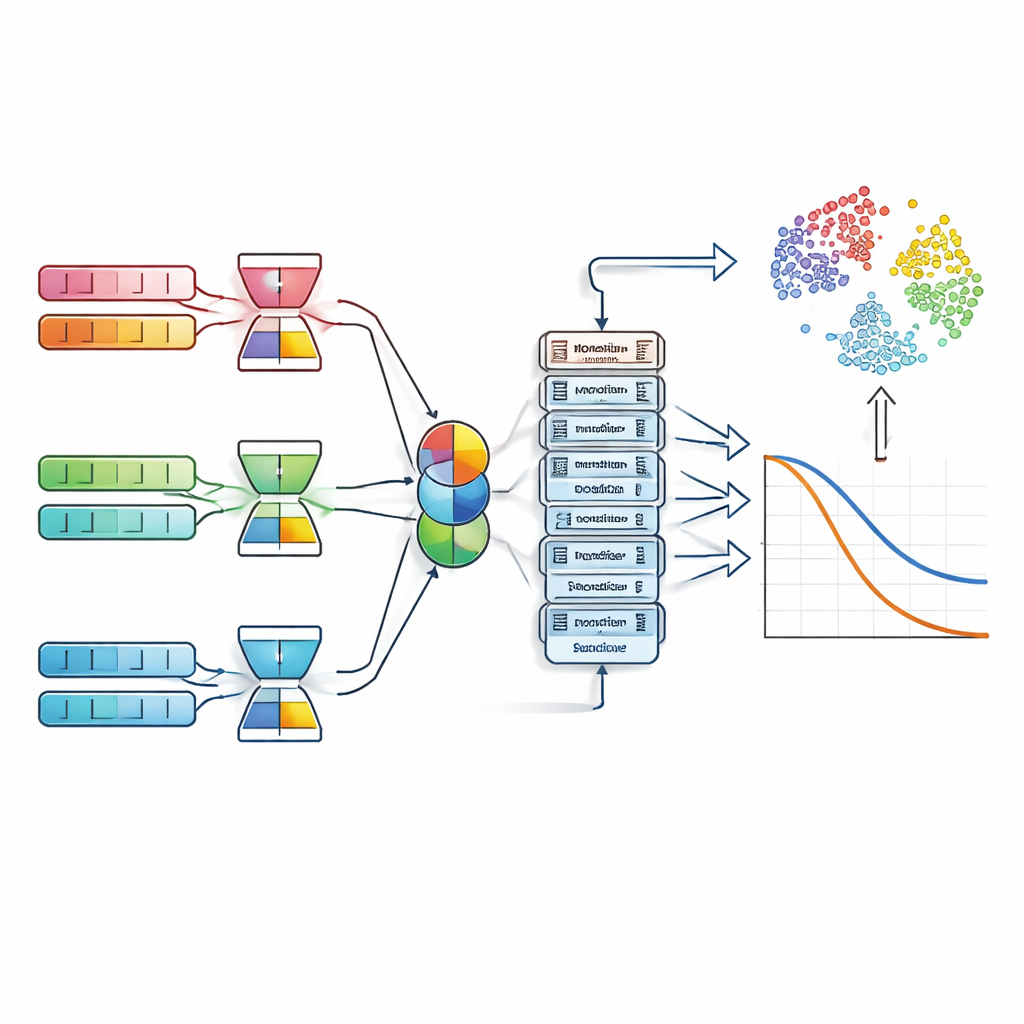
Hoe het systeem patronen in gezondheidsdata leest
Om het model te voeden stelde het team een grote multicentercollectie van borstkankerrecords samen uit vijf bekende bronnen. Deze omvatten duizenden patiënten met gedetailleerde klinische metingen, genexpressieprofielen, demografische informatie en leefstijlaanwijzingen. Omdat zulke gegevens ruisig en hoog‑dimensionaal kunnen zijn — vooral de tienduizenden metingen van genactiviteit — laat het systeem elk datatype eerst door een "denoising autoencoder" lopen. Deze stap comprimeert elke modaliteit tot een schonere, compacte representatie die belangrijke biologische signalen bewaart en willekeurige ruis wegfiltert.
Leren wat voor elke patiënt het zwaarst weegt
Na compressie plakt het model niet simpelweg alle kenmerken aan elkaar. In plaats daarvan past het een modaliteits‑attentiemechanisme toe dat leert hoeveel gewicht klinische, genetische of leefstijlinformatie voor elk individu moet krijgen. Voor sommige patiënten kunnen tumorgrootte en hormoonreceptorstatus domineren; voor anderen is een bepaald genpatroon of rookgeschiedenis informatiever. Deze gewogen signalen worden samengevoegd tot één patiëntprofiel en verwerkt door gestapelde transformerlagen, die zelf‑attentie gebruiken om te modelleren hoe verschillende risicofactoren met elkaar interageren. Vanuit deze gedeelde representatie voorspelt een tak het type terugkeer, terwijl een andere een continue risicoscore schat die kan worden vertaald naar overlevingscurven over vijf en tien jaar.
Prestaties, validatie en interpreteerbaarheid
In tests over de vijf datasets presteerde het verenigde systeem consequent beter dan standaardmethoden zoals logistische regressie, support vector machines, random forests, klassieke Cox‑overlevingsmodellen en eenvoudigere neurale netwerken. Het behaalde ongeveer 98–99% nauwkeurigheid bij het classificeren van het terugkeertype en een hoge concordantie‑index — een gevestigde maat voor hoe goed de voorspelde volgorde van overleving overeenkomt met de werkelijkheid. Cross‑datasetexperimenten, waarbij het model op één cohort werd getraind en op een ander werd getest, toonden aan dat het beter generaliseerde dan concurrerende benaderingen. Om te voorkomen dat het een mysterieus "black box" wordt, gebruikten de auteurs ook uitlegmethoden die aangeven welke kenmerken elke voorspelling het sterkst beïnvloedden. Tumorgrootte, HER2‑status, roken, menopauzale status, leeftijd bij diagnose en BRCA1‑mutaties bleken bijzonder belangrijk en kwamen goed overeen met huidige medische inzichten.
Wat dit betekent voor patiënten en artsen
De kernboodschap van de studie is dat één zorgvuldig ontworpen AI‑systeem veel informatie kan integreren om een rijker, betrouwbaarder beeld te geven van het risico op terugkeer van borstkanker en van overleving. Hoewel het nog prospectief getest moet worden in klinische praktijk, zou het framework op termijn artsen kunnen helpen bij het afstemmen van controleschema’s, het kiezen van behandelingen en het adviseren van patiënten met meer vertrouwen. Voor patiënten kan dit leiden tot nazorgplannen die beter aansluiten bij hun werkelijke risiconiveau — waardoor onnodige zorgen en tests voor sommigen verminderen, terwijl anderen worden geïdentificeerd die baat kunnen hebben bij nauwere monitoring of een agressievere therapie.
Bronvermelding: Malik, S., Patro, S.G.K., Al-Nussairi, A.K.J. et al. A unified multi modal transformer framework for breast cancer recurrence prediction and survival analysis. Sci Rep 16, 8334 (2026). https://doi.org/10.1038/s41598-026-37046-4
Trefwoorden: terugkeer van borstkanker, overlevingsvoorspelling, multimodaal deep learning, transformermodel, gepersonaliseerde oncologie