Clear Sky Science · nl
Met machine learning voorspellen van hemorragische transformatie na trombectomie met kwantitatieve DSA
Waarom dit belangrijk is voor beroertepatiënten
Wanneer iemand een grote beroerte krijgt, kunnen artsen in sommige gevallen het stolsel uit de hoofdslagader van de hersenen verwijderen met een klein instrument tijdens een ingreep die mechanische trombectomie heet. Dit heeft de behandeling van beroertes veranderd, maar veel patiënten herstellen toch slecht omdat sommigen nieuwe bloedingen in de hersenen ontwikkelen. De studie achter dit artikel stelt een eenvoudige maar cruciale vraag: kunnen we gebruikmaken van informatie die artsen al in de operatiekamer verzamelen, gecombineerd met moderne machine learning, om te voorspellen welke patiënten het meest waarschijnlijk zullen bloeden en extra bescherming nodig hebben?
Verder kijken dan “slagader open of dicht”
Vandaag de dag wordt succes na trombectomie meestal beoordeeld op basis van of de geblokkeerde slagader er op angiografie — een soort realtime röntgenfilm van bloedvaten — weer open uitziet. Maar deze grove beoordeling zegt niets over wat er gebeurt in de kleine downstreamvaten van de hersenen, waar schade en bloedingen daadwerkelijk optreden. Sommige patiënten met ogenschijnlijk perfecte reopening van grote vaten ontwikkelen toch ernstige hersenbloedingen, een complicatie die hemorragische transformatie wordt genoemd. De auteurs vermoedden dat meer gedetailleerde metingen van de bloedstroom in deze kleine vaten, afgeleid van dezelfde angiogrammen, verborgen aanwijzingen kunnen bevatten over wie risico loopt.
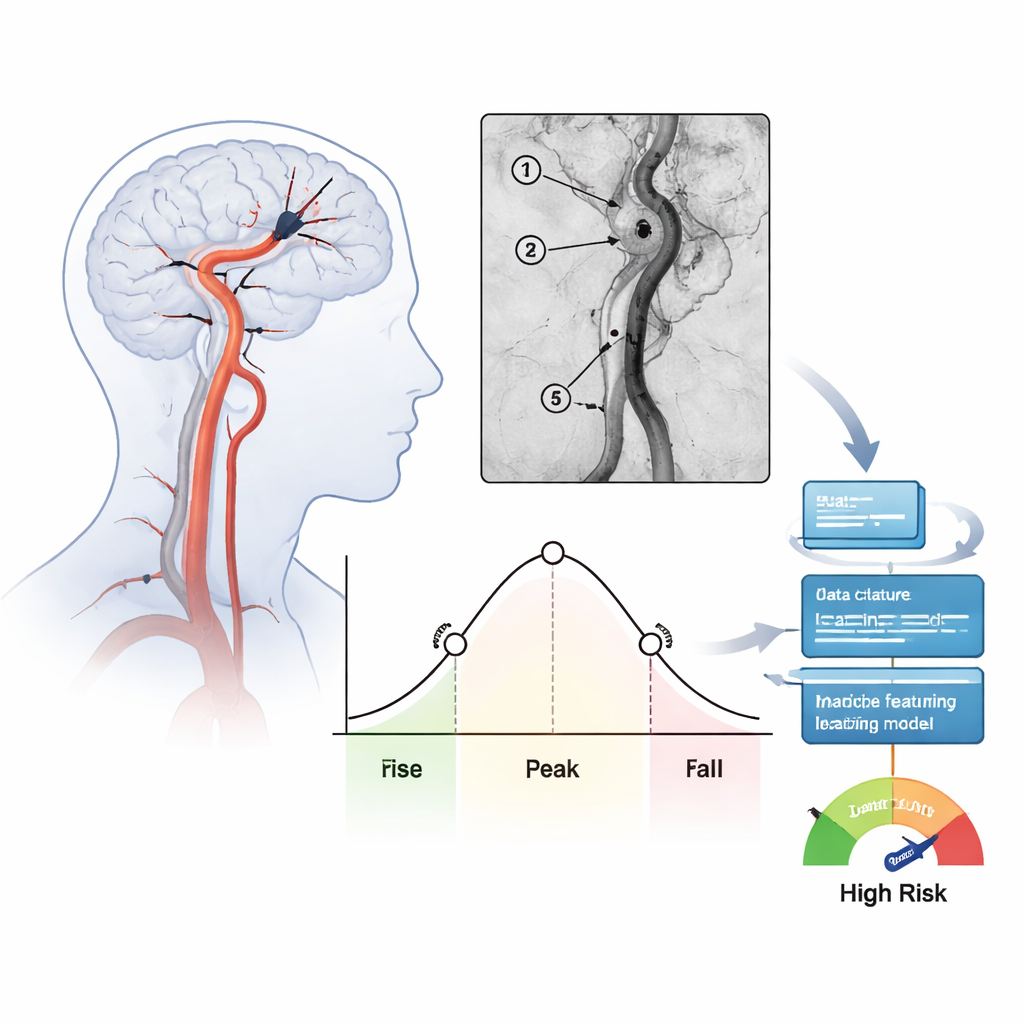
Angiogramfilms omzetten in getallen
Het team bestudeerde 171 mensen die binnen een jaar in één ziekenhuis werden behandeld voor ernstige beroertes aan de voorzijde van de hersenen. Nadat artsen het stolsel hadden verwijderd en de doorstroming waren hersteld, namen ze standaard angiografiebeelden op en analyseerden ze vervolgens hoe het geïnjecteerde contrastmiddel in- en uitwaste bij verschillende sleutelplaatsen langs de behandelde slagader. Voor elk gebied berekenden ze tijdsmetingen zoals hoe lang bloed nodig had om erdoorheen te stromen (mean transit time) en hoe breed de belangrijkste contrastpiek was (full width at half maximum). Deze cijfers vatten samen of bloed langzaam en gelijkmatig stroomt of snel en geconcentreerd in een smalle puls passeert. In totaal werden 39 dergelijke stromingskenmerken voor elke patiënt geëxtraheerd en gecontroleerd op consistentie tussen onafhankelijke beoordelaars.
De computer leren risicopatronen te herkennen
De onderzoekers gebruikten vervolgens een reeks gangbare machine-learningmethoden om te bepalen of deze stromingskenmerken, alleen of gecombineerd met basale klinische gegevens zoals leeftijd en ernst van de beroerte, patiënten die later bloedingen ontwikkelden konden onderscheiden van degenen die dat niet deden. Om overfitting te vermijden, gebruikten ze eerst vijf verschillende feature-selectietechnieken om de meest informatieve metingen te kiezen, en ze splitsten de data herhaaldelijk in trainings- en testgroepen met crossvalidatie. Van de vele geteste combinaties presteerde een relatief simpel model — logistieke regressie, afgestemd met een “Elastic Net” feature-filter — het beste. Wanneer het model alleen op angiografieafgeleide stromingsmetingen vertrouwde, onderscheidde het patiënten met en zonder bloedingen met een gemiddelde area under the ROC curve van ongeveer 0,81. Met toevoeging van klinische factoren steeg de prestatie naar ongeveer 0,86, wat suggereert dat het model een sterke beslissingshulp kan zijn.
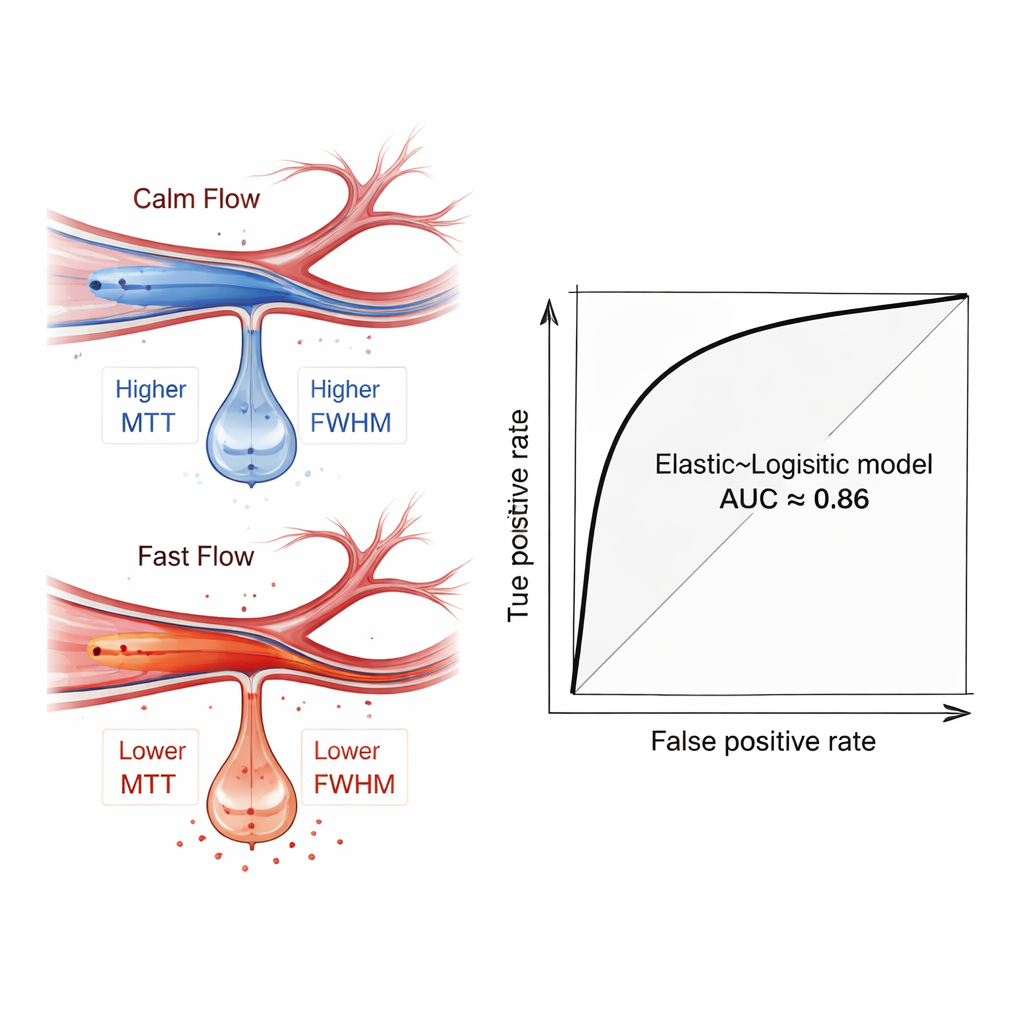
Wat de bloedstroomsignalen onthulden
Door in de getrainde modellen te duiken, gebruikten de auteurs een interpreteerbaarheidstechniek genaamd SHAP om te zien welke kenmerken het meest relevant waren. Metingen die vastleggen hoe lang en hoe verspreid de stromingspuls is — vooral in een verder gelegen tak van de middelste hersenslagader — vielen op als belangrijke voorspellers. Patiënten die later bleden vertoonden vaak snellere, meer gefocuste flow in deze distale vaten, zichtbaar als kortere transitietijden en smallere pieken. Dit patroon is een hemodynamische vingerafdruk van “hyperperfusie”, een toestand waarin kwetsbaar hersenweefsel, dat lange tijd van bloed was verstoken, plotseling met hogesnelheidsbloed wordt doorgespoeld en daardoor eerder kan lekken en bloeden. Belangrijk is dat dit signaal naar voren kwam zelfs wanneer eenvoudige groepsvergelijkheden geen dramatische statistische verschillen lieten zien, wat de waarde van multifeature- en machinaal gebaseerde analyse benadrukt.
Hoe dit de zorg aan het bed kan veranderen
Aangezien de methode gebruikmaakt van beelden die al tijdens de trombectomie worden verkregen, zijn er geen extra scans, contrastmiddel of straling nodig. Zodra interessegebieden zijn uitgetekend — een stap die momenteel enkele minuten duurt — kan de computer automatisch stromingsmetingen berekenen en een gepersonaliseerde schatting van het bloedingsrisico genereren. In principe kan dit artsen helpen bij het afstemmen van bloeddrukdoelen, beslissen hoe agressief bloedverdunners te gebruiken en het plannen van vervroegde CT-scans bij patiënten die als hoogrisico worden aangemerkt. De auteurs waarschuwen dat hun studie retrospectief is en uit één centrum komt, dus grotere, multiziekenhuisproeven nodig zijn voordat het hulpmiddel routinematig kan worden ingezet. Toch biedt het een duidelijk bewijs van het concept: door beroerte-angiogrammen om te zetten in rijke numerieke data en machine learning erdoor te laten snuffelen, kunnen we verder gaan dan alleen de vraag “Is de slagader open?” naar “Is de microcirculatie van de hersenen veilig?” — een verschuiving die mogelijk uiteindelijk meer patiënten kan besparen van gevaarlijke bloedingen na behandeling.
Bronvermelding: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Trefwoorden: beroerte, mechanische trombectomie, hersenbloeding, machine learning, angiografie