Clear Sky Science · nl
Invloed van systeemtherapieën specifiek voor neuro-endocriene neoplasmata op expressie en functie van CXCR4 in neuro-endocriene tumoren
Waarom dit ertoe doet voor toekomstige kankerzorg
Wanneer bepaalde zeldzame tumoren van darm en alvleesklier agressiever worden, verliezen ze vaak hun reactie op standaard gerichte behandelingen. Artsen en onderzoekers hebben dringend nieuwe manieren nodig om deze moeilijker te behandelen tumoren zichtbaar te maken en aan te vallen. Deze studie stelt een praktische vraag met grote implicaties: veranderen de chemotherapieën en gerichte medicijnen die patiënten al krijgen een belangrijke tumormarker genaamd CXCR4, die wordt ontwikkeld zowel als diagnostisch "baken" als behandeldoel?
Een verschuivend doelwit op agressieve tumorcellen
Neuro-endocriene neoplasmata zijn zeldzame kankers die ontstaan uit hormoonproducerende cellen, meestal in de darm en de alvleesklier. In hun vroege, meer geordende vorm tonen deze tumoren vaak een oppervlaktemolecuul genaamd somatostatine-receptor 2, dat artsen kunnen afbeelden en behandelen met gespecialiseerde radioactieve middelen. Naarmate de ziekte agressiever wordt, verliezen deze tumoren die marker vaak, waardoor ze moeilijker te detecteren en te behandelen zijn. Tegelijkertijd zetten veel van deze tumoren een ander oppervlaktemolecuul aan: een receptor genaamd CXCR4, die geassocieerd wordt met snellere groei, uitzaaiing naar andere organen en slechtere overleving. Omdat CXCR4 met een PET-tracer afgebeeld kan worden en mogelijk bestreden kan worden met radioactieve of antilichaam-gebaseerde middelen, is het een veelbelovend "reserve"-doel geworden zodra standaardopties falen.
Reële geneesmiddelen testen in tumormodellen
De onderzoekers wilden weten hoe de middelen die al gebruikt worden om hooggradige neuro-endocriene tumoren te behandelen CXCR4 zelf beïnvloeden. Als deze medicijnen per ongeluk CXCR4 verlagen, zouden ze toekomstige op CXCR4 gebaseerde beeldvorming of therapieën kunnen verzwakken — maar ze zouden ook kunnen bijdragen aan het temmen van de agressiviteit van de kanker. Het team werkte met drie verschillende menselijke tumorcellenlijnen die agressieve vormen van de ziekte vertegenwoordigen, waaronder één hybride lijn die vooral moeilijk te behandelen tumoren goed nabootst. Ze stelden deze cellen bloot aan zes veelgebruikte middelen: de chemotherapieën cisplatine, etoposide, streptozotocine, 5‑fluorouracil, het orale middel temozolomide, en de gerichte mTOR-remmer everolimus. Na behandeling maten ze CXCR4 op genetisch en proteiniveau en testten ze hoe goed de cellen nog een CXCR4-zoekende PET-tracer konden opnemen.
Sommige middelen dempen het CXCR4-signaal
De resultaten lieten zien dat niet alle kankermiddelen gelijk zijn met betrekking tot deze receptor. Cisplatine verminderde duidelijk de genetische activiteit van CXCR4 in twee van de drie cellijnen en sneed de traceropname significant in twee lijnen, wat betekent dat er minder functionele receptoren waren waar de tracer aan kon binden. Temozolomide en everolimus verlaagden ook CXCR4-niveaus op genetisch en proteïne niveau in meerdere celtypen, hoewel dit niet altijd leidde tot een statistisch duidelijke daling in traceropname. Daarentegen hadden etoposide en streptozotocine weinig effect op CXCR4, terwijl 5‑fluorouracil bescheiden veranderingen veroorzaakte die de tracerbinding niet sterk beïnvloedden. Over het geheel genomen suggereerde het patroon dat cisplatine, temozolomide en everolimus CXCR4 kunnen dempen in deze agressieve tumorcellen, terwijl de andere middelen het grotendeels onaangetast laten.
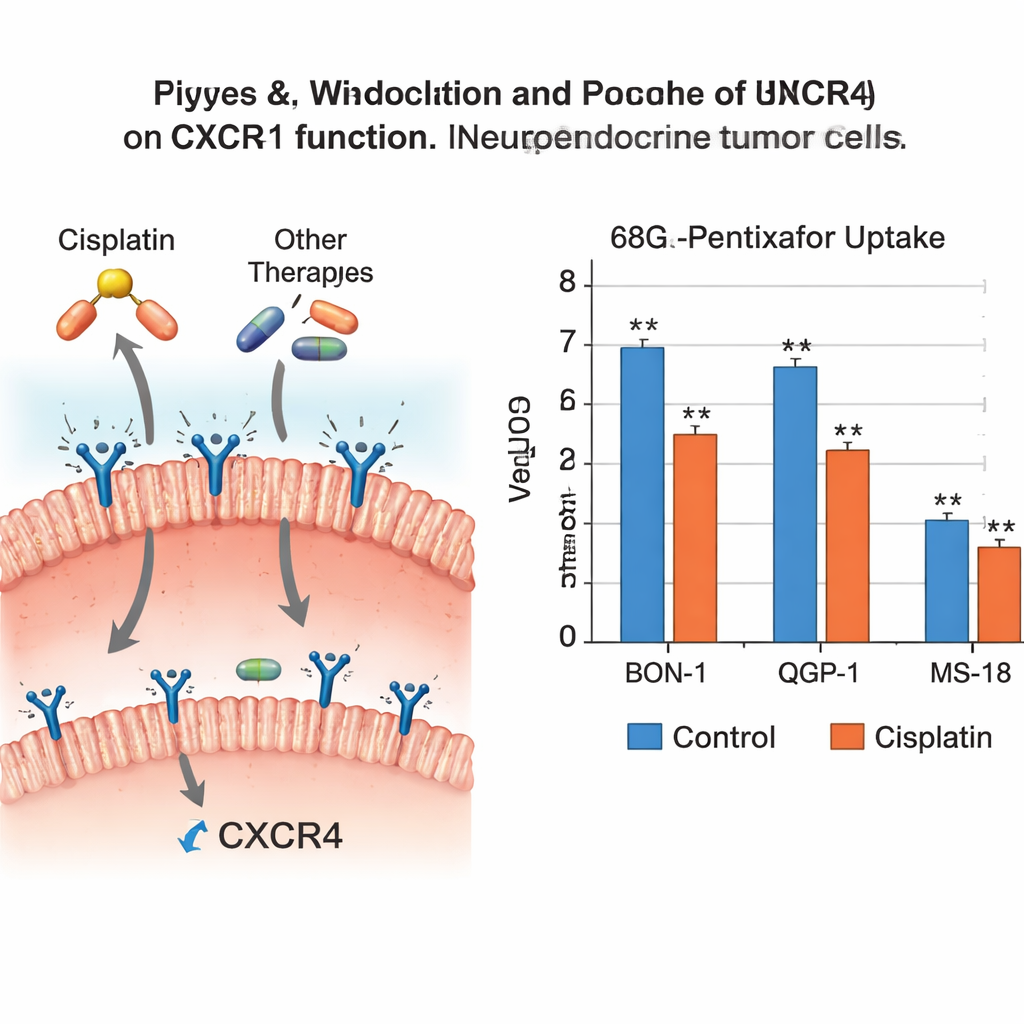
Wat dit betekent voor beeldvorming en timing van behandelingen
Deze bevindingen dragen een dubbele boodschap voor toekomstige patiëntenzorg. Aan de ene kant kan het dempen van CXCR4 deel uitmaken van hoe middelen zoals cisplatine, temozolomide en everolimus de uitzaaiing van tumoren afremmen, omdat hoge CXCR4-waarden gekoppeld zijn aan invasiviteit en metastasering. Aan de andere kant, als de CXCR4 van een tumor onderdrukt wordt door lopende behandeling, kunnen op CXCR4 gebaseerde PET-scans de hoeveelheid ziekte onderschatten en kunnen CXCR4-gerichte radioactieve therapieën minder aanknooppunten hebben om te raken. De studie suggereert dat het combineren van CXCR4-gerichte behandelingen direct met deze systemische middelen waarschijnlijk niet zal zorgen dat die CXCR4-gerichte therapieën beter werken, en ze mogelijk zelfs kan verzwakken.
Een nieuw puzzelstuk voor gepersonaliseerde therapie
Voor niet-specialisten is de belangrijkste conclusie dat één tumormarker twee rollen tegelijk kan vervullen: ze kan een waarschuwingssignaal zijn voor agressieve ziekte en tegelijkertijd een bruikbare handgreep voor beeldvorming en gerichte behandeling. Dit onderzoek toont dat sommige gevestigde kankermiddelen die marker stilletjes omhoog of omlaag kunnen bijstellen. In de praktijk kan dit van invloed zijn op wanneer CXCR4-gebaseerde scans en therapieën gepland worden — bij voorkeur wanneer de receptor het meest overvloedig is — en kan het helpen verklaren waarom bepaalde behandelingen effectief zijn tegen snelgroeiende neuro-endocriene tumoren. Hoewel deze resultaten voortkomen uit cellijnen en bevestiging bij patiënten nodig is, vormen ze een belangrijke stap richting slimmer opvolgen en sequencen van therapieën voor mensen met deze uitdagende kankers.
Bronvermelding: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Trefwoorden: neuro-endocriene tumoren, CXCR4, cisplatine, everolimus, gerichte beeldvorming