Clear Sky Science · nl
Een ontworpen M13-fage–rGO elektrochemische biosensor voor snelle detectie van viraal eiwit in complexe matrices
Waarom snelle virustests nog steeds belangrijk zijn
De COVID-19-pandemie maakte duidelijk hoe cruciaal het is om virussen snel op te sporen, niet alleen bij patiënten maar ook op locaties zoals afvalwaterzuiveringen en productielijnen voor levensmiddelen. De huidige laboratoriumtests zijn krachtig maar kunnen traag en duur zijn en afhankelijk van kwetsbare biologische componenten die moeilijk te vervoeren en te bewaren zijn. Deze studie presenteert een nieuw type miniatuursensor die gebruikmaakt van ontworpen virussen en een vel geavanceerd koolstofmateriaal om een sleutelprotein van SARS-CoV-2 in minder dan een seconde te detecteren, zelfs in rommelige real-world monsters zoals bloedserum, melk en afvalwater.
Een onschadelijk virus veranderen in een slimme detector
In het hart van het apparaat staat M13, een onschadelijk virus dat normaal gesproken bacteriën infecteert. Het lange, staafvormige lichaam is bedekt met vele identieke omhullende eiwitten die wetenschappers genetisch kunnen herprogrammeren. Het team voegde een korte, op maat gemaakte peptide toe aan een van deze eiwitten zodat de M13-deeltjes het S1-fragment van het coronavirus-spike-eiwit zouden herkennen en eraan zouden hechten. Een tweede variant van het virus, met een geschudde peptide, diende als controle om aan te tonen dat de reactie voortkomt uit echte herkenning en niet uit willekeurige adhesie.
Gebouwd op een vel atoomdun koolstof
Om dit programmeerbare virus in een sensor te veranderen, hechtten de onderzoekers het aan een vlak folie van gereduceerd grafeenoxide, een zeer geleidend koolstofmateriaal dat wordt verkregen door chemische bewerking van grafiet. Nadat grafeenoxide op kleine glaschips was verspreid en verwarmd om het in gereduceerd grafeenoxide om te zetten, voegden ze een koppelingsmolecuul toe dat aan het koolstofoppervlak hecht en ook bindt aan aminegroepen op het virus. Dit creëerde een dichte laag M13-deeltjes die verankerd waren op het geleidende folie. Elektronenmicroscopie en atomische krachtsmicroscopie bevestigden dat elke fabricagestap het oppervlak veranderde zoals verwacht, en elektrische metingen toonden dat het toevoegen van de koppeling en daarna het virus geleidelijk de weerstand verhoogde, een teken dat het oppervlak succesvol werd gecoat.
Virusbinding aflezen als een elektrische puls
Anders dan veel biosensoren die extra chemicaliën of bewegende onderdelen nodig hebben, werkt dit platform als een eenvoudige weerstand onder een zeer kleine constante spanning. Wanneer het S1-eiwit op het virusbedekte oppervlak landt en bindt aan de weergegeven peptide, verandert dat licht in de manier waarop lading door de grafeenlaag beweegt. Dit verschijnt als een korte piek in de elektrische stroom die ongeveer 300 milliseconden optreedt nadat er een druppel monster op de chip is geplaatst, en vervolgens vervaagt naarmate het systeem tot rust komt. Door de aangelegde spanning te tunen vond het team een optimaal punt rond minus 0,8 millivolt, waar het signaal van echte S1-binding sterk was terwijl achtergrondruis en reacties op niet-gerelateerde eiwitten, zoals bovien serumalbumine, laag bleven.
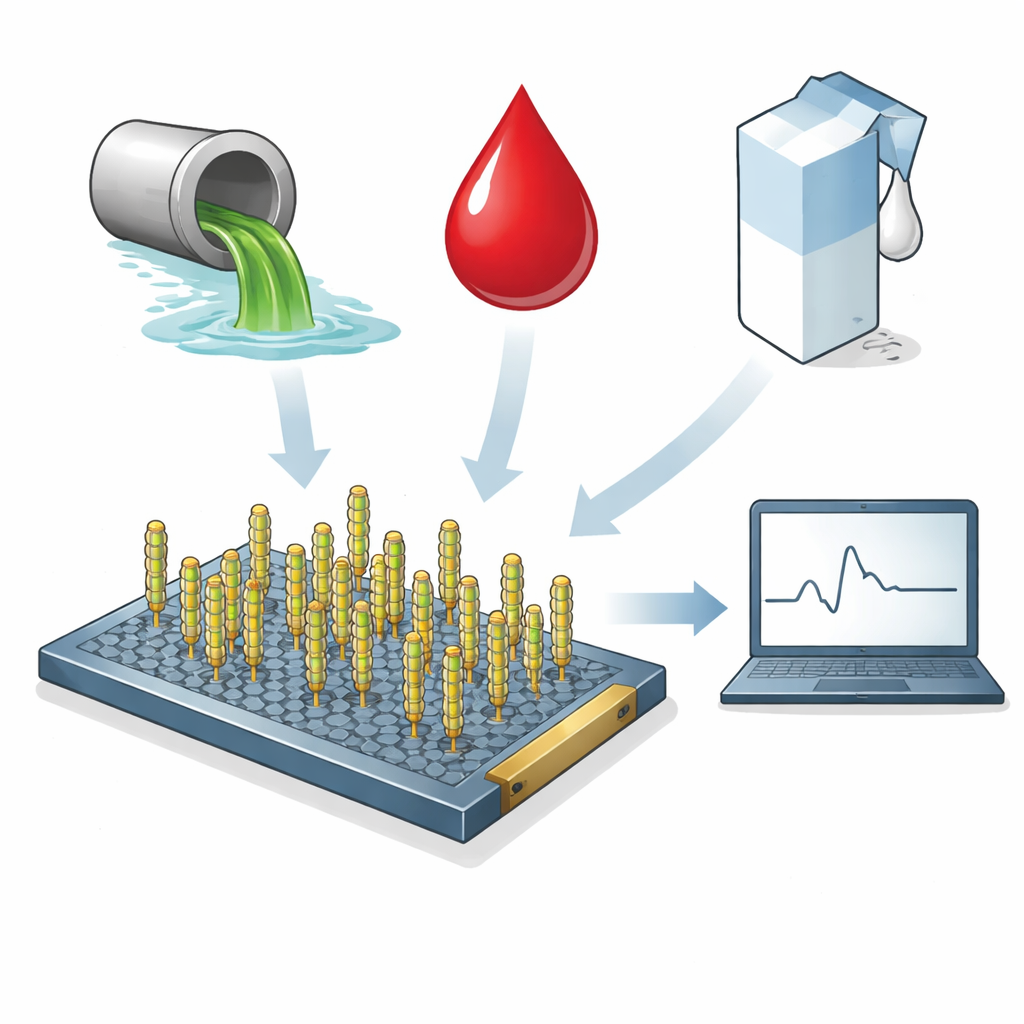
Werken in rommelige real-world monsters
De onderzoekers daagden de sensor vervolgens uit met soorten complexe mengsels die delicate laboratoriumreagentia vaak onschadelijk maken. Ze testten het apparaat in buffer, stedelijk afvalwater, foetaal bovien serum (een model voor bloed) en gepasteuriseerde melk, met en zonder toegevoegd S1-eiwit. Met behulp van een statistisch gedefinieerde drempel voor een positief resultaat detecteerde de sensor extreem lage eiwitniveaus in eenvoudige buffer—tot ongeveer 10⁻⁴ picogram per milliliter—vergelijkbaar met of beter dan veel op antilichamen gebaseerde systemen. In afvalwater gaf het apparaat betrouwbaar hogere S1-niveaus aan, terwijl het in serum en melk ook consequent lagere concentraties detecteerde, allemaal binnen een fractie van een seconde. Belangrijk is dat een controle-sensor met het geschudde virus weinig reactie op S1 vertoonde, wat bevestigt dat het signaal afhankelijk is van de ontworpen bindingssequentie. Een parallelle sensor met een conventioneel antilichaam op hetzelfde grafeenplatform presteerde vergelijkbaar, wat suggereert dat het virusgebaseerde systeem de gevoeligheid van antilichamen kan evenaren terwijl het mogelijk goedkoper en makkelijker te produceren is.

Wat dit kan betekenen voor alledaags testen
Antilichamen, de werkpaarden van veel diagnostiek, zijn duur om te produceren, gevoelig voor warmte en vereisen doorgaans koude opslag van fabriek tot kliniek. Daarentegen kunnen M13-virussen in bacteriën worden gekweekt als een eenvoudige cultuur, zijn ze beter bestand tegen zwaardere omstandigheden en kunnen ze worden herprogrammeerd door hun genetische code te herschrijven. Door deze robuustheid en flexibiliteit te combineren met een snelle, energiezuinige elektronische uitlezing op grafeen, schetst de studie een pad naar draagbare, goedkope apparaten die kunnen worden aangepast om veel verschillende ziekte-indicatoren of verontreinigingen te detecteren door eenvoudig de weergegeven peptide te veranderen. Het werk bevindt zich nog in de proof-of-concept-fase en is nog niet getest in menselijke klinische monsters, maar het wijst op een toekomst waarin handzame sensoren virale eiwitten en andere biomarkers binnen enkele seconden kunnen screenen in klinieken, riolen of zelfs voedselproducten, zonder de logistieke last van traditionele antilichaamtests.
Bronvermelding: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Trefwoorden: biosensor, grafeen, bacteriofaag, SARS-CoV-2, elektrochemische detectie