Clear Sky Science · nl
Labelvrije fluorescente levensduurbeelden kunnen kanker onderscheiden van gezond weefsel bij spontaan optredende orale tumoren bij honden
Kanker in een nieuw licht zien
Orale kankers bij zowel mensen als huisdieren zijn berucht moeilijk volledig te verwijderen. Chirurgen moeten ruime “veiligheids”marges rond een tumor wegsnijden om te voorkomen dat verborgen kankercellen achterblijven, maar in de mond kan dat betekenen dat belangrijk bot, tanden en zacht weefsel verloren gaan, met gevolgen voor eten en spreken. Deze studie onderzoekt een lichtgebaseerde beeldvormingstechniek die tijdens een operatie bij honden wordt gebruikt en chirurgen in realtime zou kunnen helpen kanker van gezond weefsel te onderscheiden—mogelijk met behoud van meer normaal weefsel terwijl de kanker toch onder controle blijft.
Waarom tumorranden zo moeilijk te vinden zijn
In de hedendaagse hoofd- en halstumorchirurgie vertrouwen artsen vaak op snelle bevroren-weefselanalyse om te beoordelen of de randen van een verwijderde tumor echt vrij van kanker zijn. Dat proces is traag, bemonstert slechts kleine gebieden en kan ziekte missen. Vergelijkbare uitdagingen bestaan bij de behandeling van honden met orale tumoren, waarbij lokaal terugkomen veel voorkomt. Omdat er geen betrouwbare manier is om microscopische kanker tijdens een operatie te “zien”, verwijderen chirurgen doorgaans ruime marges, wat kauwen, slikken en uiterlijk kan aantasten. De auteurs wilden een niet-invasieve beeldvormingstechniek testen die in de operatiekamer een duidelijker grens tussen kanker en normaal weefsel zou kunnen trekken.
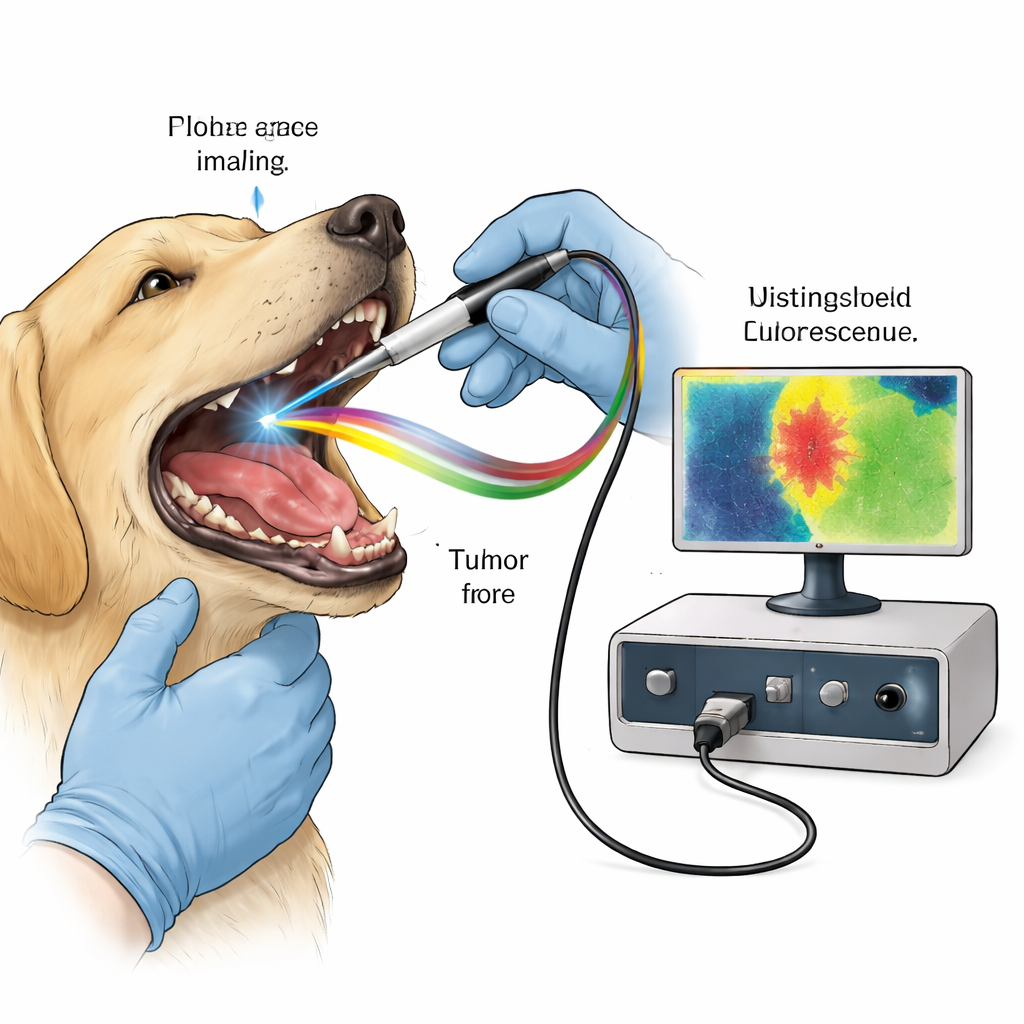
De natuurlijke gloed als chirurgische gids gebruiken
Veel moleculen in ons weefsel zenden van nature zwak fluorescerend licht uit nadat ze zijn geprikkeld door een korte laserpuls. Collageen in bindweefsel en moleculen die met celmetabolisme samenhangen zoals NADH en FAD hebben elk karakteristieke kleuren en timing tijdens hun gloed en verval. Kanker verstoort weefselstructuur en energiegebruik, en verandert dit fluorescerende vingerafdruk subtiel. Fluorescentielevensduurbeeldvorming (FLIm) meet niet alleen hoe helder weefsel gloeidt; het meet hoe lang die gloed aanhoudt in miljardsten van een seconde, een eigenschap die minder wordt beïnvloed door kijkomstandigheden. Het team gebruikte een aangepast handprobe dat snelle ultravioletpulsen in het tumorgebied van onder narcose zijnde honden schijnt en de terugkerende fluorescentie registreert in drie spectrale kanalen die zijn afgestemd op collageen, metabolische moleculen en een rood-uitstralend verbinding genaamd protoporfyrine IX (PpIX).
Een kankerzoekend kleurstofje toevoegen: hulp of hype?
PpIX kan zich in veel tumoren ophopen door patiënten een voorloper, 5-aminolevulinezuur (5-ALA), oraal toe te dienen. Onder blauw licht gloeien gebieden rijk aan PpIX vaak felroze en worden ze door chirurgen gebruikt om kanker te herkennen. De onderzoekers bevestigden eerst in hondenslijmvliestamcellen voor orale kanker dat 5-ALA leidde tot sterke PpIX-fluorescentie en toonden aan dat genen betrokken bij de productie en opname van 5-ALA actiever waren in kankercellen. Ze schreven vervolgens 15 huisdieren met spontaan optredende orale tumoren in en gaven hen enkele uren voor de operatie 5-ALA. In de operatiekamer fluoresceerden de meeste tumoren zichtbaar, maar ook sommige niet-kankerachtige ontstekings- of virale laesies lichtten op, wat suggereert dat visuele kleur op zichzelf mogelijk niet betrouwbaar de tumorgrenzen markeert.
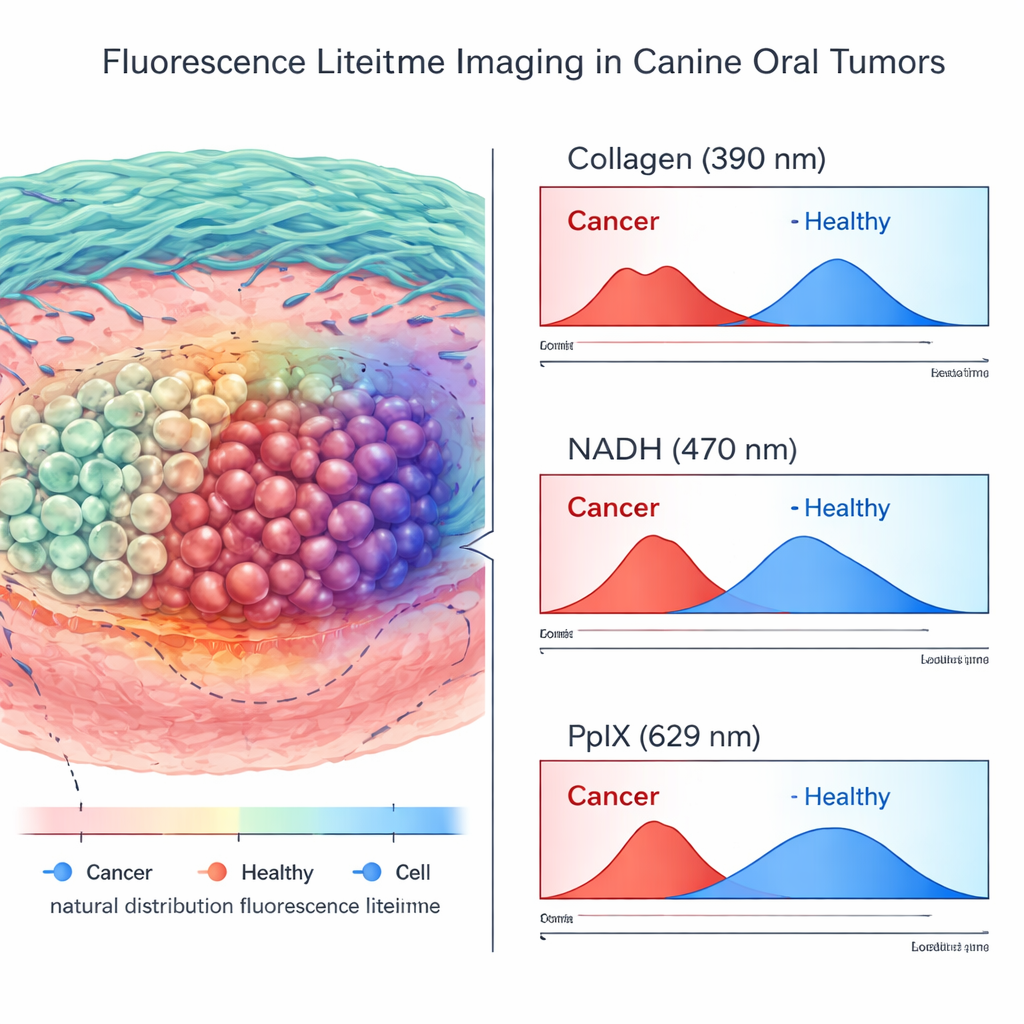
Wat de levensduurbeelden onthulden
Over meer dan 200.000 hoogwaardige meetpunten uit tumoren en nabijgelegen normaal weefsel vergeleek het team FLIm-signalen met gedetailleerde pathologiskaarten. Ze vonden dat veel levensduur- en intensiteitskenmerken significant verschilden tussen kanker en gezond weefsel. De sterkste en meest consistente scheiding kwam echter uit de labelvrije kanalen: kortere levensduren in het collageengevoelige band en karakteristieke verschuivingen in het NADH-gevoelige band waren sterk gelinkt aan kanker. Ter vergelijking gaf het PpIX-kanaal—dat door de toegediende 5-ALA werd versterkt—minder betrouwbare informatie in levend weefsel. De metingen varieerden sterk in normale gebieden, waarschijnlijk omdat ontstoken tandvlees en mucosa ofwel 5-ALA ophoopten of van nature fluorescerende porfyrinen bevatten die het tumorsignaal imiteerden.
Van operatiekamer naar laboratorium en terug
Toen de onderzoekers de verwijderde specimens op de operatietafel beeldden, veranderde het beeld enigszins. Buiten het lichaam werden sommige PpIX-gebaseerde kenmerken nuttiger om kanker van gezond weefsel te onderscheiden, wat wijst op een potentiële rol bij ‘chairside’ margescontroles. Toch, wanneer geavanceerde statistische modellen en machinaal leren werden toegepast, leunden de best presterende classificatoren voor zowel intraoperatieve als ex-operatieve gegevens zwaar op de natuurlijke autofluorescentiesignalen in plaats van op de toegevoegde kleurstof. Labelvrije FLIm behaalde op zichzelf respectabele nauwkeurigheid bij het onderscheiden van kanker van normaal weefsel, terwijl het toevoegen van PpIX weinig toevoegde en soms verwarring veroorzaakte.
Wat dit betekent voor toekomstige operaties
Voor huisdiereigenaren en uiteindelijk menselijke patiënten is de belangrijkste boodschap dat chirurgen ooit een lichtgebaseerd hulpmiddel kunnen hebben dat hen helpt te zien waar kanker eindigt en gezond weefsel begint, zonder afhankelijk te zijn van extra geneesmiddelen of kleurstoffen. Dit werk bij honden—een realistisch groot-diermodel van menselijke orale kanker—laat zien dat de eigen fluorescerende handtekeningen van het lichaam voldoende kunnen zijn om beslissingen in de operatiekamer te sturen. Het toevoegen van 5-ALA en PpIX verbeterde de nauwkeurigheid in deze context niet genoeg om de extra kosten, complexiteit en mogelijke bijwerkingen te rechtvaardigen. De auteurs concluderen dat toekomstige inspanningen zich zouden moeten richten op het verfijnen van labelvrije fluorescentielevensduurbeeldvorming zelf—mogelijk met analyses toegespitst op specifieke anatomische locaties—in plaats van het najagen van meer contrastmiddelen. Als dit succesvol is, zou zulke technologie heroperaties kunnen verminderen en meer normaal weefsel kunnen behouden terwijl de kanker toch onder controle blijft.
Bronvermelding: Goldschmidt, S., Marcu, L., Ehrlich, K. et al. Label-free fluorescence lifetime imaging can distinguish cancer from healthy tissue in spontaneously occurring canine oral tumors. Sci Rep 16, 6077 (2026). https://doi.org/10.1038/s41598-026-37001-3
Trefwoorden: beeldvorming van mondkanker, orale tumoren bij honden, fluorescente levensduur, chirurgische marges, 5-ALA PpIX