Clear Sky Science · nl
Ampliconsequencing met Oxford Nanopore-technologie als diagnostisch alternatief voor kleine herkauwerslentivirussen bij schapen
Verborgen infecties in alledaagse schapen
Schapen wereldwijd dragen vaak stilletjes virussen met zich mee die hun gezondheid aantasten, hun levensduur verkorten en boeren geld kosten — vaak zonder duidelijke symptomen gedurende jaren. Deze studie onderzoekt een nieuwe manier om die verborgen infecties op te sporen met behulp van draagbare DNA-sequencingtechnologie, en biedt daarmee een mogelijke doorbraak in hoe we dierenwelzijn, boerene inkomsten en zelfs voedselzekerheid beschermen.
Een trage, kostbare ziekte die moeilijk te zien is
Het onderzoek richt zich op kleine herkauwerslentivirussen (SRLV), een groep virussen die schapen en geiten infecteren. Bij schapen veroorzaken ze Maedi-Visna, een langdurige infectie die ademhalingsproblemen, artritis, hersenziekte en chronische uierontsteking kan veroorzaken. Veel geïnfecteerde dieren tonen nooit duidelijke symptomen, maar het virus verlaagt toch de melkproductie, verhoogt het aantal lamsterfte en dwingt tot vroeg slachten. In sommige Europese melkflokken, onder andere in Spanje en Griekenland, kan ongeveer de helft van de dieren geïnfecteerd zijn, wat dit tot een van de belangrijkste schaapziekten op intensieve bedrijven maakt.
Waarom huidige tests veel geïnfecteerde dieren missen
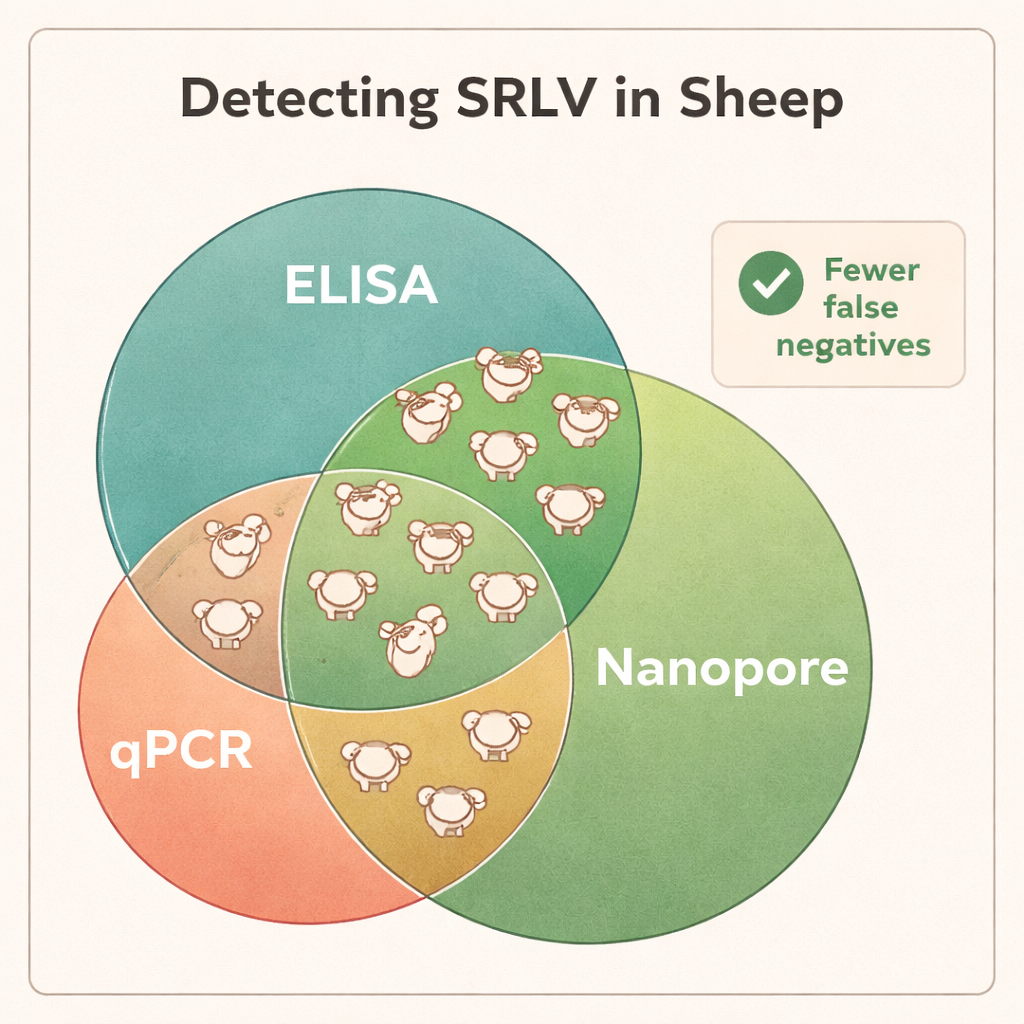
Tegenwoordig vertrouwen bedrijven voornamelijk op bloedtesten die naar antilichamen zoeken (ELISA) of op standaard DNA-tests (qPCR) om te bepalen welke dieren geïnfecteerd zijn en uit de kudde moeten worden verwijderd. Maar SRLVs muteren en recombineren snel, waardoor veel licht verschillende virusvarianten ontstaan. Sommige varianten worden slecht herkend door antilichaamtests, en sommige geïnfecteerde schapen ontwikkelen helemaal geen sterke antilichaamreactie. qPCR, dat zich richt op korte en zeer specifieke stukjes viraal DNA, kan ook falen als die doelregio’s veranderen. Als gevolg daarvan testen veel werkelijk geïnfecteerde dieren negatief en blijven in de kudde, waar ze het virus stil verspreiden.
Realtime DNA-lezen om het virus te vinden
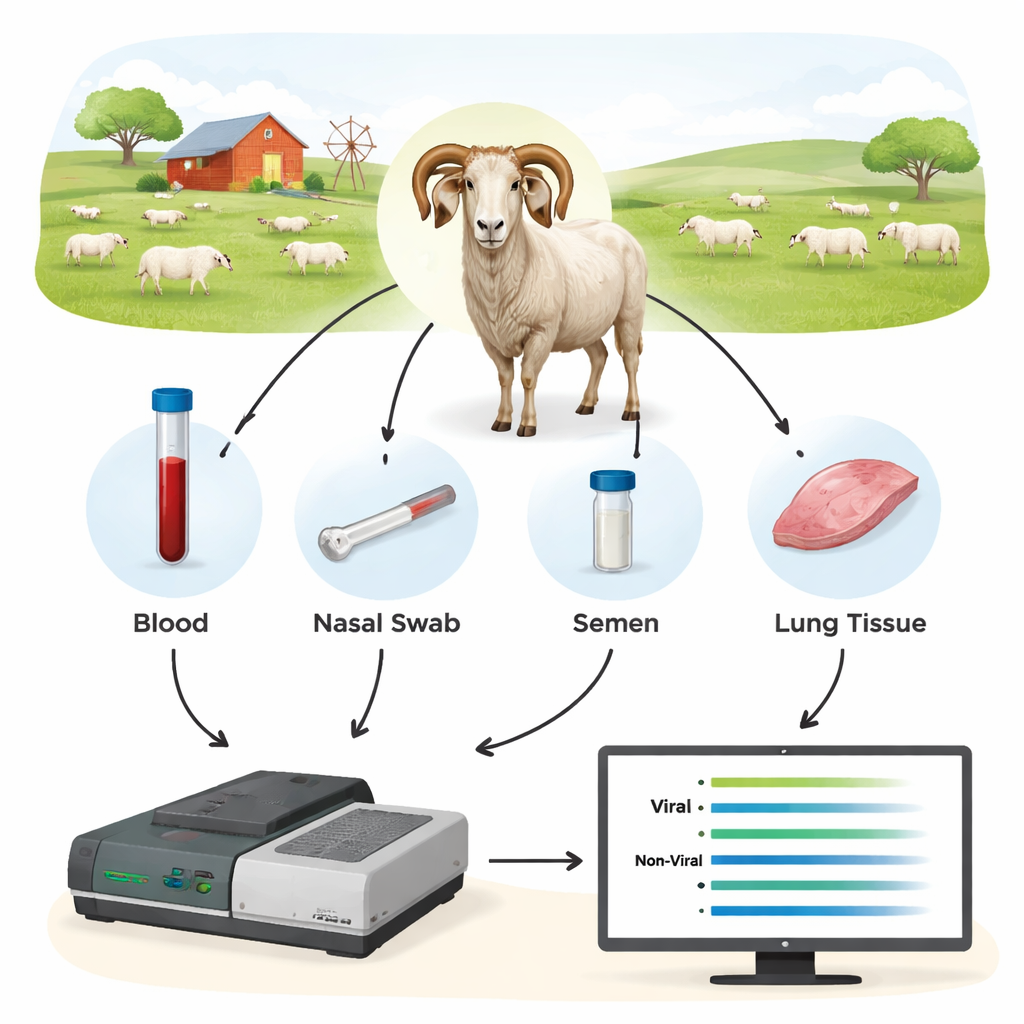
De onderzoekers testten een derde-generatie DNA-methode genaamd Oxford Nanopore-sequencing als een nieuw type diagnostisch instrument. In plaats van naar één klein stukje viraal DNA te zoeken, versterkten ze eerst langere stukken van belangrijke virusgenen uit de monsters van de dieren en sequentieerden vervolgens die fragmenten in realtime op een Nanopore-apparaat. Ze verzamelden bloed, neusswabs, sperma en cellen uit bloed en longen van 44 rammen en aanvullende schapen, van wie velen al met conventionele methoden waren getest. Door te focussen op virale regio’s die relatief geconserveerd zijn maar nog steeds lang genoeg om het exacte stamtype te onthullen, kon het team zowel infecties detecteren als bepalen welke virusvarianten aanwezig waren.
Bloed werkt het beste — en vindt wat andere tests missen
Sequencing toonde aan dat DNA uit volledig bloed het meest betrouwbare materiaal was om SRLV op te sporen, hoewel het virus voornamelijk in een kleine subset van witte bloedcellen leeft. Longweefsel van sterk geïnfecteerde dieren leverde zeer hoge hoeveelheden viraal DNA op, maar zulke monsters zijn alleen beschikbaar na slacht. Daarentegen leverden neusswabs, sperma en gezuiverde witte bloedcellen te weinig viraal materiaal voor consistente diagnose. Toen de wetenschappers Nanopore-resultaten vergeleken met de standaard ELISA- en qPCR-tests, waren de verschillen opvallend: Nanopore-sequencing bevestigde infectie bij alle ELISA-positieve rammen, maar onthulde ook dat veel ELISA-negatieve dieren eigenlijk geïnfecteerd waren. Over verschillende kuddes bleek ongeveer 40–45% van de dieren die door ELISA als “negatief” waren aangemerkt het virus te dragen, en qPCR miste een nog groter aandeel. De sequencingdata toonden ook co-infecties met verschillende SRLV-typen in sommige rammen aan — informatie die traditionele tests niet gemakkelijk kunnen leveren.
Van simpele ja/nee-antwoorden naar diepere inzichten
Omdat Nanopore de daadwerkelijke virale sequenties leest, kan het verder gaan dan een eenvoudige ja-of-nee-diagnose. Het team gebruikte de gegevens om virusstammen te vergelijken, stambomen van de circulerende virussen in hun kuddes te bouwen, en subtiele verschillen in virale eiwitten te bestuderen die kunnen verklaren waarom sommige dieren ontsnappen aan detectie door standaard ELISA-kits. Ze toonden aan dat bepaalde versies van een sleutelviruseiwit, dat door commerciële antilichaamtests wordt aangetast, duidelijk verschillen tussen antilichaam-positieve en antilichaam-negatieve dieren. In de loop van de tijd kan zulke informatie zowel serologische tests verfijnen als fokprogramma’s ondersteunen die dieren selecteren die van nature resistenter zijn tegen infectie.
Wat dit betekent voor boeren en diergezondheid
Voor niet-specialisten is de kernboodschap simpel: door langere stukken viraal DNA direct te lezen kan Nanopore-sequencing meer geïnfecteerde schapen sneller en nauwkeuriger opsporen dan de huidige routinetests. Het vertelt ons ook welke exacte virusstammen in een kudde aanwezig zijn. Hoewel deze aanpak nog complexer en duurder is dan een enkele bloedtest, wordt de technologie sneller, goedkoper en draagbaarder. Als deze methode in beheersprogramma’s wordt geïntegreerd, kan ze het aantal “verborgen” dragers sterk verminderen, het ontwerp van vaccins en tests verbeteren en de fok van resistentere dieren ondersteunen — wat schapenhouderij duurzamer en diervriendelijker kan maken.
Bronvermelding: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Trefwoorden: schaapgezondheid, lentivirus, nanopore-sequencing, veterinaire diagnostiek, Maedi-Visna