Clear Sky Science · nl
Breedwerkende antimicrobiële nanodeeltjes met lage toxiciteit ter voorkoming van biofilmvorming op urologische hulpmiddelen
Waarom medische implantaten ons soms in de steek laten
De moderne geneeskunde is afhankelijk van kunststof buizen en implantaten om urine af te voeren, geblokkeerde nieren te ondersteunen en seksuele functie te herstellen. Tegelijkertijd kunnen deze dezelfde apparaten bacteriën aantrekken, die plakkerige beschermende gemeenschappen vormen die biofilms worden genoemd. Zodra een biofilm zich vormt, zijn infecties moeilijk te behandelen, wat artsen vaak dwingt het hulpmiddel te verwijderen of te vervangen. Deze studie onderzoekt een nieuw soort microscopische coating, gemaakt van goud en zilver omhuld met een koolstoflaag, die is ontworpen om die biofilms te stoppen voordat ze beginnen.
Het verborgen probleem van kleverige ziekteverwekkers
Katheters, ureterstents en opblaasbare penisprotheses helpen honderdduizenden patiënten, maar bieden ook ideale vestigingsplaatsen voor microben. Bacteriën hechten zich aan het oppervlak van het apparaat en scheiden een lijmachtige matrix van suikers, eiwitten en vetten uit, waardoor een vesting ontstaat die hen beschermt tegen antibiotica en het immuunsysteem. Daardoor vormen door apparaten veroorzaakte infecties meer dan een kwart van alle ziekenhuisinfecties en kosten ze jaarlijks honderden miljoenen dollars. Huidige beschermende coatings op basis van antibiotica of simpel zilver slagen er niet goed in biofilms op de lange termijn te voorkomen en kunnen bijdragen aan toenemende antibioticumresistentie.
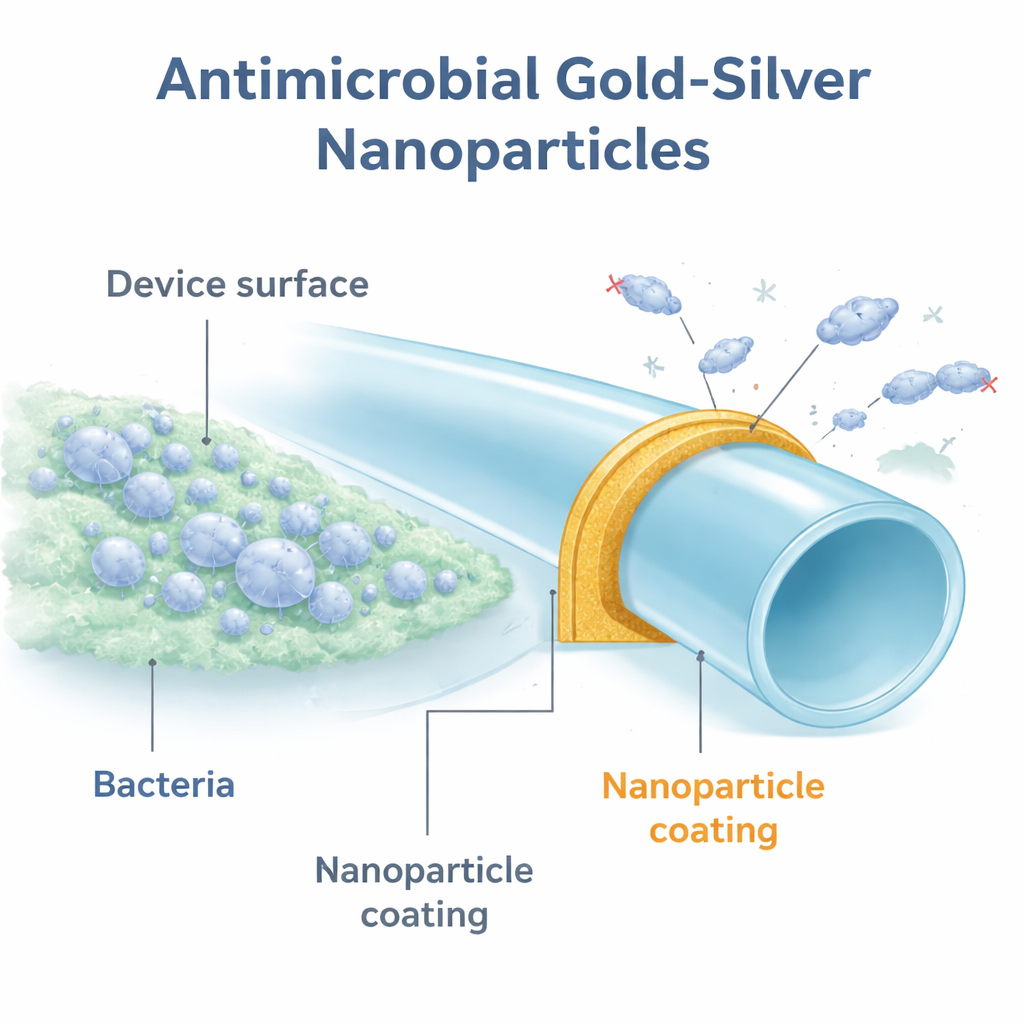
Een nieuw soort beschermend pantser
De onderzoekers richtten zich op kleine metalen deeltjes van slechts enkele miljardsten van een meter breed. Deze nanodeeltjes werden opgebouwd rond een koolstofkooi-materiaal genaamd polyhydroxyfullereen, dat bekendstaat als niet-toxisch en de prestaties van bepaalde metalen kan verbeteren. Ze maakten verschillende versies met verschillende metalen en coaten kleine schijfjes van polyurethaan, een kunststof die vaak in urologische hulpmiddelen wordt gebruikt. Toen ze deze gecoate schijfjes testten tegen een standaardstam van Escherichia coli, toonden alleen de deeltjes met zilver sterke antibacteriële effecten. De duidelijke uitblinker was een goud–zilverkombinatie, aangeduid als GSNPs, die het aantal bacteriën met maximaal 100.000 keer verminderde vergeleken met ongecoat plastic.
Het tegengaan van urologische ziekteverwekkers uit de praktijk
Om te zien of dit effect zich ook buiten een laboratoriumstam voordeed, testte het team hun beste coating tegen zes soorten bacteriën die rechtstreeks waren geïsoleerd van geïnfecteerde ureterstents en penisprotheses. Dit betrof zowel Gram-positieve als Gram-negatieve soorten die bekendstaan om hardnekkige infecties te veroorzaken. Bij bacteriëniveaus vergelijkbaar met die bij patiënten, behaalden de GSNP-gecoate oppervlakken een 100% vermindering van zowel vrij zwevende als aan het oppervlak gehechte bacteriën voor alle geteste stammen. In aparte experimenten stelden de onderzoekers bacteriën bloot aan verschillende nanodeeltjesconcentraties in vloeistof en schatten ze in hoeveel GSNP nodig was om groei te stoppen. Alle stammen werden volledig geremd bij of onder 3 microgram GSNP per milliliter vloeistof, waarbij voor sommige Gram-positieve organismen iets hogere hoeveelheden nodig waren.
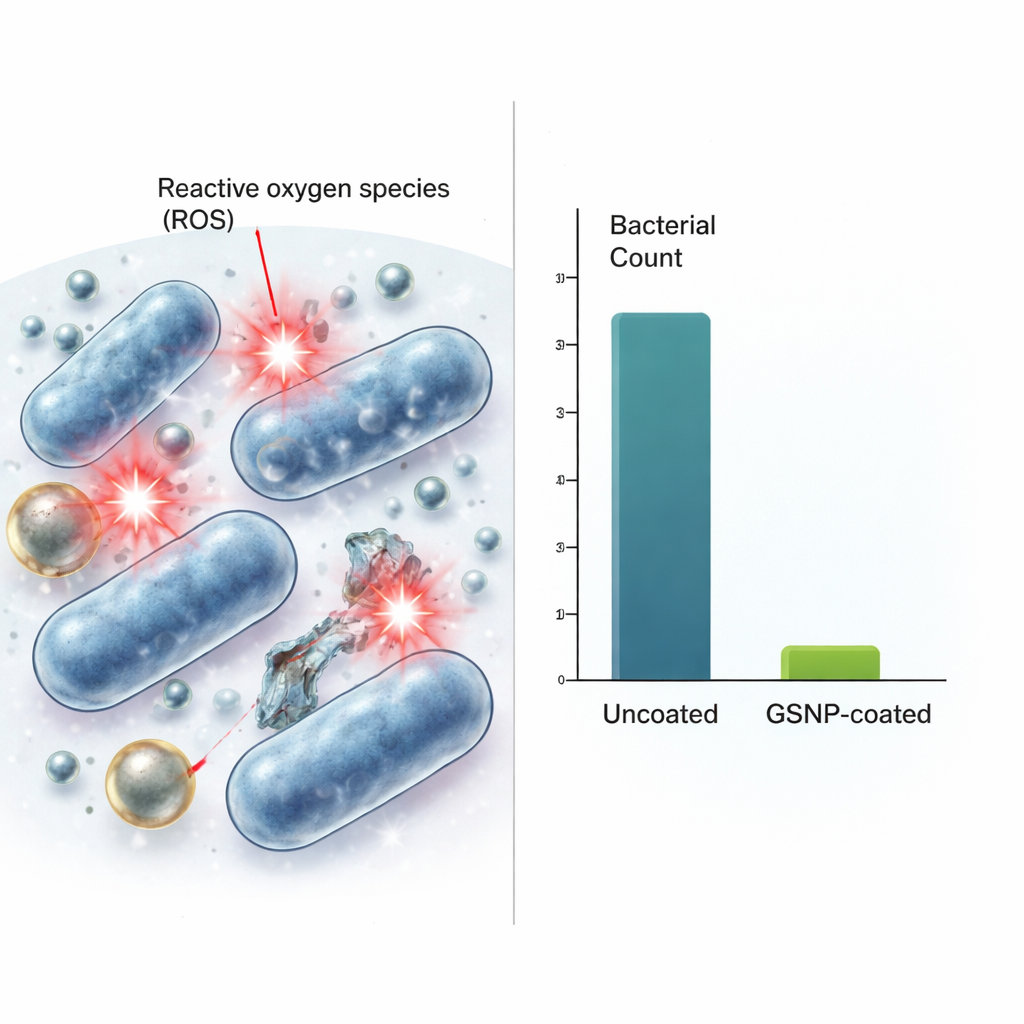
Hoe ze werken en hoe veilig ze zijn
Het team onderzocht vervolgens hoe deze coatings bacteriën doden en of ze ook menselijke cellen kunnen schaden. Hun gegevens wijzen op reactieve zuurstofsoorten—chemisch reactieve vormen van zuurstof—als een belangrijk onderdeel van het doodmechanisme. Hoewel de nanodeeltjes op zichzelf deze reactieve moleculen niet genereerden, produceerden bacteriën die aan GSNPs waren blootgesteld veel hogere niveaus dan onbehandelde bacteriën, wat suggereert dat de deeltjes schadelijke chemie in of nabij de microben opwekken. Wanneer muisfibroblasten werden blootgesteld aan vergelijkbare of hogere concentraties GSNPs, bleef meer dan 80% van de cellen leven bij de worst-case antibacteriële dosis. Met andere woorden: de niveaus die bacteriën uitroeiden hadden slechts een beperkte impact op zoogdiercellen. De GSNPs waren ook dramatisch effectiever dan een commercieel goud–zilver nanodeeltjeproduct dat zij naast elkaar testten en bereikten bij gelijkwaardige doses grofweg een miljoenvoud grotere bacteriereductie.
Wat dit voor patiënten zou kunnen betekenen
Hoewel dit werk in het laboratorium is uitgevoerd en nog niet in dieren of mensen, wijzen de bevindingen op een veelbelovende nieuwe strategie voor veiligere medische implantaten. Een dunne laag GSNPs op een katheter of prothese zou brede bescherming tegen veel verschillende bacteriën kunnen bieden, de noodzaak van verwijdering van het apparaat kunnen verminderen, en dat doen zonder te steunen op traditionele antibiotica. De coating gebruikt weinig metaal, vertoont in initële tests relatief lage toxiciteit en is eenvoudig te vervaardigen. Met verdere techniek om de langetermijnstabiliteit te verbeteren en zorgvuldige tests in realistische modellen, zouden deze goud–zilveren nanodeeltjescoatings kunnen helpen vitale urologische hulpmiddelen voor patiënten te laten werken in plaats van een thuisbasis voor infectie te worden.
Bronvermelding: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Trefwoorden: biofilm, urologische hulpmiddelen, antimicrobiële coating, nanodeeltjes, goud-zilver