Clear Sky Science · nl
Kwantiatieve proteomische analyse van plasma na remote ischemic conditioning bij acuut ischemisch beroerte
Waarom het knijpen van een arm de hersenen kan helpen beschermen
Wanneer iemand een beroerte krijgt door een afgesloten bloedvat, bedreigt elke minuut zonder bloedtoevoer hersencellen. Standaardbehandelingen proberen het afgesloten vat weer open te krijgen, maar veel patiënten komen te laat of komen niet in aanmerking. Onderzoekers verkennen een verrassend eenvoudige aanvullende therapie: kortstondig de bloedtoevoer naar een arm of been afklemmen met een bloeddrukmanchet, een strategie die remote ischemic conditioning (RIC) wordt genoemd. Deze studie stelt een cruciale vraag voor het vertalen van die gedachte naar echte behandeling: wat verandert RIC precies in het bloed van beroertepatiënten, en kunnen die veranderingen aanwijzingen geven wie er het meest baat bij heeft?
Een zachte stresssignaal van ledemaat naar hersenen
RIC werkt door herhaaldelijk een manchet op een ledemaat op te blazen gedurende een paar minuten en daarna te laten leeglopen, waardoor korte, onschadelijke periodes van verminderde bloedstroom ontstaan. Dierexperimente en vroege klinische onderzoeken suggereren dat deze “gecontroleerde stress” signalen naar verre organen, waaronder de hersenen, kan sturen om beschermende programma’s aan te zetten. In een grote klinische studie genaamd RICAMIS deden patiënten met een matige ischemische beroerte die naast de gebruikelijke zorg RIC kregen het beter na 90 dagen dan degenen die alleen de gebruikelijke zorg ontvingen. Een andere studie (RESIST) zag dit voordeel echter niet, waardoor artsen onzeker blijven over wanneer en voor wie RIC echt werkt. De huidige studie duikt in het bloed van patiënten om naar moleculaire aanwijzingen te zoeken — meetbare eiwitten, of biomarkers, die in de tijd veranderen met RIC.
Het bloed van patiënten volgen tijdens hun ziekenhuisopname
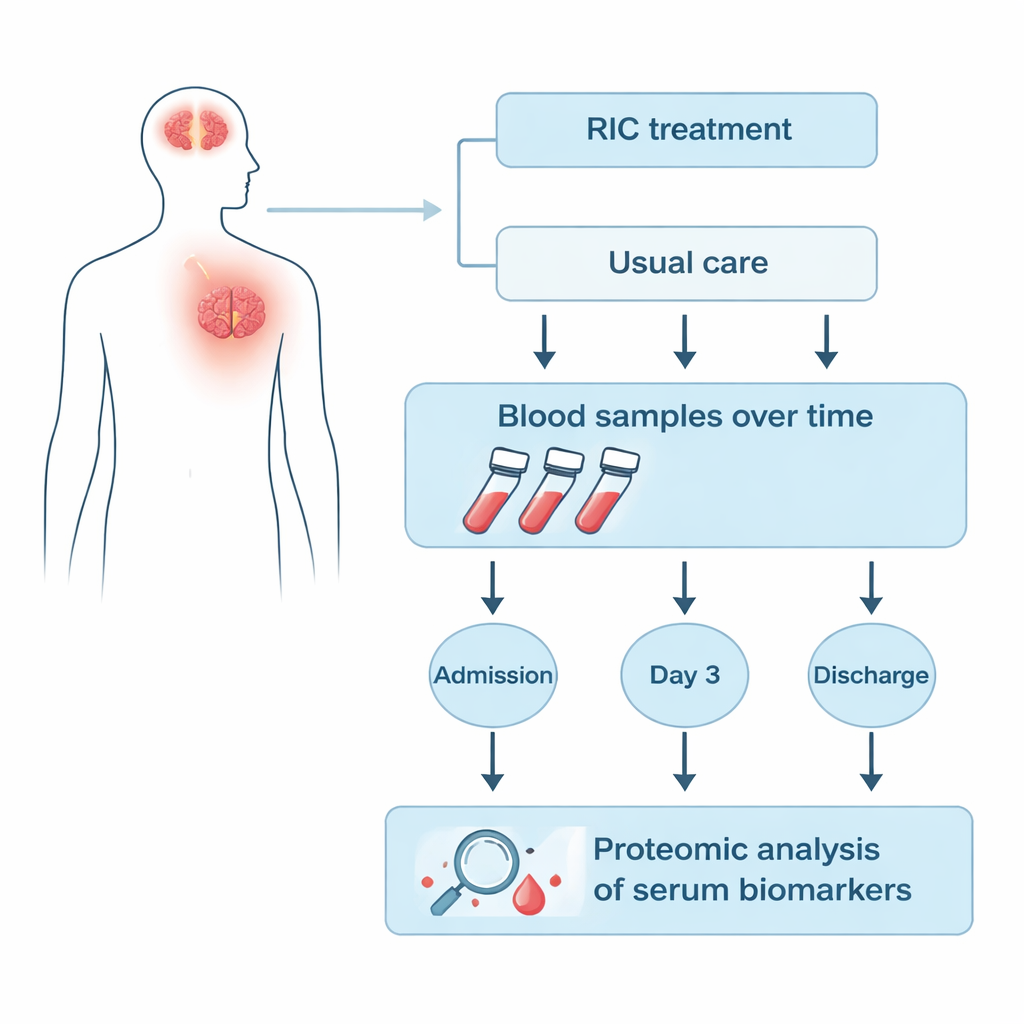
De onderzoekers concentreerden zich op 25 patiënten uit de RICAMIS‑trial bij wie bloedmonsters op drie momenten werden verzameld: bij opname, drie dagen nadat de behandeling was toegewezen, en bij ontslag uit het ziekenhuis. Negen patiënten kregen RIC plus gebruikelijke zorg, terwijl zestien alleen gebruikelijke zorg ontvingen. Met een techniek die kwantitatieve proteomica wordt genoemd, mat het team honderden eiwitten in het serumgedeelte van het bloed in één keer, in plaats van slechts een paar vooraf geselecteerde markers te onderzoeken. Vervolgens vergeleken ze hoe het niveau van elk eiwit in de loop van de tijd steeg of daalde in de RIC‑groep versus de controlegroep om signaturen te vinden die specifiek aan RIC gekoppeld waren.
Negen opvallende signalen in de bloedbaan
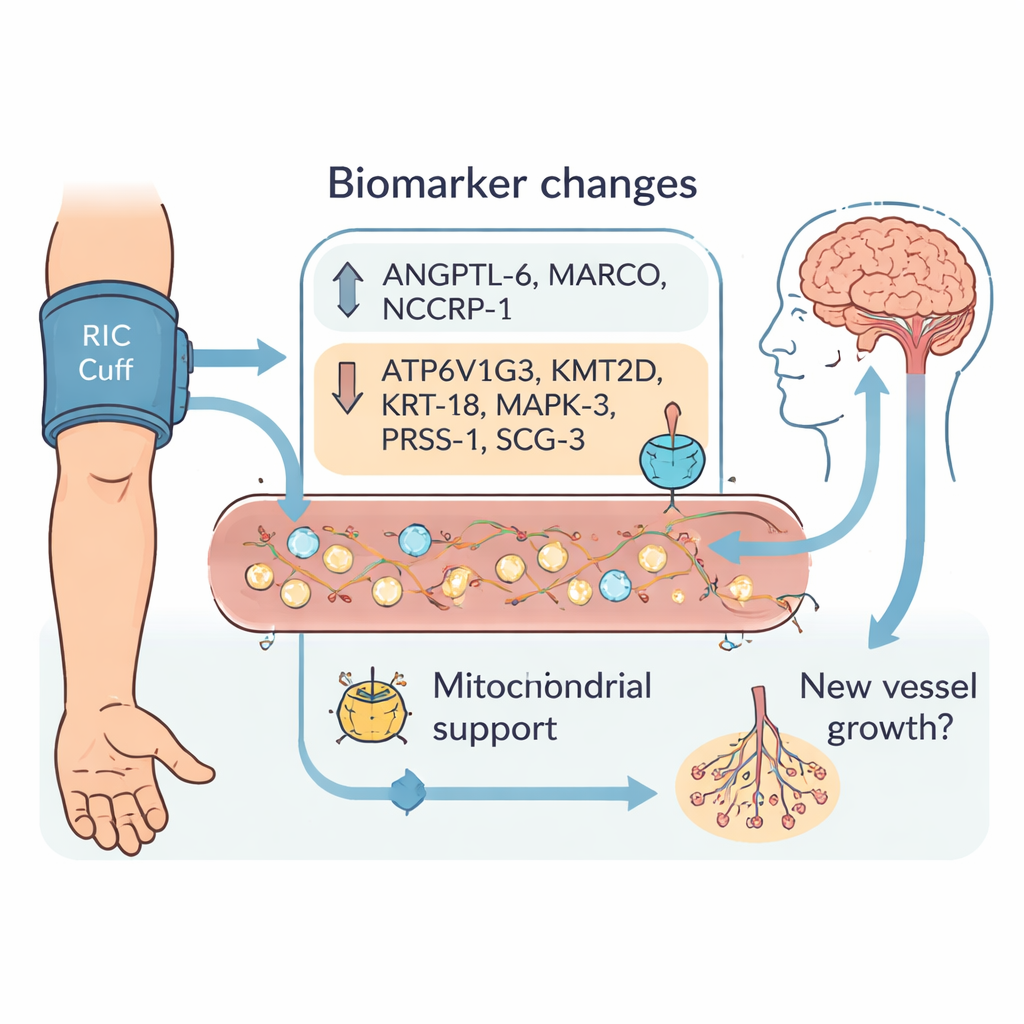
Gedurende de ziekenhuisopname verschoof tientallen eiwitten op verschillende manieren tussen de twee groepen. Na zorgvuldige filtering benadrukte het team negen biomarkers waarvan de veranderingen van opname naar dag 3 en naar ontslag duidelijk RIC‑behandelde patiënten van controles scheidden. Drie eiwitten — ANGPTL‑6, MARCO en NCCRP‑1 — namen meer toe bij RIC. Zes anderen — ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 en SCG‑3 — hadden de neiging te dalen. Veel van deze moleculen zijn betrokken bij hoe cellen energie beheren in hun kleine energiecentrales, de mitochondriën, of bij hoe nieuwe bloedvaten groeien en zich herstructureren. Dit past bij het idee dat RIC niet louter neuronen tegen schade beschermt, maar mogelijk beschadigde hersengebieden helpt reorganiseren, hun bloedvoorziening te herstellen en functie terug te winnen over dagen tot weken.
Aanwijzingen over energiegebruik en nieuwe vaatgroei
Om beter te begrijpen wat deze negen eiwitten mogelijk doen, koppelden de auteurs ze aan bekende biologische routes. Twee ervan, KMT2D en MAPK‑3, zijn verbonden met hoe DNA is verpakt en hoe genen aan of uit worden gezet, vooral in programma’s gerelateerd aan vaatgroei. Anderen, zoals ATP6V1G3 en KRT‑18, zijn in eerder werk in verband gebracht met het behoud van gezonde mitochondriën en het beschermen van hartweefsel na schade. Gezamenlijk wijzen deze patronen erop dat RIC het lichaam kan aanzetten tot efficiënter energiegebruik en het bevorderen van groei of herschikking van bloedvaten — wat mogelijk de bloedstroom rond het door de beroerte beschadigde gebied verbetert. Tegelijkertijd kunnen sommige markers, zoals NCCRP‑1 en MARCO, de acute stress‑ en immuunreacties van het lichaam op de manchetinflatie zelf weerspiegelen, wat benadrukt dat RIC een complexe, lichaamsbrede reactie teweegbrengt.
Wat dit betekent voor toekomstige beroertezorg
Deze kleine verkennende studie kan niet precies bewijzen hoe RIC de hersenen beschermt en betrof slechts 25 patiënten uit één land, dus de bevindingen moeten worden bevestigd in veel grotere en diverse groepen. Toch is het identificeren van een korte lijst van negen eiwitten die consequent in tegengestelde richtingen bewegen met en zonder RIC een belangrijke stap. In de toekomst zouden zulke biomarkers artsen kunnen helpen snel te bepalen of RIC bij een bepaalde patiënt effect heeft, de keuze sturen wie het zou moeten krijgen, of zelfs geneesmiddelen inspireren die de gunstige effecten nabootsen zonder de manchet. Voor nu versterkt het werk een eenvoudig maar krachtig idee: door veilig een deel van het lichaam te belasten, kunnen we de hersenen mogelijk aanzetten tot een actievere, veerkrachtigere toestand die beter kan herstellen na een beroerte.
Bronvermelding: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Trefwoorden: acuut ischemisch beroerte, remote ischemic conditioning, serum biomarkers, proteomische analyse, neuroprotectie