Clear Sky Science · nl
Een pro-inflammatoire subpopulatie neutrofielen veroorzaakt intestinale ischemie–reperfusieletsel via de ATF4-gemedieerde endoplasmatisch reticulum stressroute
Wanneer bloedtoevoer de darmen schaadt
Chirurgen en intensivecare-artsen staan al lang voor een gevaarlijk raadsel: wanneer de bloedtoevoer naar de darm wordt afgesneden en vervolgens wordt hersteld, kan het herstellen van de doorbloeding zelf de darmwand ernstig beschadigen. Dit proces, intestinale ischemie–reperfusieletsel genoemd, kan leiden tot levensbedreigende complicaties zoals sepsis en multiple orgaanfalen. De hier samengevatte studie laat zien dat niet alle immuuncellen die ter plaatse komen gelijk zijn — een bijzonder agressieve subgroep van witte bloedcellen speelt een hoofdrol in het veranderen van een levensreddende reactie in een schadelijke.
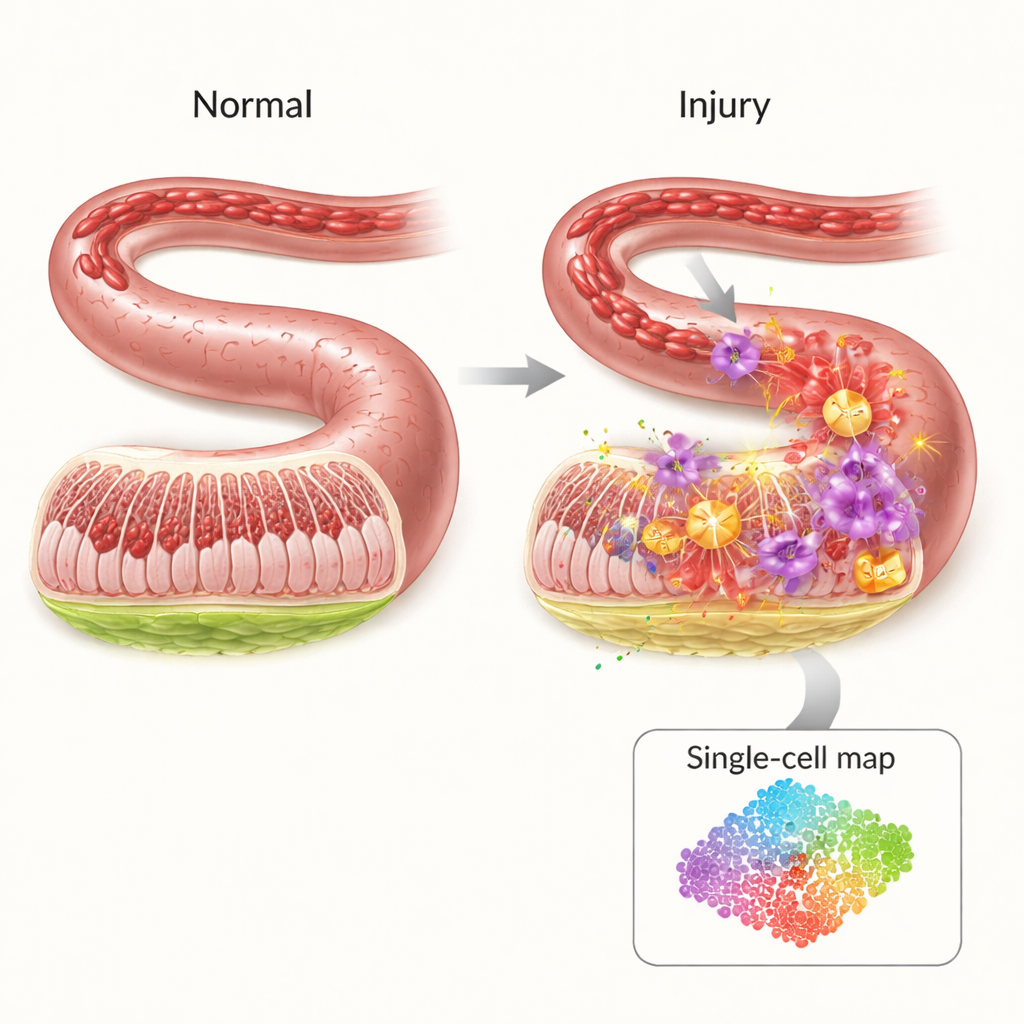
De kwetsbare beschermende wand van de darm
De binnenkant van de darm is bekleed met een dun maar hoog georganiseerd barrièresysteem dat bacteriën en toxines in de darm houdt terwijl voedingsstoffen doorgelaten worden. Wanneer de bloedstroom onderbroken wordt — bijvoorbeeld tijdens shock, grote chirurgie of ernstig trauma — wordt deze barrière van zuurstof beroofd. Verrassend genoeg ontstaat het meeste letsel niet tijdens de gebrek aan bloed zelf, maar wanneer de circulatie terugkeert. De plotselinge toestroom van zuurstof en immuuncellen ontketent een storm van ontstekingssignalen en reactieve moleculen die gaten in de darmwand kunnen slaan, waardoor ziekteverwekkers in de bloedbaan kunnen lekken. Ondanks het klinische belang hebben artsen momenteel weinig gerichte behandelingen om deze cascade te voorkomen.
Inzoomen op individuele cellen
Om te achterhalen wie wat doet tijdens deze crisis, gebruikten de onderzoekers single-cell RNA-sequencing, een techniek die afleest welke genen actief zijn in duizenden individuele cellen tegelijk. In een muismodel van intestinale ischemie–reperfusie vergeleken ze gewonde darmen met gezonde en brachten 19 belangrijke celtypen in kaart. Ze vonden dat bepaalde immuuncellen — met name neutrofielen en inflammatoire monocyten — dramatisch toenamen na letsel, terwijl beschermende cellen zoals T-cellen, B-cellen en natural killer-cellen afnamen. Communicatienetwerken tussen celtypen verschoof ook, waarbij neutrofielen naar voren kwamen als centrale knooppunten die veel ontstekingssignalen verstuurden en ontvingen, wat wijst op hun sleutelrol in het veroorzaken van schade.
Een schadelijke subgroep van eerstelijnsresponders
Neutrofielen behoren tot de snelste eerstelijnsresponders van het lichaam, ze stormen via de bloedbaan naar plekken om infecties aan te pakken en afval op te ruimen. Maar deze studie toont aan dat binnen de neutrofielenpopulatie een bijzonder agressieve subgroep verantwoordelijk is voor veel van de nevenschade in de darm. Wanneer de wetenschappers neutrofielen bij muizen uitputten voordat ze ischemie–reperfusie opwekten, vertoonden de dieren minder darmverkorting, lagere niveaus van letselmarkeringen in het bloed, een betere weefselverschijning onder de microscoop en strakkere sluitende eiwitten in de darmwand. In co-cultuurexperimenten schaadden neutrofielen afkomstig van gewonde muizen direct darmcellen: ze verlaagden hun overleving, verhoogden celdood en verstoorden sleutel‑"rits"-eiwitten die de intestinale barrière intact houden.
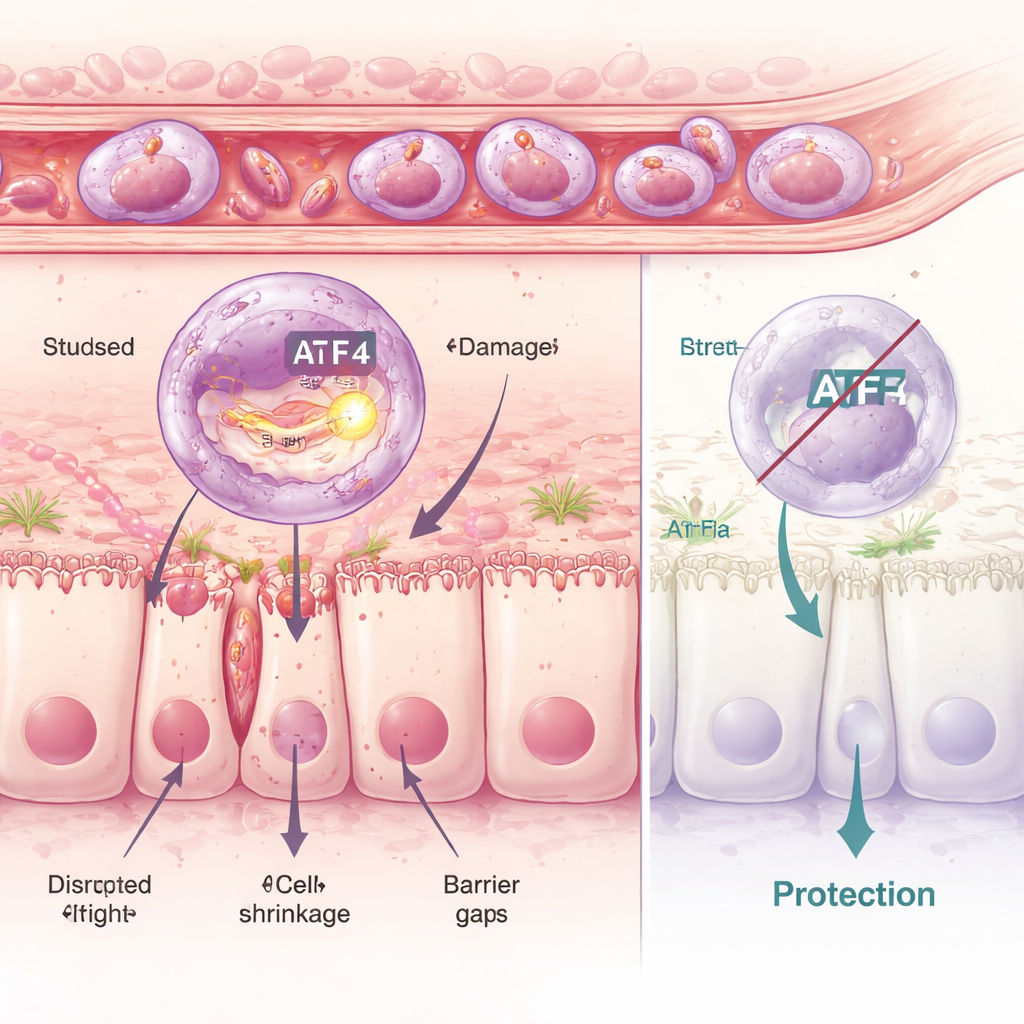
Stress binnenin cellen: wanneer kwaliteitscontrole faalt
Dieper gravend onderzochten de onderzoekers neutrofielen één voor één en identificeerden zes verschillende subgroepen. Eén cluster, aangeduid als C5, stak eruit door zijn sterke inflammatoire profiel en door het activeren van een moleculair stressprogramma in een structuur die het endoplasmatisch reticulum wordt genoemd, de eiwitvouwwerkplaats van de cel. Een belangrijke regulator van dit programma is een eiwit genaamd ATF4. In de schadelijke C5-cellen waren ATF4 en zijn doelgenen sterk actief. Door geneesmiddelen te gebruiken die dit interne stressantwoord ofwel opvoerden ofwel dempten, toonde het team aan dat meer stress meer darmschade betekende, terwijl het blokkeren ervan de intestinale barrière beschermde. Muizen die genetisch zo gemodificeerd waren dat ze geen ATF4 konden maken, waren grotendeels beschermd: zelfs wanneer stress‑inducerende geneesmiddelen werden toegediend, konden hun neutrofielen het schadelijke programma niet volledig uitvoeren en bleef de darmwand veel beter intact.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk schetsen deze bevindingen een duidelijk beeld voor niet‑specialisten: tussen de zwerm immuuncellen die de darm binnenstromen wanneer de bloedtoevoer terugkeert, gedraagt een specifieke, stress‑geprimede subgroep neutrofielen zich als een te fanatieke opruimploeg die het gebouw afbreekt samen met het puin. Hun destructieve kracht berust op een ingebouwd stresspad dat binnen de cellen door ATF4 wordt gecontroleerd. Dit pad temperen — zonder alle neutrofielen uit te schakelen — zou een manier kunnen bieden om de darm te beschermen tijdens risicovolle gebeurtenissen zoals grote chirurgie, ernstige infectie of trauma. Hoewel verder onderzoek nodig is om deze resultaten bij mensen te bevestigen en veilige, precieze geneesmiddelen te vinden, opent de studie een veelbelovende weg naar therapieën die de darmbarrière intact houden wanneer patiënten die het hardst nodig hebben.
Bronvermelding: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Trefwoorden: intestinale barrière, ischemie reperfusie, neutrofielen, endoplasmatisch reticulum stress, ATF4