Clear Sky Science · nl
CKAAKN-peptide-geconjugeerde langcirculerende nanoliposomen voor gerichte aflevering van oridonine aan alvleesklierkankers
Waarom dit onderzoek ertoe doet
Alvleesklierkanker is een van de dodelijkste vormen van kanker, deels omdat ze meestal laat wordt ontdekt en vaak resistent is tegen standaardchemotherapie. Deze studie onderzoekt een slimmere manier om een uit kruiden afgeleid anti-kankerverbinding, oridonine, rechtstreeks naar alvleeskliertumoren te brengen met behulp van kleine vetachtige belletjes die nanoliposomen worden genoemd. Door meer van het geneesmiddel bij de tumor te krijgen terwijl gezond weefsel wordt gespaard, wijst dit werk op zachtere, effectievere behandelingsopties voor een kanker die die dringend nodig heeft.
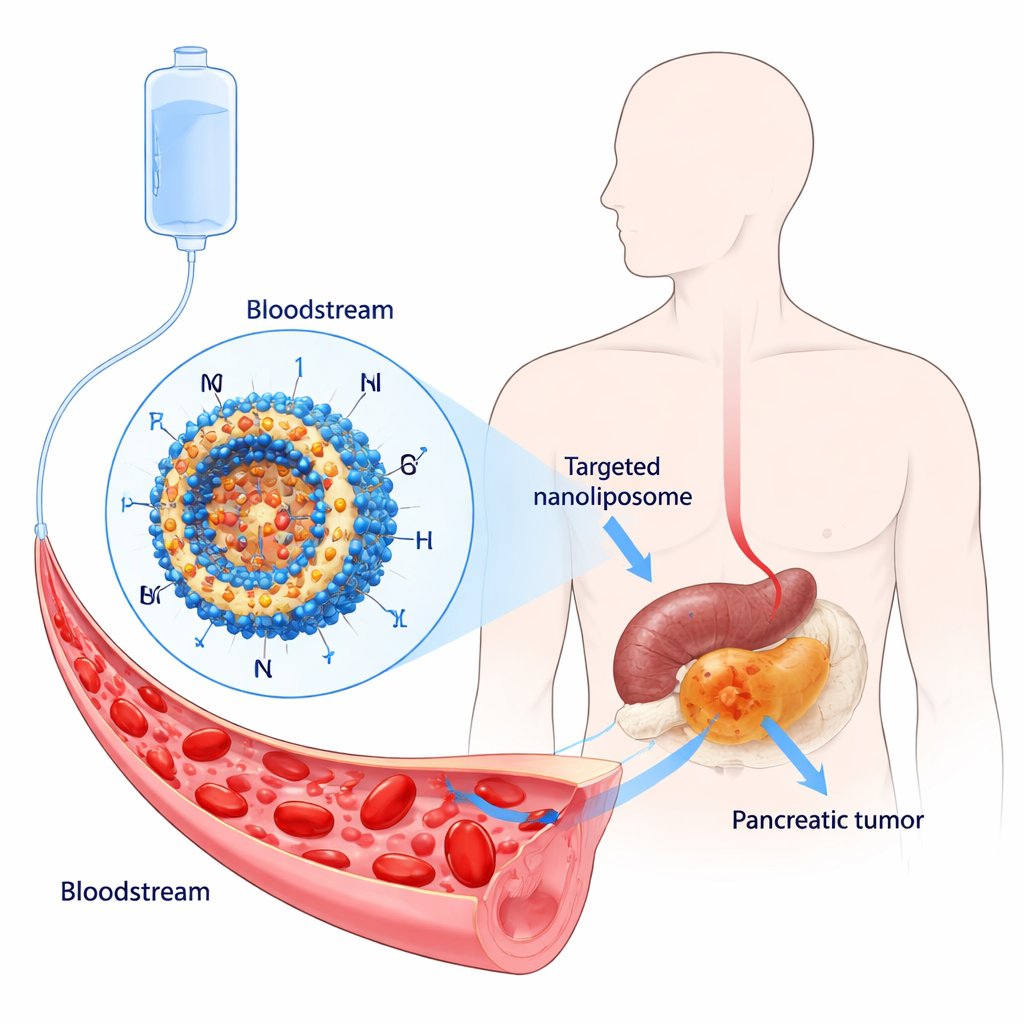
Een dodelijke kanker die moeilijk te behandelen is
Alvleesklierkanker heeft de grimmige bijnaam “koning der kankers” gekregen omdat de overlevingscijfers voor de meeste patiënten nog steeds in het enkelcijferige percentage liggen. Slechts een klein deel van de mensen komt in aanmerking voor een operatie en zelfs dan komt de tumor bij velen terug. Chemotherapiemiddelen zoals paclitaxel en cisplatine kunnen de ziekte vertragen, maar veroorzaken sterke bijwerkingen en tumorcellen worden vaak resistent. Onderzoekers zoeken daarom naar medicijnen die zowel preciezer als minder toxisch zijn, samen met afgiftesystemen die het geneesmiddel concentreren in de tumor in plaats van het hele lichaam te overstromen.
Een kruidachtige molecule omzetten in moderne geneeskunde
Oridonine is een natuurlijke verbinding die wordt gewonnen uit de traditionele Chinese medicinale plant Rabdosia rubescens. Laboratoriumstudies hebben aangetoond dat het veel soorten kankercellen, waaronder pancreascellen, kan doden of hun groei kan vertragen door de celdeling te verstoren en geprogrammeerde celdood te induceren. Oridonine op zichzelf is echter moeilijk als geneesmiddel te gebruiken: het lost slecht op in water, wordt slecht opgenomen en kan bij hogere doses toxisch zijn. Om het potentieel te benutten, pakten de auteurs oridonine in nanoliposomen—kleine bolletjes gemaakt van lipiden die lijken op die in celmembranen—ontworpen om het geneesmiddel veilig door de bloedbaan te vervoeren en langzaam vrij te geven op de tumorlocatie.
Ontwerpen van een “stealth” homing-verpakking voor het geneesmiddel
Het team ontwikkelde een tweelaags afgiftesysteem. Eerst creëerden ze langcirculerende liposomen door het oppervlak te coaten met polyethyleenglycol (PEG), een flexibel, waterminend polymeer dat de deeltjes helpt immuuncellen te ontwijken en langer in het bloed te blijven. Vervolgens voegden ze een kort peptide toe, CKAAKN, dat fungeert als een hominglabel voor alvleesklierkanker. Dit peptide bootst een deel van het Wnt-signaleringspad na, dat in veel pancreastumoren abnormaal actief is, waardoor de gewijzigde liposomen (genoemd ORI@CPD-Lipo) zich kunnen hechten aan kankercellen die bijpassende receptoren tonen. De uiteindelijke deeltjes waren ongeveer 100 nanometer in diameter, bevatten veel oridonine en gaven het geneesmiddel langzaam vrij over vele uren in plaats van in één keer.
Hoe de gerichte deeltjes zich gedragen in cellen en dieren
In kweekproeven werden de met CKAAKN getagde liposomen veel efficiënter opgenomen door menselijke alvleesklierkankercellen dan door normale alvleeskliercellen, vooral tijdens de eerste paar uren van contact. Wanneer overtollig vrij CKAAKN-peptide werd toegevoegd als lokaas, namen de kankercellen minder deeltjes op, wat het idee ondersteunt dat er een specifieke bindingsstap betrokken is. Lege liposomen vertoonden lage toxiciteit en beschadigden geen rode bloedcellen, wat op een goede veiligheid wijst. Wanneer geladen met oridonine, doodden de gerichte liposomen kankercellen effectiever dan ofwel vrije oridonine of niet-gericht liposomen, en ze vertraagden sterker de migratie van kankercellen over een kras-“wond” in een schaal. Bij muizen met pancreastumoren bouwden fluorescein-gelabelde gerichte liposomen zich tot 48 uur in de tumor op en accumuleerden daar meer dan niet-gerichte liposomen, terwijl ze zoals verwacht grotendeels via de lever en milt werden uitgescheiden.
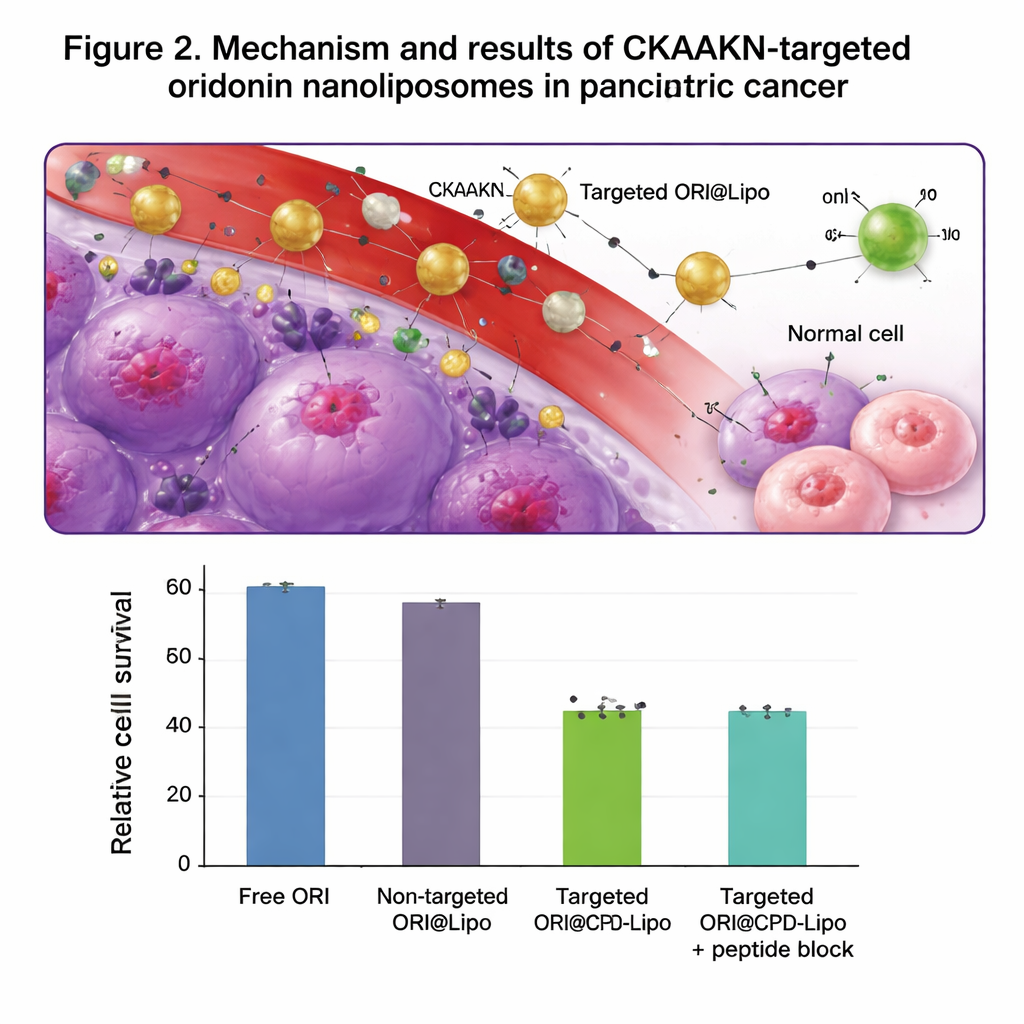
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Gezamenlijk tonen de resultaten aan dat het combineren van een traditioneel kruidachtig bestanddeel met een moderne, precieze afgiftewagen zijn antitumorkracht in laboratoriummodellen aanzienlijk kan vergroten. De met CKAAKN versierde, langcirculerende nanoliposomen leiden meer oridonine naar alvleesklierkankercellen terwijl de blootstelling van normaal weefsel wordt beperkt, wat de kankerceldood vergroot en de beweging vermindert die tot uitzaaiing kan leiden. Hoewel deze bevindingen nog preklinisch zijn en de auteurs opmerken dat volledige dierexperimentele behandelingen en klinische proeven nodig zijn, legt het werk een solide basis voor gerichte nanomedicijnbenaderingen bij alvleesklierkanker en suggereert het een algemene strategie om andere veelbelovende natuurlijke moleculen om te zetten in praktische, tumorzoekende geneesmiddelen.
Bronvermelding: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Trefwoorden: alvleesklierkanker, nanoliposomen, gerichte medicijnafgifte, oridonine, tumor-homing peptide