Clear Sky Science · nl
Metadynamica onthult luteoline-gemedieerde conformationele stabilisatie tegen avapritinib-resistente PDGFRα D842V/G680R GIST
Waarom dit van belang is voor kankerbehandeling
Gerichte kankergeneesmiddelen kunnen opmerkelijk goed werken—totdat tumoren manieren ontwikkelen om eraan te ontsnappen. Dit artikel onderzoekt hoe een veelvoorkomende plantenverbinding, luteoline, mogelijk kan helpen de werkzaamheid te herstellen van een belangrijk middel tegen bepaalde gastro-intestinale stromatumoren (GIST), een type kanker in het spijsverteringskanaal. Met geavanceerde computersimulaties laten de onderzoekers zien hoe luteoline een misvormd eiwit in kankercellen zou kunnen stabiliseren zodat het bestaande geneesmiddel zich weer kan vasthechten, wat wijst op een nieuwe manier om medicatieresistentie te bestrijden zonder de behandeling helemaal opnieuw uit te vinden. 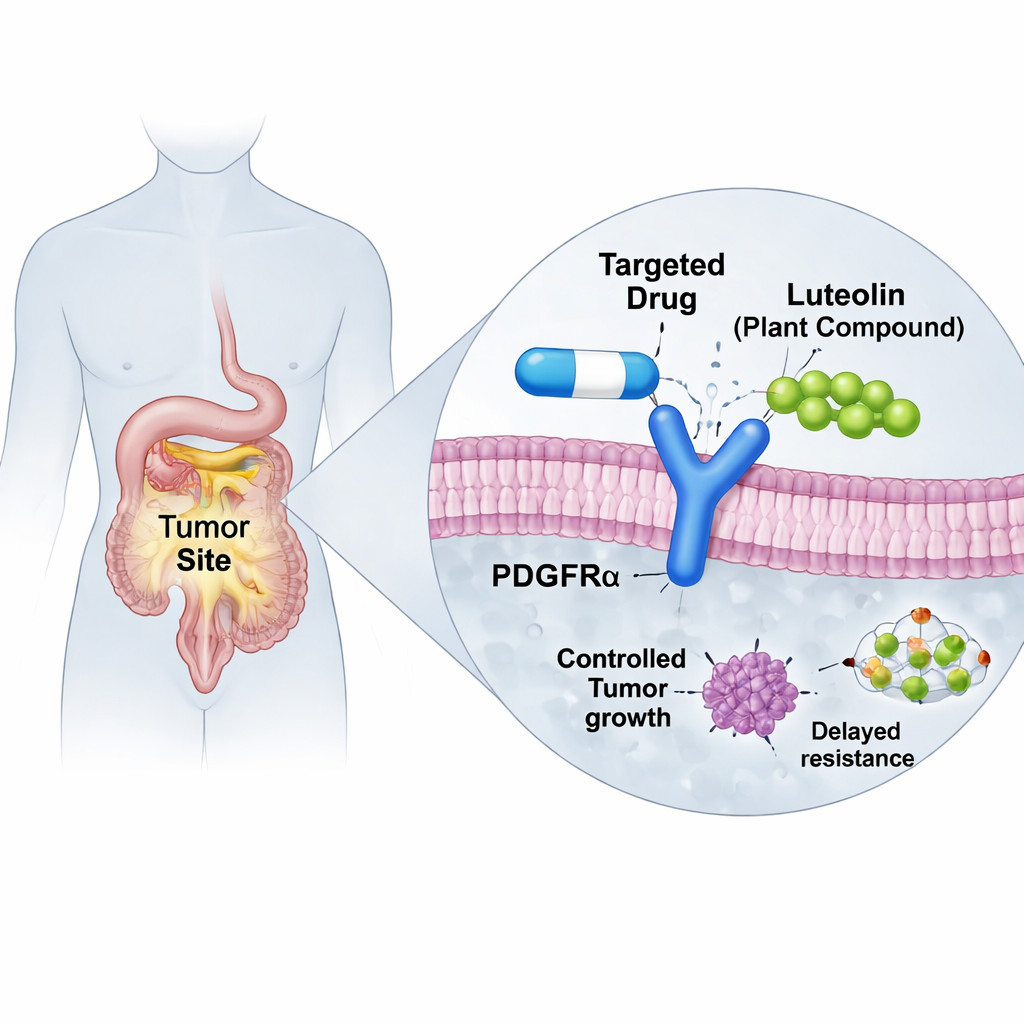
Het probleem van tumoren die leren geneesmiddelen te ontwijken
GISTs groeien vaak door defecte "aan-knoppen" in celmembraaneiwitten bekend als KIT of PDGFRα, die voortdurende groeisignalen aansturen. Moderne tabletten, tyrosinekinaseremmers genoemd, zijn ontworpen om deze schakelaars uit te zetten en hebben de uitkomsten voor veel patiënten sterk verbeterd. Maar een veelvoorkomende mutatie in PDGFRα, genaamd D842V, maakt het oudere middel imatinib grotendeels nutteloos. Een nieuwer geneesmiddel, avapritinib, is specifiek ontwikkeld om deze hardnekkige mutant te temmen en heeft opmerkelijk succes getoond in klinische studies. Helaas kunnen tumoren zich toch aanpassen. Sommige patiënten ontwikkelen bijkomende veranderingen in PDGFRα, zoals een secundaire G680R-mutatie, die fysiek verhinderend werkt voor avapritinib om comfortabel in zijn bindingspocket te passen, waardoor het medicijn uitvalt en resistentie toeneemt.
Een plantmolecuul met een intrigerende vorm
Natuurlijke producten vormen een rijke bron van ideeën voor geneesmiddelen, en flavonoïden—kleurige verbindingen die voorkomen in veel vruchten, groenten en medicinale planten—staan erom bekend dat ze interacties aangaan met eiwitten die groeiregulatie in cellen sturen. Luteoline, een van die flavonoïden die voorkomt in een Middellandse Zeestruik genaamd Retama monosperma, is al bestudeerd vanwege zijn antikanker- en ontstekingsremmende eigenschappen en lijkt veilig bij niveaus die met orale supplementen haalbaar zijn. Op basis van eerder screeningswerk vermoedden de auteurs dat luteoline aan PDGFRα zou kunnen binden op een plek nabij, maar niet overlappend met, de gebruikelijke geneesmiddelbindingssite. Als dat klopt, zou luteoline als een subtiele steun kunnen fungeren en het eiwit in een vorm kunnen duwen die avapritinib weer verwelkomt.
Het simuleren van een moleculair partnerschap
Om dit idee in silico te testen bouwde het team gedetailleerde driedimensionale computermodellen van het resistente PDGFRα-eiwit met zowel de D842V- als G680R-mutaties. Ze simuleerden het gedrag van avapritinib alleen en hoe het zich gedroeg wanneer luteoline in de buurt aanwezig was, en volgden atomaire bewegingen gedurende honderden nanoseconden—miljarden van een seconde in realtime. Wanneer alleen avapritinib gebonden was, dreef het medicijn geleidelijk uit zijn pocket naarmate de omvangrijke G680R-verandering het wegduwde, en raakte het volledig los van het eiwit. In contrast bleef avapritinib grotendeels op zijn plaats wanneer luteoline ook op een aparte “allosterische” site naast een sleutelhelix gebonden was. Het eiwit als geheel boog minder, belangrijke structurele segmenten behielden hun vorm, en essentiële contacten tussen het middel en het eiwit bleven veel langer bestaan. 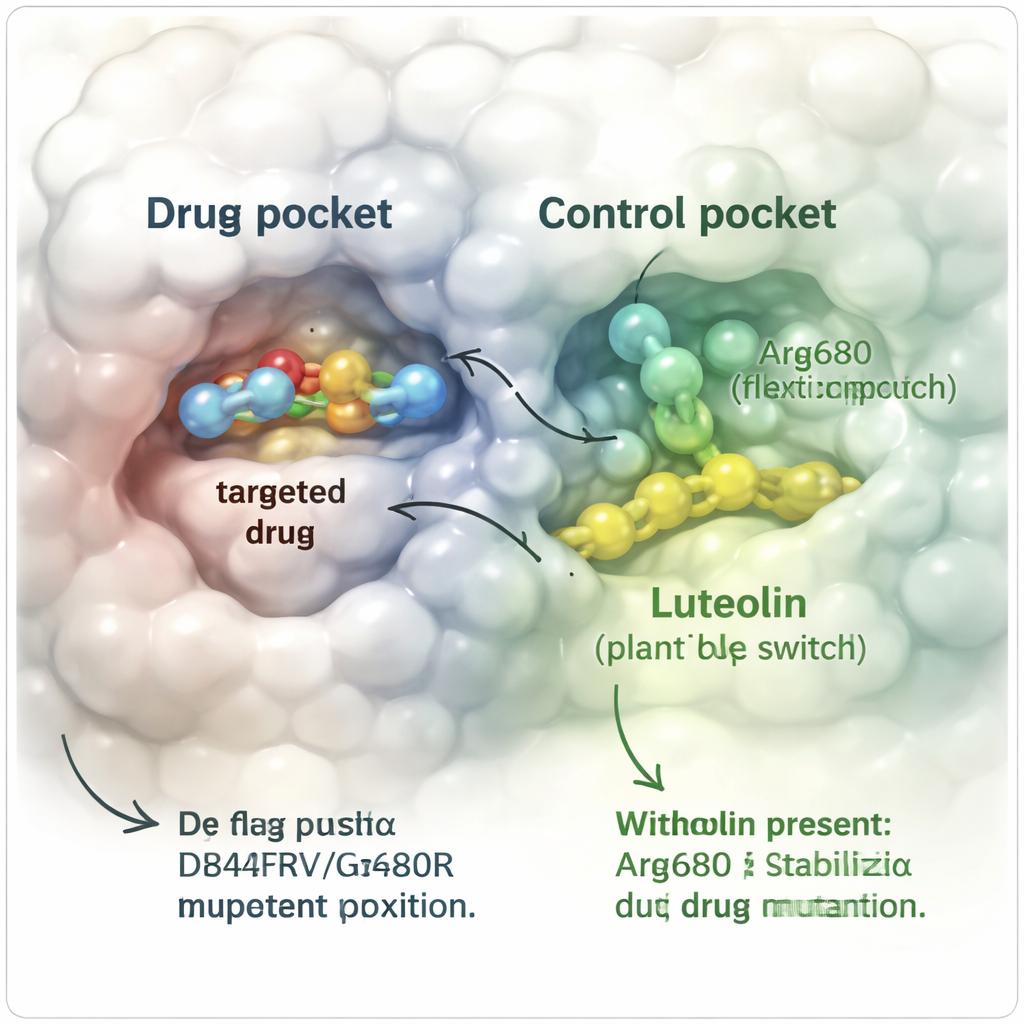
Een dwalende moleculaire schakel vastzetten
Standaard simulaties missen nog steeds zeldzame maar belangrijke vormveranderingen, dus schakelden de onderzoekers over op een verbeterde methode genaamd metadynamica om vollediger te verkennen hoe het eiwit zou kunnen draaien en buigen. Ze concentreerden zich op het gedrag van het gewijzigde aminozuur Arg680, dat fungeert als een klein flexibel armpje nabij de medicijnpocket. Zonder luteoline onderzocht dit armpje vele posities en gleed het middel gemakkelijk weg, met relatief lage energiebarrières om te ontsnappen. Met luteoline op zijn plek werd Arg680 in een specifieke oriëntatie gehouden die niet langer in conflict was met het geneesmiddel. Het energielandschap verschuifde: het systeem gaf nu de voorkeur aan conformaties waarin avapritinib gebonden bleef, en de energetische "heuvel" die het medicijn zou moeten beklimmen om te ontsnappen werd meerdere kilocalorieën hoger, waardoor dissociatie veel onwaarschijnlijker werd.
Wat dit voor patiënten zou kunnen betekenen
Simpel gezegd suggereert de studie dat luteoline kan werken als een moleculaire spalk, die een vervormd kankereiwit stabiliseert zodat een bestaand gerichte middel het weer stevig kan binden. In plaats van voor elke resistentiemutatie een geheel nieuw geneesmiddel te ontwerpen, kan het combineren van de huidige therapie met een zorgvuldig gekozen hulpverbinding de effectiviteit herstellen. Het werk is gebaseerd op krachtige maar louter computationele methoden, dus laboratorium- en dierstudies zijn nog nodig om te bevestigen of luteoline, of een verwant molecuul dat is geoptimaliseerd voor betere geneesmiddeleigenschappen, avapritinib in levende systemen daadwerkelijk versterkt. Toch zou het concept om kleine allosterische hulpstoffen te gebruiken om resistente kankertargets opnieuw te stabiliseren een nieuw pad kunnen openen om de levensduur van de huidige precisietherapieën te verlengen.
Bronvermelding: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Trefwoorden: medicatieresistentie, gastro-intestinaal stromatumor, tyrosinekinaseremmers, luteoline, allosterische modulatie